-
C、N、O、Na、Mg、Al、S、Cl是常见的八种元素,根据元素及其化合物性质,回答下列问题:
(1)S在周期表中的位置为______;CO2的电子式是_______。
(2)比较O、Na元素常见离子的半径大小(用化学式表示,下同)____>____;__________比较S、Cl元素的最高价氧化物对应水化物的酸性强弱: ____>____ 。_______________
(3)已知:
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
工业制镁时,电解MgCl2而不电解MgO的原因是___________;制铝时,电解Al2O3而不电解AlCl3的原因是___________ 。
(4)碳与镁形成的1 mol化合物Q与水反应,生成2 mol Mg(OH)2和1 mol烃, 该烃分子中碳氢质量比为9:1,烃的结构简式为______;Q的化学式为_______ 。
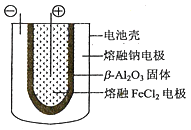
(5)熔融状态下,钠和FeCl2能组成可充电电池(装置示意图如下),反应原理为:2Na+ FeCl2 Fe + 2NaCl .放电时,电池的正极反应式为___________;充电时,_______(写物质名称)电极接电源的负极;该电池的电解质为_______。
Fe + 2NaCl .放电时,电池的正极反应式为___________;充电时,_______(写物质名称)电极接电源的负极;该电池的电解质为_______。
-
C、N、O、Na、Al、Si、S、Cl是常见的八种元素
请回答下列问题:
(1)Si在元素周期表中的位置为__ ;CO2的电子式是_______。
(2)上述元素中原子半径最大的是(写元素符号)______;最高价氧化物对应的水化物酸性最强的是__________(写化学式)。
(3)下列事实能说明O元素的非金属性比S元素的非金属性强的是__。
a.O2与H2S溶液反应,溶液变浑浊
b.O和S两元素的简单氢化物受热分解,前者的分解温度高
c.在氧化还原反应中,1molO2比1molS得电子多
(4)金刚石具有优良的耐磨,耐腐蚀性,应用广泛。一定条件下,Na还原CCl4可制备金刚石。反应结束冷却至室温后,回收其中的CCl4的实验操作名称为_____,除去粗产品中少里钠的试剂为_______。
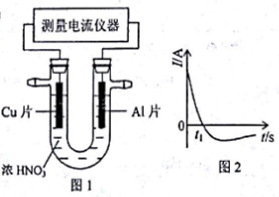
(5)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图l),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。0~t1时,原电池的负极是Al片,此时,正极的电极反应式是_______,溶液中的H+向__极移动。t1时,原电池中电子流动方向发生改变,其原因是:___________。
-
X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。据此回答下列问题:
(1)L的常见原子组成符号为 ;M在元素周期表中的位置为 ;五种元素的原子半径从大到小的顺序是 (用具体元素符号表示)。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为 ,B的结构式为 。Z和L也能组成原子数目比2∶4的分子C, 已知1 mol 液态C和液态B燃烧时生成无毒无害物质,并释放524.5 kJ的热量,试写出该反应的热化学方程式为 。
(3)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为 ,其最高价氧化物对应的水化物化学式为 。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是 (填字母代号)。
| A.+99.7 kJ·mol-1 | B.+29.7 kJ·mol-1 | C.-20.6 kJ·mol-1 | D.-241.8 kJ·mol-1 |
(4)用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R。写出阳极生成R的电极反应式: 。
-
下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
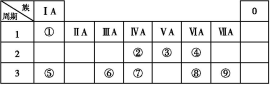
(1)已知由①、③、④三种元素组成的某种常见化合物的水溶液呈酸性,则符合该条件的化合物的化学式可能为 (至少写两种)。
(2)由表中①、④两种元素按原子个数比为1∶1构成的化合物的稀溶液易被催化分解,通常使用的催化剂为 (填序号)。
a、MnO2 b、FeCl3 c、Na2SO3 d、KMnO4
(3)下图中A~F是由部分上表中元素组成的单质或化合物,其中A、B、C为单质,转化关系如下:
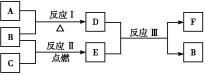
Ⅰ.若B为黄色固体,A为原子半径最小的原子组成的单质。
①F的电子式为 。
②实验测得起始参加反应的B和最后生成的B质量相等,则起始参加反应的A和C的物质的量之比是 。
Ⅱ.若D为淡黄色固体,焰色反应为黄色,组成C的元素的原子最外层电子数是内层电子数的2倍。
①下列关于D的说法正确的是 (填字母)。
a.能与水发生化合反应
b.既有氧化性,又有还原性
c.既含离子键,又含非极性共价键
d.是一种碱性氧化物
②用惰性电极将F的饱和溶液进行电解,则阳极反应式是 。
-
【化学-选修3 物质结构与性质】
铁和铜都是日常生活中常见的金属,有着广泛的用途。请回答下列问题:
(1)铁在元素周期表中的位置 。
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于______(填晶体类型).Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=______ 。Fe(CO)x在一定条件下发生反应:Fe(CO)x(s) Fe(s)+ xCO(g)。已知反应过程中只断裂配位键,则该反应生成物含有的化学键类型有 、 。
Fe(s)+ xCO(g)。已知反应过程中只断裂配位键,则该反应生成物含有的化学键类型有 、 。
(3)k3[Fe(CN)6]溶液可用于检验 (填离子符号)。CN-中碳原子杂化轨道类型为 ,C、N、O三元素的第一电离能由大到小的顺序为 (用元素符号表示)。
(4)铜晶体铜碳原子的堆积方式如图所示。

①基态铜原子的核外电子排布式为 。
②每个铜原子周围距离最近的铜原子数目 。
(5)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如图所示(黑点代表铜原子)。

①该晶体的化学式为 。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于 (填“离子”、“共价”)化合物。
③已知该晶体的密度为ρg.cm-3,阿伏伽德罗常数为NA,
则该晶体中铜原子和M原子之间的最短距离为 pm(只写计算式)。
-
如表所示为元素周期表的一部分,参照元素①~⑩在表中的位置,请回答下列问题:

(1)写出①和④两种元素原子按1:1组成的常见化合物的电子式______。
(2)用电子式表示⑥和⑨形成化合物的过程:______。
(3)③、⑧、⑩的最高价氧化物对应水化物的酸性由强到弱的顺序为 ______(用化学式表示)。
(4)已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式 ______。
(5)⑤、⑥、⑩的离子半径由大到小的顺序为 ______(用离子符号表示)。
-
下表为部分短周期元素化合价及其相应原子半径的数据。请回答下列问题:
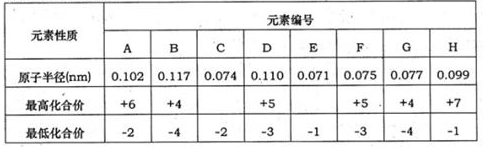
(1)元素G在周期中的位置是________;元素F所形成的常见单质的电子式为________。
(2)A、B、C、E的氢化物稳定性顺序是________。(用化学式回答)
(3)分子组成为ACH2的物质在水中会强烈水解,产生使品红溶液褪色的无色气体和一种强酸。该反应的化学方程式是________。
(4)请写出B的单质的一种重要用途________;工业上制取该单质的原理反应为 ________。
(5)请设计一个实验方案,使铜和A的最高价氧化物对应的水化物的稀溶液反应,得到蓝色溶液和氢气。请在方框内绘出该实验方案原理装置示意图。

-
已知B、C为常见的两种金属单质,E、I为常见的两种非金属单质,A为硫酸盐反应②为D的溶液与C在加热条件下的反应,P溶液和G溶液中具有相同的阳离子,请根据要求回答下列问题.

(1)B元素在周期表的位置:______,
(2)物质I的电子式:______.
(3)Y转变为X的现象是:______.涉及的反应方程式为:______.
(4)写出反应④的化学反应方程式:______.物质F与HI水溶液的离子反应方程式 式:______.
(5)向沸水中加入H的饱和溶液,可得到红褐色溶液,其溶液所具有性质______.
A.具有丁达尔效应
B.处加直流电源阳极附近溶液颜色加深
C.加入盐酸溶液出现先沉淀后溶解的现象
D.能透过半透膜,不能透过滤纸
(6)向含1molG的溶液中加入1molNa2O2,所发生的离子反应方程式:______.
-
图1是部分短周期元素的常见化合价与原子序数的关系图:
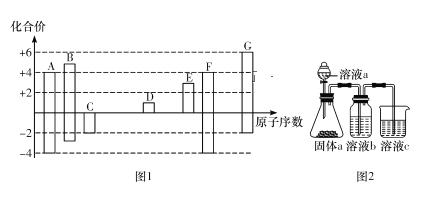
请回答下列问题:
(1)元素F在周期表中的位置为________________
(2)C、D、E、G的简单离子半径由大到小的顺序为_______________(用离子符号表示)。
(3)二元化合物X是含有元素A的18电子分子,3 g X(g)在25 ℃ 101 kPa 下完全燃烧生成稳定的化合物时放出Q kJ的热量,写出表示X燃烧热的热化学方程式:________________
(4)某同学设计实验用图2所示装置证明元素A、B、F的非金属性强弱(其中溶液b和溶液c均足量)。
①溶液b为_________________
②溶液c中发生反应的离子方程式为__________________
-
图1是部分短周期元素的常见化合价与原子序数的关系图:
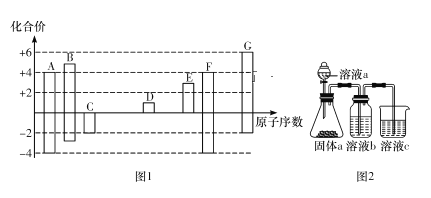
请回答下列问题:
(1)元素F在周期表中的位置为________________
(2)C、D、E、G的简单离子半径由大到小的顺序为_______________(用离子符号表示)。
(3)二元化合物X是含有元素A的18电子分子,3 g X(g)在25 ℃ 101 kPa 下完全燃烧生成稳定的化合物时放出Q kJ的热量,写出表示X燃烧热的热化学方程式:________________
(4)某同学设计实验用图2所示装置证明元素A、B、F的非金属性强弱(其中溶液b和溶液c均足量)。
①溶液b为_________________
②溶液c中发生反应的离子方程式为__________________











