-
为了验证干燥的氯气无漂白性,湿润的氯气具有漂白性,某同学设计实验如下图。其中B、C、D、E、F分别盛有饱和食盐水、浓硫酸。干燥红色布条、浓硫酸、湿润红色布条。

请回答:
(1)E中浓硫酸的作用____________。
(2)将F中的湿润布条换成卷曲的细铜丝,并用酒精灯加热,可看到的现象是_____________。
(3)若用装置A制取2.24L(标况)氯气,消耗10mol/L浓盐酸的体积明显大于40mL,造成该结果的可能原因有______________。
A.浓盐酸的挥发 B.随反应进行盐酸浓度下降
C.加热时火力不够猛 D.MnO2固体过量
-
(12分)某同学设计的制取氯气和验证氯气部分化学性质的实验装置如下图甲所示:
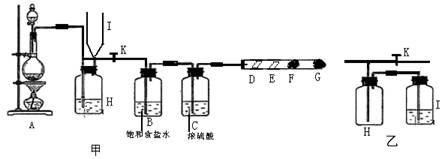
其中D处放有干燥的紫色石蕊试纸,E处放有湿润的紫色石蕊试纸, F、G处依次放有喷上少量淀粉KI溶液、浓NaOH溶液的棉球。回答下列问题:
(1)在装置A中放入有关药品后,打开活塞K,将分液漏斗中的液体加入烧瓶中,关闭分液漏斗的活塞,点燃酒精灯,请写出A处反应的离子方程式:
________
(2)B处饱和食盐水是为了除去________,C处浓硫酸的作用是________。
(3)实验中可观察到颜色的变化:D处________,E处________,F处________,G处棉球的作用是________,G处反应的离子方程式________。
(4)当F处棉球变色,立即关闭活塞K,可看到I瓶中液面上升,H瓶中充满黄绿色气体。则H瓶中加入的液体一般为________,甲中H—I装置的作用为________。若将甲中的H—I装置置换为乙装置,是否可行(填“是”或“否”)________,理由是________。
-
氯仿(CHC13)是无色透明液体,不溶于水和浓硫酸,溶于醇,沸点为61.2℃,工业品氯仿中常含有少量乙醇。某校同学设计实验制备少量氯仿。
(1)甲组同学设计下列装置用干燥纯净的氯气制备实验原料漂白粉[已知:3Ca(ClO)2  Ca(ClO3)2+2CaCl2 △H>0]。
Ca(ClO3)2+2CaCl2 △H>0]。
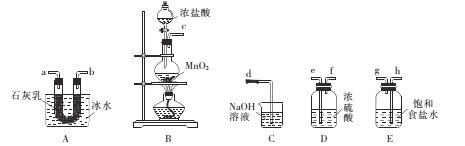
①各仪器接口连接顺序为____(气流白左至右,用小写字母表示)。
②装置B中发生反应的离子方程式为 ___。
③装置A用冰水冷却的目的是____。
(2)乙组同学用甲组制得的漂白粉与乙醇溶液反应制备氯仿的实验装置如图。
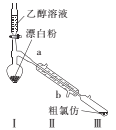
①装置I需控制温度约为70℃,适宜的加热方式是 ___,温度不宜过高,其目的是____。
②装置Ⅱ的名称是____。
③一定条件下,装置I中漂白粉先与乙醇溶液反应生成Cl2和Ca(OH)2,然后Cl2与CH3CH2OH反应生成CCl3CHO,CCl3CHO再与Ca(OH)2反应生成CHC13和一种盐,CCl3CHO与Ca(OH)2反应的化学方程式为 _________。
(3)丙组同学用下列方法对乙组制得的粗产品进行提纯。已知浓硫酸能与乙醇混溶。
步骤I.向粗产品中加入适量浓硫酸,搅拌至呈淡咖啡色,分液得有机层;
步骤Ⅱ.用15%的Na2CO3溶液洗涤多次,分液得有机层;
步骤Ⅲ.向有机层中加入少量无水CaCl2。
步骤I中用浓硫酸洗涤的目的是____;步骤Ⅱ中证明已洗涤干净的依据是____;步骤Ⅲ中加入少量无水CaCl2的目的是 ___。
-
某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4 2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
2CaSO4+2Cl2↑+2H2O 。他们设计了如下制取氯气并验证其性质的实验。
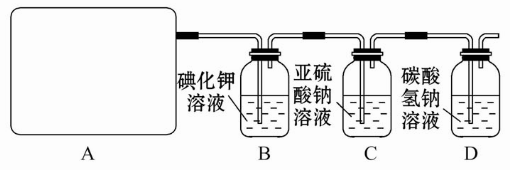
试回答:(1)该实验中A部分的装置是____(填写装置的序号)。
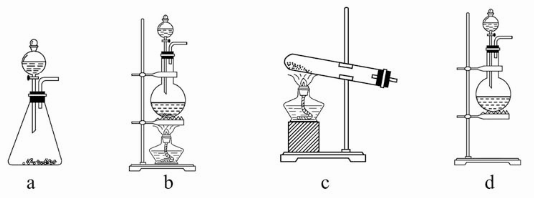
(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):____________________________。
(3)若D中反应后的溶液具有漂白性,请写出D装置中发生反应的离子方程式
__________________。
(4)该实验存在明显的缺陷,请你提出改进的方法___________。
(5)该小组又进行了如下实验:称取漂白粉2.0 g ,研磨后溶解,配制成250 mL溶液,取25 mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置。待完全反应后,用0.1 mol/L的Na2S2O3溶液作标准溶液滴定反应生成的碘,已知反应式为: 2Na2S2O3+I2=Na2S4O6 + 2NaI 反应完成时,共用去Na2S2O3
20.0 mL。则该漂白粉中Ca(ClO)2的质量分数为:_____________。
-
研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4
 2CaSO4+2Cl2↑+2H2O.他们设计了如下制取氯气并验证其性质的实验.
2CaSO4+2Cl2↑+2H2O.他们设计了如下制取氯气并验证其性质的实验.
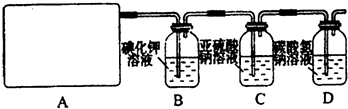
试回答:(1)该实验中A部分的装置是______(填写装置的序号).
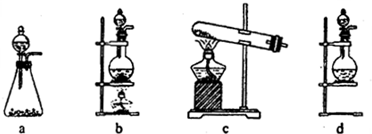
(2)(1)选项中d装置的两个主要的玻璃器皿的名称分别是______、______.
(3)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):______.
(4)分别写出C装置、D装置发生反应的离子方程式______.
(5)该实验存在明显的缺陷,请你从化学反应的视角提出改进的方法是______.所发生反应的化学方程式是______.
(6)该小组又进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取25mL加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置.待完全反应后,用0.1mol/L的Na2S2O3溶液作标准溶液滴定反应生成的碘,已知反应方程式为:
2Na2S2O3+I2═Na2S4O6+2NaI 反应完成时,共用去Na2S2O3 20.0mL.则该漂白粉中Ca(ClO)2的质量分数为______.(保留至0.01%)
-
某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4
 2CaSO4+2Cl2↑+2H2O.他们设计了如下制取氯气并验证其性质的实验.
2CaSO4+2Cl2↑+2H2O.他们设计了如下制取氯气并验证其性质的实验.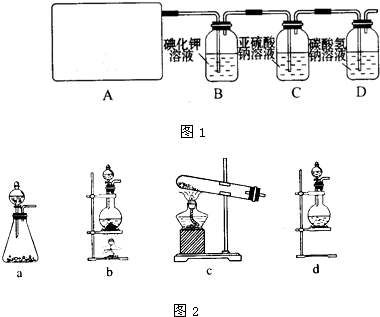
试回答:
(1)该实验中图1A部分的装置是图2________(填写装置的序号).
(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):________.
(3)写出D装置中发生反应的离子方程式________.
(4)该实验存在明显的缺陷,请你提出改进的方法________.
-
利用如图所示装置,在仪器①②③中分别依次加入下列各选项中所对应的试剂进行实验,能达到实验目的的是
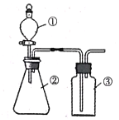
A. 浓盐酸、浓硫酸、浓硫酸,制取干燥的氯化氢气体
B. 浓盐酸、二氧化锰、饱和食盐水,制取纯浄的氯气
C. 稀硫酸、溶液X、澄清石灰水,检验溶液X中是否含有CO32—
D. 浓盐酸、碳酸钙、水玻璃,验证盐酸、碳酸、硅酸的酸性强弱
-
利用如图所示装置,在仪器①②③中分别依次加入下列各选项中所对应的试剂进行实验,能达到实验目的的是

A. 浓盐酸、浓硫酸、浓硫酸,制取干燥的氯化氢气体
B. 浓盐酸、二氧化锰、饱和食盐水,制取纯浄的氯气
C. 稀硫酸、溶液X、澄清石灰水,检验溶液X中是否含有CO32—
D. 浓盐酸、碳酸钙、水玻璃,验证盐酸、碳酸、硅酸的酸性强弱
-
下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将干燥纯净的氯气通入装有湿润的红色纸条的试剂瓶中 | 红色褪去 | 干燥的氯气有漂白性 |
| B | 往乙醇中加入适量浓硫酸制备乙烯,并将产生的气体直接通入酸性KMnO4溶液中 | 酸性KMnO4溶液紫红色褪去 | 证明乙烯能被酸性高锰酸钾氧化 |
| C | 取少量BaSO4固体于试管中,加入足量的盐酸 | 固体不溶解 | BaSO4不溶于盐酸,且可以用盐酸和BaCl2溶液检验SO42— |
| D | 在分液漏斗中加入碘水后再加入CCl4,充分振荡 | 分层,且上层溶液呈紫色 | CCl4可作为碘的萃取剂 |
-
下列实验操作中现象以及结论均正确的是
| 实验操作 | 现象 | 结论 |
| A | 将干燥纯净的氯气通入装有湿润的红色纸条的试剂瓶中 | 纸条褪色 | 氯气有漂白性 |
| B | 将一定量的浓硫酸加入蔗糖 | 固体变黑膨胀 | 浓硫酸有吸水性和强氧化性 |
| C | 向酸性KMnO4溶液中通入SO2气体 | KMnO4溶液褪色 | SO2有还原性 |
| D | 金属钠投入CuSO4溶液 | 析出红色固体 | 钠的金属性比铜强 |










