-
(12分)铜及其化合物在工农业生产及日常生活中应用非常广泛。某研究小组用粗铜(含杂质铁)制备氯化铜晶体(CuCl2.2H2O)的流程如下。
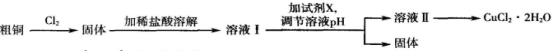
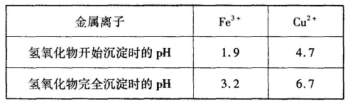
已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
请回答下列问题:
(1)溶液I中加入试剂X可以调节溶液pH,从而除去Fe3+且不引入杂质。
①试剂X可选用下列物质中的__________(填代号)。
a.CuO b.NaOH c.Cu d.Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是__________。
(2)由溶液Ⅱ制备CuCl2.2H2O的操作依次为:边滴加浓盐酸边加热浓缩、__________(填操作名称)、过滤、洗涤干燥。
(3)向溶液Ⅱ中通入H2S气体,溶液变浑浊,pH减小,用离子方程式解释其原因:__________.
(4)某学习小组用碘量法测定CuCl2.2H2O样品的纯度(杂质不与发生反应)。实验如下:
a.准确称取CuCl2.2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250 mL待测溶液。(已知: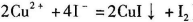 )
)
b.移取25. 00 mL待测溶液于锥形瓶中,加几滴指示剂,用c mol Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL。 (已知:
Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL。 (已知: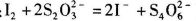 )
)
①实验中使用的指示剂名称为____________。
②达到滴定终点时,仰视滴定管读数将使测定结果_________(填“偏高”、“偏低”或“无影响”)。
③该样品中CuCl2.2H2O 的质量分数为_________(用含m、c、V的代数式表示,不用化简)。
-
铜及其化合物在工农业生产及日常生活中应用非常广泛。某研究小组用粗铜(含杂质铁)制备氯化铜晶体(CuCl2·2H2O )的流程如下。

已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| 金属离子 | Fe3+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 6.7 |
请回答下列问题:
(1)溶液I中加入试剂X可以调节溶液pH,从而除去Fe3+且不引入杂质。
①试剂X可选用下列物质中的__________(填代号)。
a.CuO b.NaOH c.Cu d..Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是__________。
(2)由溶液Ⅱ制备CuCl2·2H2O的操作依次为:边滴加浓盐酸边加热浓缩、__________(填操作名称)、过滤、洗涤干燥。
(3)向0.1 mol·L-1的CuCl2溶液中通入H2S气体,溶液变浑浊,pH减小,用离子方程式解释其原因: 若KSP[CuS]=1.2×10-36 ,则生成沉淀时需要S2-的浓度为 mol·L-1。
(4)某学习小组用碘量法测定CuCl2·2H2O样品的纯度(杂质不发生反应)。实验如下:
a.准确称取CuCl2·2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250 mL待测溶液。(已知:2Cu2++4I-=2CuI+I2)
b.移取25.00 mL待测溶液于锥形瓶中,加几滴指示剂,用c mol·L-1Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL。(已知:I2+2S2O32-=2I-+S4O62-)
①实验中使用的指示剂名称为____________,达到滴定终点时,溶液颜色变化为 。
②该样品中CuCl2·2H2O 的质量分数为_________(用含m、c、V的代数式表示,不用化简)。
-
铜及其化合物在工农业生产及日常生活中应用非常广泛。某研究小组用粗铜(含杂质铁)制备氯化铜晶体(CuCl2·2H2O)的流程如下:

已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| 金属离子 | Fe3+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 6.7 |
请回答下列问题:
(1)溶液Ⅰ中加入试剂X可以调节溶液pH,从而除去Fe3+且不引人杂质
①试剂X选用下列物质中的_______(填代号)。
a.NaOH b.CuO c.Cu d.Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是____________________________。
(2)检验溶液Ⅰ中的存在Fe3+实验操作是_____________________。
(3)向溶液Ⅱ中通入H2S气体,溶液变浑浊,pH减小,用离子方程式解释其原因________________;
(4)某学习小组用碘量法测定CuCl2•2H2O样品的纯度(杂质不参与反应),实验如下:
a.准确称取CuCl2•2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250mL待测溶液.(已知:2Cu2++4I-═2Cu↓+I2)
b.移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用cmol•L-1Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为VmL.(已知:I2+2S2O32-═2I-+S4O62-)
①实验中使用的指示剂名称为___________;
②达到滴定终点时,仰视滴定管读数将使测定结果__________(填“偏高”“偏低”或“无影响”)
③该样品中的质量分数为__________(用含m,c,V的代数式表示,不用化简)。
(5)在空气中由CuCl2•2H2O晶体得到纯的无水CuCl2的合理方法是________________。
-
(6分)氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体(CuCl2·2H2O)。
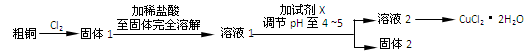
(1)实验室采用如下图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。

① 仪器A的名称是________。
② 装置B中发生反应的离子方程式是________。
③ 有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”)________。
④ NaOH溶液的作用________
(2)试剂X用于调节pH以除去杂质, X可选用下列试剂中的(填序号)________。
a.NaOH b.NH3·H2O c.CuO d.Cu2(OH) 2CO3 e.CuSO4
-
氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体(CuCl2·2H2O)。
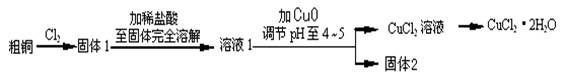
(1)实验室采用如下图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。

① 仪器A的名称是 。
② 装置B中发生反应的离子方程式是 。
③ 有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”) 。
④装置Ⅳ中盛装的试剂是________,其作用是________。
(2)在CuCl2溶液转化为CuCl2·2H2O的操作过程中,发现溶液颜色由蓝色变为黄绿色。小组同学欲探究其原因。
已知:在氯化铜溶液中有如下转化关系:
Cu(H2O)42+(aq) +4Cl-(aq) CuCl42-(aq) +4H2O(l)
CuCl42-(aq) +4H2O(l)
蓝色 黄色
①上述反应的化学平衡常数表达式是K= 。
若增大氯离子浓度,K值(填“增大”、“减小”或“不变”) 。
②现欲使溶液由黄色变成黄绿色或蓝色,请写出两种可采用的方法
a.________ b.________。
-
氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。某研究小组用粗铜(含杂质Fe)按下述流程制备氯化铜晶体(CuCl2·2H2O)。
(1)实验室采用如下图所示的装置,可将粗铜与Cl2反应转化为固体1(部分仪器和夹持装置已略去)。

① 仪器A的名称是 。
② 装置B中发生反应的离子方程式是 。
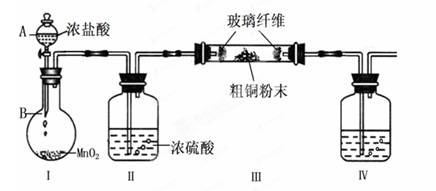 ③ 有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”) 。
③ 有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”) 。
④装置Ⅳ中盛装的试剂是________,其作用是________。
(2)在CuCl2溶液转化为CuCl2·2H2O的操作过程中,发现溶液颜色由蓝色变为黄绿色。小组同学欲探究其原因。
已知:在氯化铜溶液中有如下转化关系:
Cu(H2O)42+(aq) +4Cl-(aq) CuCl42-(aq) +4H2O(l)
CuCl42-(aq) +4H2O(l)
蓝色 黄色
① 上述反应的化学平衡常数表达式是K= 。若增大氯离子浓度,K值(填“增大”、“减小”或“不变”) 。
② 现欲使溶液由黄色变成黄绿色或蓝色,请写出两种可采用的方法
a.________ b.________。
-
氯化物在工业生产、日常生活中应用都非常广泛。某学习小组为探究一些实用性很强的氯化物,进行了一系列的资料查询与具体实验。
(1)用于制造电池的原材料二氯亚砜(SOCl2),是一种液态化合物,沸点为77℃。在盛10mL水的锥形瓶中小心滴加8~10滴SOCl2可观察到剧烈反应,液面上形成白雾,并逸出刺激性气味的气体,该气体可使沾有品红试液的滤纸褪色。轻轻振荡锥形 瓶,待白雾消失后往溶液中滴加AgNO3溶液,有不溶于稀HNO3的白色沉淀析出。室温下,小组某同学取2.38g SOCl2与水发生上述反应,测得放出热量为17.88 kJ。根据以上实验,写出SOCl2与水反应的热化学方程式_______________________。
瓶,待白雾消失后往溶液中滴加AgNO3溶液,有不溶于稀HNO3的白色沉淀析出。室温下,小组某同学取2.38g SOCl2与水发生上述反应,测得放出热量为17.88 kJ。根据以上实验,写出SOCl2与水反应的热化学方程式_______________________。
(2)低温蒸干AlCl3溶液得到固体的主要成分是___________;小组某同学想制取无水Al Cl3固体,他提出可以用AlCl3·6H2O与SOCl2混合后共热来制取无水AlCl3固体,你认为可行吗?请说明原因______________。
Cl3固体,他提出可以用AlCl3·6H2O与SOCl2混合后共热来制取无水AlCl3固体,你认为可行吗?请说明原因______________。
(3)TiO2是一种非常好的催化剂。某同学通过查阅资料显示:TiCl4水解程度很大,可以用于TiO2的制备,制备时加入大量的水,同时加热,促进水解趋于完全,所得TiO2·xH2O经焙烧得TiO2。请写出TiCl4水解的化学方程式__________________________。
(4)某同学利用NaCl溶液设计实验验证Fe在原电池反应中的生成物,使用Cu电极、Fe电极、经过酸化的3%NaCl溶液,组成原电池装置,实验结束后,该同学往Fe电极区滴入2滴黄色铁氰化钾溶液,现象是:______________________________。
-
铁、铜等金属及其化合物在日常生产生活中用途非常广泛.
Ⅰ.实验室欲制备0.3mol Cu(NO3)2晶体,甲、乙两同学分别设计实验方案如下:
甲:Cu Cu(NO3)2 ;乙:Cu
Cu(NO3)2 ;乙:Cu CuO
CuO  Cu(NO3)2
Cu(NO3)2
(1)从绿色化学的角度分析,___________同学的方案更合理
(2)乙同学实验时通入O2的速率不宜过大,为便于观察和控制产生O2的速率,宜选择__________装置(填字母序号)。

Ⅱ.某化学实验小组通过实验来探究一包黑色粉是否由Fe3O4、CuO组成探究过程如下:
(1)提出假设:
假设1.黑色粉末是CuO;
假设2.黑色粉末是Fe3O4;
假设3.黑色粉末是CuO和Fe3O4的混合物。
(2)设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
①若假设1成立,则实验现象是溶液显蓝色。
②若假设2或3成立,则实验现象是__________。
为进一步探究,继续向所得溶液加入足量铁粉,若产生_________的现象,则假设3成立。
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。
为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若假设2成立,则产生__________现象;若假设3成立,则产生________现象。
Ⅲ.由Fe3O4、FeO、CuO、Fe组成的固体混合物,在加热条件下用足量的CO还原,得到金属混合物2.86g,将生成的CO2气体用足量的澄清石灰水吸收后,产生5.00g白色沉淀。固体混合物的质量是________。
-
(12分)铁、铜单质及其化合物应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O), 为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:
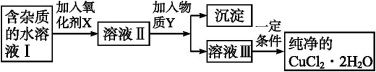
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见下表:
| Fe3+ | Fe2+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.0 | 6.7 |
请回答下列问题:
(1)得到溶液II,需加入氧化剂X, 最适合作氧化剂X的是 。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)加入氧化剂X的目的是 。
(3)为了除去Fe3+,需加入物质Y调节溶液的PH值为
(4)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体? (填“能”或“不能”)。若能,不用回答;若不能,回答该如何操作? 。
(5)已知Fe(OH)3的Ksp=1×10-35mol4/L4 ;若Fe3+沉淀完全时,在溶液中Fe3+的浓度为1×10-5mol/L, 则此时溶液的PH最小为 .
-
(17分)铁、铜单质及其化合物应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:
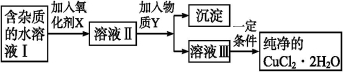
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见下表:
| Fe3+ | Fe2+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.0 | 6.7 |
请回答下列问题:
(1)加入氧化剂的目的是 。
(2)最适合作氧化剂X的是 。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)加入的物质Y是 。
(4)若不用物质Y而是直接用碱能不能达到目的? (填“能”或“不能”)。若不能,试解释原因 。
(5)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体? (填“能”或“不能”)。若能,不用回答;若不能,回答该如何操作? 。
(6)若向溶液Ⅱ中加入碳酸钙,产生的现象是 。(3分)
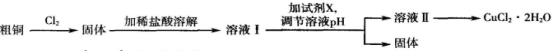

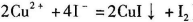 )
)Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL。 (已知:
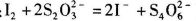 )
)






 ③ 有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”)
③ 有同学认为应在浓硫酸洗气瓶前增加吸收HCl的装置,你认为是否必要(填“是”或“否”)

