-
(1)已知天然气和水蒸气反应的热化学方程式为:CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.4kJ•mol-1,则制得56g CO需要吸收的热量为________ kJ;
(2)CO可继续与水蒸气反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.0kJ•mol-1,若将1mol CH4与足量水蒸气充分反应得到1molCO2,该反应的焓变△H=________kJ•mol-1.高二化学填空题中等难度题查看答案及解析
-
(6分)(1)已知天然气和水蒸气反应的热化学方程式为:CH4(g) + H2O(g)
CO(g)+ 3H2(g) ΔH = +206.4kJ·mol-1,则制得56g CO需要吸收的热量为 ________ kJ;
(2)CO可继续与水蒸气反应:CO(g)+H2O(g)
CO2(g)+H2(g) ΔH =-41.0kJ·mol-1 ,若将1mol CH4与足量水蒸气充分反应得到1molCO2,该反应的焓变ΔH =________kJ·mol-1。
高二化学填空题中等难度题查看答案及解析
-
甲烷液化可获得工业原料甲醇,反应原理是:
①CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH1=+206.4 kJ·mol-1
②CO(g)+H2O(g)===CO2(g)+H2(g) ΔH2=-41.0 kJ·mol-1
③CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH3=-49.0 kJ·mol-1
下列说法不正确的是
A. 升高温度,反应①中CH4转化率提高
B. 反应③是CO2资源化利用的方法之一
C. CO(g)+2H2(g)===CH3OH(g) ΔH=-90.0 kJ·mol-1
D. 上述合成甲醇过程中需要向原料气中补充H2
高二化学单选题中等难度题查看答案及解析
-
第一题:已知:
①CH4(g) + H2O(g)
CO(g) + 3H2(g) ∆H1 = +206.4 kJ/mol
②CO(g) + H2O(g)
CO2(g) + H2(g) ∆H2 = -41.0 kJ/mol
③CH4 (g) + 2H2O(g)
CO2(g) + 4H2(g) ∆H3
请回答:
(1)反应①属于 (填“吸热”或“放热”)反应。
(2)反应①消耗8 g CH4 (g)时,∆H = kJ/mol。
(3)反应②生成2 mol H2(g)时,∆H = ___________ kJ/mol。
(4)反应③的∆H3 =___________ kJ/mol。
第二题:在容积为1.00 L的密闭容器中,通入一定量的N2O4,发生反应:N2O4(g)
2NO2(g)。100℃时,各物质浓度随时间变化如下图所示。

请回答:
(1)60 s内,v(N2O4) = mol/(L·s)。
(2)若升高温度,混合气体的颜色变深,则正反应是 (填“放热”或“吸热”)反应。
(3)100℃时,该反应的化学平衡常数数值为 。
(4)平衡时,N2O4的转化率是 。
高二化学填空题困难题查看答案及解析
-
氮气氢气合成氨过程中制氢气的原理如下:
①CH4(g)+H2O(g)
CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
②CO(g)+H2O(g)
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
(1)对于反应①,一定可以提高平衡体系中H2的百分含量,又能加快反应速率的措施是_______。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
(2)利用反应②,将CO进一步转化,可提高H2的产量。若1 mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18 mol CO、CO2和H2的混合气体,则CO的转化率为________。
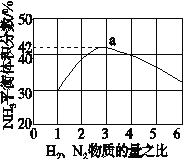
(3)图(a)表示500 ℃、60.0 MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:____________。
(4)依据温度对合成氨反应的影响,在图(b)坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图________。
高二化学综合题困难题查看答案及解析
-
(1)氨的合成是最重要的化工生产之一,工业上合成氨用的H2有多种制取的方法。用天然气跟水蒸气反应:CH4(g)+H2O(g)
CO(g)+3H2(g)。已知有关反应的能量变化如下图所示,则此制取H2反应的ΔH=____________。

(2)已知通常状况下,每充分燃烧1gCO并恢复到原状态,会释放10KJ的热量。请写出表示CO燃烧热的热化学反应方程式: 。
(3)一种甲烷燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸电解液中直接通入甲烷,同时向一个电极通入空气。此电池的正极电极反应式是__________________。
(4)利用右图装置可以模拟铁的电化学防护。

①若X为碳棒,为减缓铁的腐蚀,开关K应置于 处。
假设海水中只有NaCl溶质,写出此时总离子反应方程式:
②若X为锌,开关K置于M处,该电化学防护法称为 。写出铁电极处的电极反应式:____________。
高二化学填空题中等难度题查看答案及解析
-
(14分)(1)氨的合成是最重要的化工生产之一,工业上合成氨用的H2有多种制取的方法。用天然气跟水蒸气反应:CH4(g)+H2O(g)
CO(g)+3H2(g)。已知有关反应的能量变化如下图所示,则此制取H2反应的ΔH=____________。

(2)已知通常状况下,每充分燃烧1gCO并恢复到原状态,会释放10KJ的热量。请写出表示CO燃烧热的热化学反应方程式: 。
(3)一种甲烷燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸电解液中直接通入甲烷,同时向一个电极通入空气。此电池的负极电极反应式是________________________________________________。
(4)利用下图装置可以模拟铁的电化学防护。

①若X为碳棒,为减缓铁的腐蚀,开关K应置于 处。假设海水中只有NaCl溶质,写出此时总离子反应方程式: 。
②若X为锌,开关K置于M处,该电化学防护法称为 。
写出铁电极处的电极反应式: 。
高二化学填空题困难题查看答案及解析
-
(1)氨的合成是最重要的化工生产之一,工业上合成氨用的H2有多种制取的方法。用天然气跟水蒸气反应:CH4(g)+H2O(g)
 CO(g)+3H2(g)。已知有关反应的能量变化如下图所示,则此制取H2反应的ΔH=____________。
CO(g)+3H2(g)。已知有关反应的能量变化如下图所示,则此制取H2反应的ΔH=____________。
(2)已知通常状况下,每充分燃烧1gCO并恢复到原状态,会释放10KJ的热量。请写出表示CO燃烧热的热化学反应方程式:________________________________。
(3)一种甲烷燃料电池是采用铂或碳化钨作为电极催化剂,在稀硫酸电解液中直接通入甲烷,同时向一个电极通入空气。此电池的负极电极反应式是_______________。
(4)利用右图装置可以模拟铁的电化学防护。

① 若X为碳棒,为减缓铁的腐蚀,开关K应置于______处。假设海水中只有NaCl溶质,写出此时总离子反应方程式:__________________________________________。
② 若X为锌,开关K置于M处,该电化学防护法称为_________。写出铁电极处的电极反应式:_____________________________。
高二化学填空题困难题查看答案及解析
-
合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料.从天然气获得合成气过程中可能发生的反应有:
①CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H1=+206.1kJ/mol
②CH4(g)+CO2(g)⇌2CO(g)+2H2(g)△H2=+247.3kJ/mol
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示.反应进行的前5min内,v(H2)=______;10min时,改变的外界条件可能是______.
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等.在相同温度下发生反应②,并维持反应过程中温度不变.已知甲容器中CH4的转化率随时间变化的图象如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象______.
(3)反应③中△H3=______.800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
此时反应③中正、逆反应速率的关系式是______(填代号).CO H2O CO2 H2 0.5mol 8.5mol 2.0mol 2.0mol
a.v(正)>v(逆) b.v(正)<v(逆) c.v(正)=v(逆) d.无法判断.高二化学解答题中等难度题查看答案及解析
-
对于制氢气原理CH4(g)+H2O(g)
CO(g)+3H2(g)ΔH=+206.4 kJ·mol-1,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是
A.降低压强 B.增大水蒸气浓度 C.加入催化剂 D.升高温度
高二化学选择题中等难度题查看答案及解析