-
(15分)
短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层之和为13;B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素;D、E形成的单质在不同条件下可以生成两种不同的离子化合物;F是同周期元素中原子半径最小的。
(1)A、D以1 :1形成化合物的电子式为________。A、C形成最简单化合物的空间构型为________。B可形成晶体类型不同的多种单质,它们互称为________。
(2)A、C形成的某化合物的相对分子与D2的相等,写出该化合物与足量盐酸反应的离子方程式:________。
(3)A、C、F形成的化合物是一种常见的化学肥料,该物质的水溶液中离子浓度的大小顺序为________。
(4)C、D两元素可组成价态相同且能相互转变的化合物,它们是________(填化学式)。
(5)F2与FD2均可用于自来水的杀菌消毒,若它们在杀菌过程中的还原产物相同,则消毒等体积的自来水,所需F2和FD2的物质的量之比为________。
高三化学填空题简单题查看答案及解析
-
短周期主族元素A、B、C、D、E的原子序数依次增大,它们原子核外的电子层数之和为10;B元素的化合物种类繁多,数目庞大.C、D两种元素形成的单质是空气中含量最多的物质;D、E两元素可以生成两种不同的离子化合物.
(1)由A、C、D三元素所形成常见盐A4C2D3的溶液呈______性(填“酸”、“中”、“碱”),其原因用离子方程式表示为:______.
(2)B的相对分子质量最小的氢化物的燃烧热为890.3kJ•mol-1,写出其燃烧的化学方程式______.
(3)X、Y是均由C、D两元素组成的化合物,且C、D在X、Y中的价态相同,某温度下在2L的密闭容器中X、Y相互转化时的量变关系如图:
①该反应的化学方程式为______
②反应进行到25min时,改变的条件可能是______
A、缩小容器体积 B、充入0.4molNO2
C、充入0.4molN2O4 D、充入0.8molNO2
③30min后反应再次达到平衡,此时,Y转化为X的化学平衡常数为______(填数值).
④若反应温度不变,在2L的密闭容器中充入1.4molY,反应达平衡后Y的转化率是______.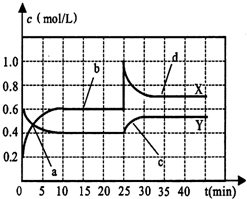
高三化学解答题中等难度题查看答案及解析
-
短周期主族元素A、B、C、D、E、F 的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)写出D与E以1∶1的原子个数比形成的化合物的电子式: _____ 。F的原子结构示意图为: 。
(2)B、D形成的化合物BD2中存在的化学键为 键(填“离子”或“共价”,下同)。A、C、F三种元素形成的化合物CA4F为 _____ 化合物。
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为: 。
(4)A、C、D、E的原子半径由大到小的顺序是 (用元素符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性 ____ 于F(填“强”或“弱”),并用化学方程式证明上述结论 。
高三化学简答题中等难度题查看答案及解析
-
短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原
子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素,D、E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(1)写出D与E以1∶1的原子个数比形成的化合物的电子式: 。F的原子结构示意图为: 。
(2)B、D形成的化合物BD2中存在的化学键为 键(填“离子”或“共价”,下同)。A、C、F三种元素形成的化合物CA4F为 化合物。
(3)化合物甲、乙由A、B、D、E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为: 。
(4)A、C、D、E的原子半径由大到小的顺序是 (用元素符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性 于F(填“强”或“弱”),并用化学方程式证明上述结论 。
高三化学填空题中等难度题查看答案及解析
-
短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层之和为13;B的化合物种类繁多,数目庞大;C、D是空气中含量最多的两种元素;D、E形成的单质在不同条件下可以生成两种不同的离子化合物;F是同周期元素中原子半径最小的.
(1)A、D以1:1形成化合物的电子式为________.A、C形成最简单化合物的空间构型为________.B可形成晶体类型不同的多种单质,它们互称为________.
(2)A、C形成的某化合物的相对分子质量与D2的相等,写出该化合物与足量盐酸反应的离子方程式:________.
(3)A、C、F形成的化合物是一种常见的化学肥料,该物质的水溶液中离子浓度的大小顺序为________.
(4)C、D两元素可组成价态相同且能相互转变的化合物,它们是________(填化学式).
(5)F2与FD2均可用于自来水的杀菌消毒,若它们在杀菌过程中的还原产物相同,则消毒等体积的自来水,所需F2和FD2的物质的量之比为________.高三化学填空题中等难度题查看答案及解析
-
短周期主族元素A、B、C、D、E的原子序数依次增大,它们的原子核外电子层数之和为10;B的化合物种类繁多,数目庞大,A、E同主族,B、C、D同周期相邻。下列说法不正确的是( )
A.常见化合物E2D2与水反应生成D的单质,同时生成的化合物溶于水能使酚酞试液变红
B.C的氢化物与C的最高价氧化物的水化物反应得到的产物中既有离子键又有共价键
C.D与A、B、C、E分别结合均能形成两种或两种以上的化合物
D.五种元素的原子半径按A~E的顺序依次增大
高三化学选择题简单题查看答案及解析
-
短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(一)
(1)化学组成为BDF2的电子式为: ,A、C、F三种元素形成的化合物CA4F为 化合物(填“离子”或“共价”)。
(2)化合物甲、乙由A,B,D,E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为: 。
(3)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是 (用元素离子符号表示)。
(4)元素B和F的非金属性强弱,B的非金属性 于F(填“强”或“弱”),并用化学方程式证明上述结论 。
(二)以CA3代替氢气研发燃料电池是当前科研的一个热点。
(1)CA3燃料电池使用的电解质溶液是2mol•L﹣1的KOH溶液,电池反应为:4 A3+3O2=2C2+6H2O.该电池负极的电极反应式为 ;每消耗3.4g CA3转移的电子数目为 。

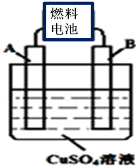
(2)用CA3燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为 ;此时向所得溶液中加入8gCuO固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为 L。
高三化学填空题极难题查看答案及解析
-
短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(一)(1)D在周期表中的位置是 ,写出实验室制备单质F的离子方程式 。
(2)化学组成为BDF2的电子式为: ,A、C、F三种元素形成的化合物CA4F为 化合物(填 “离子”或“共价”)。
(3)化合物甲、乙由A,B,D,E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为: 。
(4)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是 (用元素离子符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性 于F(填“强”或“弱”),并用化学方程式证明上述结论 。
(二)以CA3代替氢气研发氨燃料电池是当前科研的一个热点。
(1)CA3燃料电池使用的电解质溶液是2mol•L﹣1的KOH溶液,电池反应为:4 CA3+3O2=2C2+6H2O.该电池负极的电极反应式为 ;每消耗3.4g CA3转移的电子数目为 。
(2)用CA3燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为 ;此时向所得溶液中加入8gCuO固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为 L。
(3)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
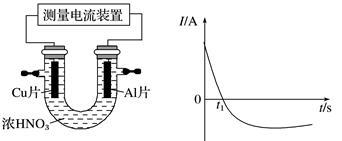
图1 图2
0~t1时,原电池的负极是Al片,此时,正极的电极反应式是 ,溶液中的H+向 极移动(填“正”或“负”),t1时,原电池中电子流动方向发生改变,其原因是 。
高三化学简答题极难题查看答案及解析
-
(12分)短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层数之和为13。已知B元素形成的化合物种类最多,D元素原子最外层电子数是次外层电子数的3倍,元素E的原子半径在同周期中最大,F元素原子最外层电子数等于其电子层数。
(1)C元素在元素周期表中的位置是_____________________,B的单质与C的最高价氧化物对应水化物的浓溶液发生反应的化学方程式是_________________
__________________________________________________________________________。
(2)由A、B、D、E四种元素形成的化合物中所含的化学键类型是_______________
_________________________________________________________。
(3)写出E2D2与A2D反应的离子方程式
_______________________________________________________________________。
(4)实验室配制100mL0.2mol·L—1由A、D、E形成化合物的溶液,需要用到的玻璃仪器除烧杯、量筒外还有_________________________;如果定容时仰视刻度线,则所配制溶液浓度______________0.2mol·L—1(埴“>”、“<”或“=”)。将F的单质溶于上述配制的溶液中所发生反应的离子方程式是_________________________________________
高三化学填空题中等难度题查看答案及解析
-
(12分)短周期主族元素A、B、C、D、E、F的原子序数依次增大,它们的原子核外电子层数之和为13。已知B元素形成的化合物种类最多,D元素原子最外层电子数是次外层电子数的3倍,元素E的原子半径在同周期中最大,F元素原子最外层电子数等于其电子层数。
(1)C元素在元素周期表中的位置是_____________________,B的单质与C的最高价氧化物对应水化物的浓溶液发生反应的化学方程式是_____________________________________
(2)由A、B、D、E四种元素形成的化合物中所含的化学键类型是_______________________
(3)写出E2D2与A2D反应的离子方程式
_______________________________________________________________________。
(4)实验室配制100mL0.2mol·L—1由A、D、E形成化合物的溶液,需要用到的玻璃仪器除烧杯、小烧杯外还有_________________________;如果定容时仰视刻度线,则所配制溶液浓度_________0.2mol·L—1(埴“>”、“<”或“=”)。将F的单质溶于上述配制的溶液中所发生反应的离子方程式是_________________________________
高三化学填空题中等难度题查看答案及解析