-
在一定温度下,将0.20molN2O4气体充入2.0L密闭容器中,间隔一定时间对该容器的气体进行分析数据如下:
时间 (s)
0
20
40
60
80
c(N2O4)mol/L
0.10
C1
0.050
C3
C4
c(NO2)mol/L
0.00
0.060
C2
0.12
0.12
(1)该反应的平衡常数表达式为________________________________,计算20s到40s二氧化氮的平均反应速率v(NO2)===____________。
(2)若在相同条件下最开始充入的是NO2气体,使得达到上述同样的平衡状态,NO2的起始浓度是___________。
(3)若在相同条件下起始时充入的NO2气体0.16mol,要计算达到平衡时NO2的转化率,请写出分析求解的思路(不必计算具体结果)____________________________。
高三化学填空题中等难度题查看答案及解析
-
NO2气体对环境有危害,应特别注意对地表水、土壤、大气和饮用水的污染。在一定温度时,将0.80 mol的NO2气体充入4 L真空的密闭容器中,每隔一段时间就对该容器内的物质进行分析,得到数据如下表所示:
时间(s)
0
20
40
60
80
n(NO2)/mol
0.80
n1
0.52
n3
n4
n(N2O4)/mol
0.00
0.10
n2
0.16
0.16
(1)在上述条件下,反应从20 s至40 s这一时间段内,NO2的平均反应速率为 mol·L-1·s-1。
(2)n3________n4(填“>”、“<”或“=”),该反应的平衡常数为 (保留小数点后一位)。
(3)达到平衡后,如向该密闭容器中再充入0.64 mol氦气,并把容器体积扩大为8 L,则平衡将______(选填“向正反应方向移动”、 “向逆反应方向移动”或“不移动”),其理由是 。
(4)若在相同情况下,最初向该容器中充入的是N2O4气体,要达到上述同样的平衡状态,起始充入N2O4的物质的量是 mol,假设在80 s时达到平衡,请在图中画出并标明该条件下此反应中N2O4和NO2的浓度随时间变化的曲线。

(5)取五等份NO2,分别加入温度不同、容积相同的恒容密闭容器中,反应相同时间后,分别测定体系中NO2的百分量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是 。

高三化学填空题简单题查看答案及解析
-
Ⅰ.在
密闭容器中放入
,在一定温度进行如下反应:
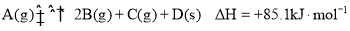
容器内气体总压强(P)与起始压强
的比值随反应时间(t)数据见下表:(提示,密闭容器中的压强比等于气体物质的量之比)
时间
0
1
2
4
8
16
20
25
1.00
1.50
1.80
2.20
2.30
2.38
2.40
2.40
回答下列问题
(1)下列能提高A的转化率的是_______
A.升高温度 B.体系中通入A气体
C.将D的浓度减小 D.通入稀有气体
,使体系压强增大到原的5倍
(2)该反应的平衡常数的表达式K_______,前2小时C的反应速率是_________
;
(3)平衡时A的转化率___________,C的体积分数__________(均保留两位有效数字)
(4)相同条件下,若该反应从逆向开始,建立与上述相同的化学平衡,则D的物质的量取值范围
______
Ⅱ.已知乙酸是一种重要的化工原料,该反应所用的原理与工业合成乙酸的原理类似;常温下,将
溶于水配成
溶液,向其中滴加等体积的
的盐酸使溶液呈中性(不考虑醋酸和盐酸的挥发),用含a和b的代数式表示醋酸的电离常数
___________
高三化学填空题中等难度题查看答案及解析
-
(15分)在100℃时,将0.40mol的二氧化氮气体充入2L抽空的密闭容器中,发生反应:
2NO2
N2O4。每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
时间/s
0
20
40
60
80
n(NO2)/mol
0.40
n1
0.26
n3
n4
n(N2O4)/mol
0.00
0.05
n2
0.08
0.08
(1)在上述条件下,从反应开始直至20 s时,二氧化氮的平均反应速率为__________
mol/(L·s)。
(2)若在相同情况下最初向该容器充入的是四氧化二氮气体,要达到上述同样的平衡状态,四氧化二氮的起始浓度是_________mol/L。假设在80s时达到平衡,请在如图中画出该条
件下N2O4和NO2的浓度随时间变化的曲线。
(3)上述(2)达到平衡后四氧化二氮的转化率为_________,混合气体的平均摩尔质量
为___________。
(4)达到平衡后,如向该密闭容器中再充入0.32molHe气,并把容器体积扩大为4L,则平衡将________(填“向左移动”、“向右移动”或“不移动”)。
高三化学填空题简单题查看答案及解析
-
在100℃时,将0.4mol的二氧化氮气体充入2L抽真空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
(1)在上述条件下,从反应开始直至20s时,二氧化氮的平均反应速率为______mol•L-1•min-1.时间(s) 20 40 60 80 n(NO2)/mol 0.4 n1 0.26 n3 n4 n(N2O4)/mol 0.05 n2 0.08 0.08
(2)n3______n4(填“>”、“<”或“=”),该反应的平衡常数的值为______;
(3)若在相同情况下最初向该容器充入的是四氧化二氮气体,要达到上述同样的平衡状态,四氧化二氮的起始浓度是______mol/L.
(4)假设从放入N2O4到平衡时需要80s,请在右图中画出并标明该条件下此反应中N2O4浓度随时间变化的曲线.
(5)在(4)中条件下达到平衡后四氧化二氮的转化率为______,混合气体的平均摩尔质量为______g.mol-1.
(6)达到平衡后,如升高温度,气体颜色会变深,则升高温度后,反应2NO2N2O4的平衡常数将______(填“增大”、“减小”或“不变”)
(7)达到平衡后,如向该密闭容器中再充入0.32molHe气,并把容器体积扩大为4L,则平衡2NO2N2O4将______.(填“向左移动”、“向右移动”或“不移动”).
(8)达到平衡后,如果缩小容器的体积,则气体的颜色变化是先变深后变浅,但比原来的颜色深,试用平衡移动原理解释其变化的原因______.
高三化学解答题中等难度题查看答案及解析
-
在1.0 L密闭容器中放入0.10molA(g),在一定温度进行如下反应应:
A(g)
B(g)+C(g) △H=+85.1kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h
0
1
2
4
8
16
20
25
30
总压强p/100kPa
4.91
5.58
6.32
7.31
8.54
9.50
9.52
9.53
9.53
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为________。
(2)由总压强P和起始压强P0计算反应物A的转化率α(A)的表达式为________。
平衡时A的转化率为________,列式并计算反应的平衡常数K ________。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总=________mol,n(A)= ________mol。
②下表为反应物A浓度与反应时间的数据,计算a=________
反应时间t/h
0
4
8
16
C(A)/(mol·L-1)
0.10
a
0.026
0.0065
分析该反应中反应反应物的浓度c(A)变化与时间间隔(△t)的规律,得出的结论是________,
由此规律推出反应在12h时反应物的浓度c(A)为________mol·L-1。
高三化学计算题中等难度题查看答案及解析
-
在1.0 L密闭容器中放入0.10 mol A(g),在一定温度进行如下反应:A(g)
B(g)+C(g) ΔH=+85.1 kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h
0
1
2
4
8
16
20
25
30
4.91
5.58
6.32
7.31
8.54
9.50
9.52
9.53
9.53
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为________。
(2)由总压强p和起始压强P0计算反应物A的转化率a(A)的表达式为________,平衡时A的转化率为________,列式并计算反应的平衡常数K________。
(3)①由总压强p和起始压强P0表示反应体系的总物质的量n(总)和反应物A的物质的量n(A),n(总)=________mol,n(A)=________mol。
②下表为反应物A浓度与反应时间的数据,计算:a=________。
反应时间t/h
0
4
8
16
c(A)/(mol·L-1)
0.10
a
0.026
0.0065
分析该反应中反应物的浓度c(A)变化与时间间隔(t)的规律,得出的结论是________,由此规律推出反应在12 h时反应物的浓度c(A)为________mol·L-1。
高三化学填空题中等难度题查看答案及解析
-
在1.0 L密闭容器中放入0.10 mol A(g),在一定温度进行如下反应:
A(g)B(g)+C(g)
ΔH=+85.1 kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h
0
1
2
4
8
16
20
25
30
总压强p/100 kPa
4.91
5.58
6.32
7.31
8.54
9.50
9.52
9.53
9.53
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为____________________。
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为______________。平衡时A的转化率为__________,列式并计算反应的平衡常数K__________________。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n(总)=________ mol,n(A)=________ mol。
②下表为反应物A浓度与反应时间的数据,计算:a=________。
反应时间t/h
0
4
8
16
c(A)/(mol·L-1)
0.10
a
0.026
0.006 5
分析该反应中反应物的浓度c(A)变化与时间间隔(Δt)的规律,得出的结论是________________________________,由此规律推出反应在12 h时反应物的浓度c(A)为__________ mol·L-1。
高三化学填空题困难题查看答案及解析
-
在1.0 L密闭容器中放入0.10 mol A(g),在一定温度进行如下反应:
A(g)
B(g)+C(g) ΔH=+85.1 kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h
0
1
2
4
8
16
20
25
30
总压强p/100 kPa
4.91
5.58
6.32
7.31
8.54
9.50
9.52
9.53
9.53
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为____________。
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为______________。平衡时A的转化率为__________,列式并计算反应的平衡常数K__________。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n(总)=____ mol,n(A)=________ mol。
②下表为反应物A浓度与反应时间的数据,计算:a=________。
反应时间t/h
0
4
8
16
c(A)/(mol·L-1)
0.10
a
0.026
0.006 5
分析该反应中反应物的浓度c(A)变化与时间间隔(Δt)的规律,得出的结论是________________________________,由此规律推出反应在12 h时反应物的浓度c(A)为__________ mol·L-1。
高三化学填空题困难题查看答案及解析
-
在1.0 L密闭容器中放入0.10 mol A(g),在一定温度进行如下反应应:
A(g)
B(g)+C(g) △H =+85.1 kJ· mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h
0
1
2
4
8
16
20
25
30
总压强p/100kPa
4.91
5.58
6.32
7.31
8.54
9.50
9.52
9.53
9.53
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为________。
(2)由总压强P和起始压强P0计算反应物A的转化率α(A)的表达式为________。
平衡时A的转化率为________,列式并计算反应的平衡常数K ________。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),
n总=________ mol,n(A)= ________mol。
②下表为反应物A浓度与反应时间的数据,计算a=________
反应时间t/h
0
4
8
16
c(A)/(mol·L-1)
0.10
a
0.026
0.0065
分析该反应中反应反应物的浓度c(A)变化与时间间隔(△t)的规律,得出的结论是________,由此规律推出反应在12h时反应物的浓度c(A)为________ mol·L-1
高三化学填空题困难题查看答案及解析