-
(1)室温时氢氧化钙的溶度积Ksp=4.7×10-6,室温时将9mL 0.02mol·L-1的氯化钙溶液与1mL pH=13的氢氧化钠溶液混合后(溶液体积可直接加和),溶液中
沉淀析出(填有或无)。
(2)2.24升(标准状态)氨气通入250mL浓度为0.1mol·L-1的硫酸溶液中,充分反应后溶液中各离子浓度由大到小的顺序为 。
(3)用下图完成相应实验。
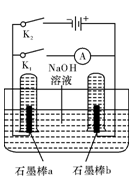
①断开K1,闭合K2接通直流电源,写出阳极的电极反应式 ;
②电解一段时间后,当两石墨棒均有气体包围时,切断K2闭合K1,发现电路中有电流通过。写出a极的电极反应式 。
-
(1)室温时氢氧化钙的溶度积KSP =4.7×10-6, 室温时将9 mL0.02 mol·L—1的氯化钙溶液与1 mL
pH=13的氢氧化钠溶液混合后(溶液体积可直接加和),溶液中________沉淀析出(填有或无).
(2)2.24升(标准状态)氨气通入250mL 浓度为0.1 mol·L—1的硫酸溶液中,充分反应后溶液中各离子浓度大小为________(按由大到小的顺序写出各离子符号)
(3) 人体血液含Ca2+。现抽取某人血样10 mL,稀释后用草酸铵[(NH4)2C2O4]溶液处理,使Ca2+完全转变为草酸钙(CaC2O4)沉淀;过滤,洗涤,将得到的沉淀用稀硫酸溶解得到草酸(H2C2O4)溶液,用5.0×10-3 mol·L-1 KMnO4溶液滴定得到的草酸至终点,共耗去2.0 mL KMnO4溶液。由上述实验数据可求得此人血液中Ca2+的物质的量浓度为________.(提示:2 KMnO4 + 5H2C2O4 + 3H2SO4 = 2MnSO4 + K2SO4 + 10CO2↑+8H2O)
(4)用下图完成相应实验.
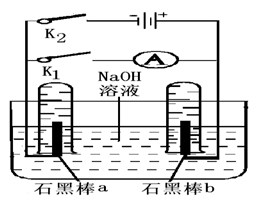
①断开K1,闭合K2接通直流电源,写出阳极 的电极反应________.
电解的总反应方程式________
②电解一段时间后,当两石墨棒均有气体包围时,切断K2闭合K1,发现电路中有电流通过. 写出a极的电极反应式________
-
向50 mL 0.018 mol·L-1 AgNO3溶液中加入50 mL 0.02 mol·L-1盐酸。已知AgCl(s)的溶度积常数Ksp= 1×10-10,混合后溶液的体积变化忽略不计。下列说法不正确的是( )
A.混合后,溶液中肯定有沉淀生成
B.沉淀生成后溶液中Ag+的浓度为10-5 mol·L-1
C.沉淀生成后溶液的pH=2
D.混合后,升高温度,溶液中Ag+的浓度增大
-
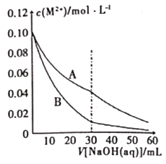
已知室温下溶度积常数:Ksp[Pb(OH)2]=2×10-15,Ksp[Fe(OH)2]=8×10-15。当溶液中金属离子浓度小于10-5mol•L-1视为沉淀完全。向20mL含0.10mol•L-1Ph2+和0.10mol•L-1Fe2+的混合溶液中滴加010amol•L-1NaOH溶液,金属阳离子浓度与滴入NaOH溶液体积的关系曲线如图所示,则下列说法正确的是( )
A. 曲线A表示 的曲线
的曲线
B. 当溶液 时,
时, 开始沉淀,
开始沉淀, 沉淀完全
沉淀完全
C. 滴入NaOH溶液体积大于30mL时,溶液中
D. 室温下,滴加NaOH溶液过程中, 比值不断增大
比值不断增大
-
已知室温下溶度积常数:Ksp[Pb(OH)2]=2×10-15,Ksp[Fe(OH)2]=8×10-15。当溶液中金属离子浓度小于10-5mol•L-1视为沉淀完全。向20mL含0.10mol•L-1Pb2+和0.10mol•L-1Fe2+的混合溶液中滴加0.10mol•L-1NaOH溶液,金属阳离子浓度与滴入NaOH溶液体积的关系曲线如图所示,则下列说法正确的是( )
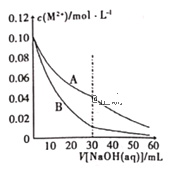
A.曲线A表示c(Pb2+)的曲线
B.当溶液pH=8时,Fe2+开始沉淀,Pb2+沉淀完全
C.滴入NaOH溶液体积大于30mL时,溶液中c(Fe2+)=4c(Pb2+)
D.室温下,滴加NaOH溶液过程中, 比值不断增大
比值不断增大
-
已知在室温时,Mg(OH)2的溶度积Ksp=5.6×10-12 (mol/L)3,要使0.2mol/lMgSO4溶液中的Mg2+沉淀较为完全[c(Mg2+)<5.6×10-6mol/L],则应向溶液中加入NaOH溶液,使溶液的pH最小为多少?
-
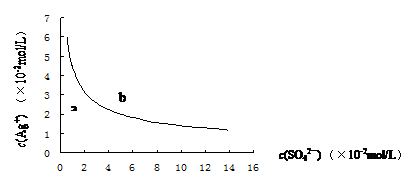
某温度T1时,Ag2SO4在水中的沉淀溶解曲线如图实线所示。下列说法正确的是( )
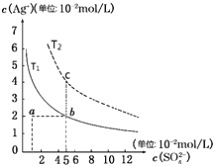
A. T1时,Ag2SO4的溶度积常数(Ksp)为1×10-3
B. T1时,0.02 mol/L的AgNO3溶液与0.2 mol/L的Na2SO4溶液等体积混合不会生成沉淀
C. b点表示T1时Ag2SO4的饱和溶液,稀释时可以使溶液由b点变到a点
D. 仅通过降温的方法,可以使T2时的饱和溶液从c点变到T1时b点
-
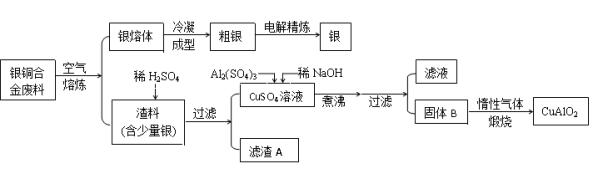
从银铜合金废料中回收银并制备铜化工产品的工艺如下:
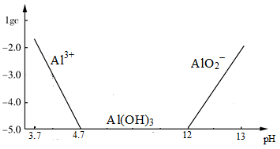
已知:①铝元素在溶液中的存在形态与溶液pH的关系如图所示。
②室温时,Cu(OH)2的溶度积Ksp=2.0×10-20,当溶液中某种离子浓度小于1.0×10-5mol/L时,认为该离子沉淀完全, 。
。
③Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃。
请回答下列问题:
(1)电解精炼银时,粗银做 极(填“阴”或“阳”),电解质选用________溶液,阴极电极反应为 。
(2)在生成固体B的过程中,需控制NaOH的加入量,使溶液的pH范围在 ,若控制不当,使NaOH过量可能会引起的反应的离子方程式为 。
(3) 煅烧过程中发生多步反应,写出最终生成CuAlO2的反应的化学方程式: 。
(4)若银铜合金中铜的质量分数为64%,理论上1.0 kg废料中的铜可完全转化为CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液 L。
-
某温度时,Ag2SO4在水中沉淀溶解平衡曲线如图所示.该温度下,下列说法正确的是( )
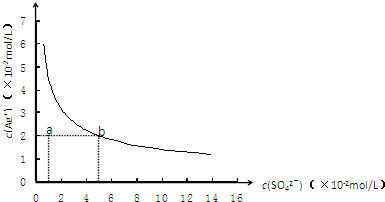
A.含有大量SO42-的溶液中肯定不存在Ag+
B.Ag2SO4的溶度积常数(Ksp)为1×10-3
C.0.02mol/L的AgNO3溶液与0.2mol/L的Na2SO4溶液等体积混合不会生成沉淀
D.a点可能为Ag2SO4的饱和溶液
-
某温度时,Ag2SO4在水中的沉淀溶解平衡曲线如图所示。该温度下,下列说法正确的是:
A.含有大量SO42-的溶液中肯定不存在Ag+
B.Ag2SO4的溶度积常数(Ksp)为1×10-4
C.0.02mol/L的AgNO3溶液与0.2mol/L的Na2SO4溶液等体积混合不会生成沉淀
D.a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点