-
一定温度下,在2.5L的恒容密闭容器中发生如下反应:CO2(g)+H2S(g) COS(g)+H2O(g)
COS(g)+H2O(g)
| 实验 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | 平衡常数 |
| CO2 | H2S | H2O | |
| I | 607 | 0.11 | 0.41 | 0.01 | |
| II | 607 | 0.22 | 0.82 | | |
| III | 620 | 0.1 | 0.4 | | 6.74×10-3 |
下列说法不正确的是( )
A. 该反应正反应为吸热反应
B. 607K时,把物质的量均为0.1mol四种反应物加入该反应器中,反应将向正反应方向进行
C. 实验Ⅱ达到平衡时容器中COS的物质的量为0.02mol
D. 实验Ⅲ中,无论是开始还是至化学平衡状态,混合气体的密度始终不变
-
一定温度下,在2.5L的恒容密闭容器中发生如下反应:CO2(g)+H2S(g) COS(g)+H2O(g)
COS(g)+H2O(g)
| 实验 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | 平衡常数 |
| CO2 | H2S | H2O | |
| I | 607 | 0.11 | 0.41 | 0.01 | |
| II | 607 | 0.22 | 0.82 | | |
| III | 620 | 0.1 | 0.4 | | 6.74×10-3 |
下列说法不正确的是( )
A. 该反应正反应为吸热反应
B. 607K时,把物质的量均为0.1mol四种反应物加入该反应器中,反应将向正反应方向进行
C. 实验Ⅱ达到平衡时容器中COS的物质的量为0.02mol
D. 实验Ⅲ中,无论是开始还是至化学平衡状态,混合气体的密度始终不变
-
一定温度下,在2.5L的恒容密闭容器中发生如下反应:CO2(g)+H2S(g) COS(g)+H2O(g)
COS(g)+H2O(g)
| 实验 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | 平衡常数 |
| CO2 | H2S | H2O | |
| I | 607 | 0.11 | 0.41 | 0.01 | |
| II | 607 | 0.22 | 0.82 | | |
| III | 620 | 0.1 | 0.4 | | 6.74×10-3 |
| | | | | |
下列说法不正确的是
A.该反应正反应为吸热反应
B.607K时,把物质的量均为0.1mol四种反应物加入该反应器中,反应将向正反应方向进行
C.实验Ⅱ达到平衡时容器中COS的物质的量为0.02mol
D.实验Ⅲ中,无论是开始还是至化学平衡状态,混合气体的密度始终不变
-
在一定温度下将1mol CO和9mol水蒸气放在密闭的容器中发生下列反应:
CO(g)+H2O(g)  CO2(g)+H2(g)达到平衡后,已知该反应平衡常数为K=1.0,达到新的平衡后,CO2和H2的物质的量之和为( )
CO2(g)+H2(g)达到平衡后,已知该反应平衡常数为K=1.0,达到新的平衡后,CO2和H2的物质的量之和为( )
A.1.2mol B .1.5mol C. 1.8mol D . 2.5mol
-
在一定温度下将3 mol CO2和2 mol H2混合于2 L的密闭容器中,发生如下反应:CO2(g)+H2(g)  CO(g)+H2O(g)。
CO(g)+H2O(g)。
(1)已知在700 ℃时,该反应的平衡常数K1=0.5,则该温度下反应CO(g)+H2O(g)  CO2(g)+H2(g) 的平衡常数K2=________。
CO2(g)+H2(g) 的平衡常数K2=________。
(2)已知在1 000 ℃时,该反应的平衡常数K3为1.0,则该反应为__ ______反应(填“吸热”或“放热”)。
(3)能判断该反应达到化学平衡状态的依据是_________。(填编号)
A.容器中压强不变
B.c(CO2)=c(CO)
C.生成a mol CO2的同时消耗a mol H2
D.混合气体的平均相对分子质量不变
(4)在1 000 ℃下,某时刻CO2的物质的量为2.0 mol,则此时v正_______v逆(填“>”、“=”或“<”),该温度下反应达到平衡时,CO2的转化率为_________。
-
在一固定体积的密闭容器中,充入2 mol CO2和1 mol H2发生如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数与温度(T)的关系如下表:
CO(g)+H2O(g),其化学平衡常数与温度(T)的关系如下表:
| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_________________。
(2)若反应在830 ℃下达到平衡,则CO2气体的转化率为________。
(3)若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO的浓度增大,则容器内气体温度________(填“升高”、“降低”或“不能确定”)。
(4)能判断该反应是否达到化学平衡状态的依据是____________。
A 容器内压强不变 B 混合气体中c(CO)不变
C v正(H2)=v逆(H2O) D c(CO2)=c(CO)
E c(CO2 )·c(H2)=c(CO)·c(H2O)
(5)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx,可用CxHy(烃)催化还原NOx消除氮氧化物的污染。
已知:CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ·mol-1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H2
CH4(g)+2NO2(g) = N2(g)+CO2(g)+2H2O(g) △H3=-867 kJ·mol-1
△H2=_____________。
-
在一定温度下将3mol CO2和2mol H2混合于2L的密闭容器中,发生如下反应:CO2(g)+H2(g)⇌CO(g)+H2O(g)
(1)该反应的化学平衡常数表达式K=_____.
(2)已知在700℃时,该反应的平衡常数K1=0.6,则该温度下反应CO(g)+H2O(g)⇌CO2(g)+H2(g)的平衡常数K2=_____,反应 CO2(g)+
CO2(g)+ H2(g)⇌
H2(g)⇌ CO(g)+
CO(g)+ H2O(g)的平衡常数K3=_____.
H2O(g)的平衡常数K3=_____.
(3)已知在1 000℃时,该反应的平衡常数K4为1.0,则该反应为_____反应(填“吸热”或“放热”).
(4)能判断该反应达到化学平衡状态的依据是_____.
A.容器中压强不变
B.c(CO2)=c(CO)
C.生成a mol CO2的同时消耗a mol H2
D.混合气体的平均相对分子质量不变
(5)在1 000℃下,某时刻CO2的物质的量为2.0mol,则此时v(正)_____v(逆)(填“>”、“=”或“<”).
-
5000C下发生如下反应H2(g)+CO2(g) H2O(g)+CO(g)△H<0,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。(已知此温度下该反应的平衡常数K=
H2O(g)+CO(g)△H<0,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。(已知此温度下该反应的平衡常数K= )
)
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
(1)、平衡时,甲中CO2转化率为
在甲、乙、丙三个恒容密闭容器中CO2转化率大小比较________
(2).丙中达平衡需要20S,则 反应速率V(CO2)=________
(3).甲中的反应速率-时间图像如图,在图中画出丙的反应速率-时间图像
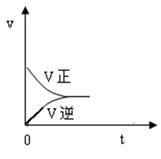
(4)升高温度,平衡常数K________ (填 “大于”“小于”“等于”)
(填 “大于”“小于”“等于”)
-
在一定温度下将3 mol CO2和2 mol H2混合于2 L的密闭容器中,发生如下反应:CO2(g)+H2(g)  CO(g)+H2O(g)
CO(g)+H2O(g)
(1)该反应的化学平衡常数表达式K=________。
(2)已知在700 ℃时,该反应的平衡常数K1=0.6,则该温度下反应CO(g)+H2O(g)  CO2(g)+H2(g)的平衡常数K2=________,反应1/2CO2(g)+1/2H2(g)
CO2(g)+H2(g)的平衡常数K2=________,反应1/2CO2(g)+1/2H2(g)  1/2CO(g)+1/2H2O(g)的平衡常数K3=________。
1/2CO(g)+1/2H2O(g)的平衡常数K3=________。
(3)已知在1 000 ℃时,该反应的平衡常数K4为1.0,则该反应为________反应(填“吸热”或“放热”)。
(4)能判断该反应达到化学平衡状态的依据是________。(填编号)
A.容器中压强不变
B.c(CO2)=c(CO)
C.生成a mol CO2的同时消耗a mol H2
D.混合气体的平均相对分子质量不变
(5)在1 000 ℃下,某时刻CO2的物质的量为2.0 mol,则此时v正________v逆(填“>”、“=”或“<”)。该温度下反应达到平衡时,CO2的转化率为________。
-
在一定温度下,将3 mol CO2和2 mol H2混合于2 L的密闭容器中,发生如下反应:
CO2(g)+H2(g) CO(g)+H2O(g)。
CO(g)+H2O(g)。
(1)该 反应的化学平
反应的化学平 衡常数表达式K=________。
衡常数表达式K=________。
(2)已知在700 ℃时,该反应的平衡常数K1=0.5,则该温度下反应CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数K2=________
CO2(g)+H2(g)的平衡常数K2=________
(3)已知在100 0 ℃时,该反应的平衡常数K3=1.0,则该反应为_________反应(填“吸热”或“放热”)。
0 ℃时,该反应的平衡常数K3=1.0,则该反应为_________反应(填“吸热”或“放热”)。
(4)在1 000 ℃下,从开始到20s时反应达到平衡状态,则CO浓度为____________mol/L,CO2的转化率为____________。此温度下,若某时刻CO2的物质的量为2 mol,则此时v正______________v逆(填“>”、“=”或“<”)。
CO(g) +H2O(g) △H。其平衡常数(K)和温度(T)的关系如下表:
CO(g) +H2O(g) 的化学反应速率(v)与时间(t)的关系如图所示,在图中t2 时只改变一个条件,则改变的条件是_________。
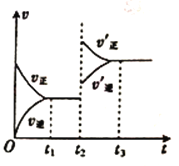
2CO(g) △H1
CO(g) +H2(g) △H2
CO(g) +H2O(g) △H=_______(用含△H1、△H2 的代数式表示)。
