2SO2(g)+O2(g)=2SO3(g) ΔH=-198kJ/mol,在V2O5存在时,该反应的机理为:V2O5+SO22VO2+SO3(快) 4VO2+O2
2V2O5(慢)
下列说法正确的是
A. 反应速率主要取决于V2O5的质量 B. VO2是该反应的催化剂
C. 逆反应的活化能大于198kJ/mol D. 增大SO2的浓度可显著提高反应速率
高二化学单选题中等难度题
2SO2(g)+O2(g)=2SO3(g) ΔH=-198kJ/mol,在V2O5存在时,该反应的机理为:V2O5+SO22VO2+SO3(快) 4VO2+O2
2V2O5(慢)
下列说法正确的是
A. 反应速率主要取决于V2O5的质量 B. VO2是该反应的催化剂
C. 逆反应的活化能大于198kJ/mol D. 增大SO2的浓度可显著提高反应速率
高二化学单选题中等难度题
2SO2(g)+O2(g)=2SO3(g) ΔH=-198kJ/mol,在V2O5存在时,该反应的机理为:V2O5+SO22VO2+SO3(快) 4VO2+O2
2V2O5(慢)
下列说法正确的是
A. 反应速率主要取决于V2O5的质量 B. VO2是该反应的催化剂
C. 逆反应的活化能大于198kJ/mol D. 增大SO2的浓度可显著提高反应速率
高二化学单选题中等难度题查看答案及解析
在一个恒温恒压的密闭容器中,有V2O5存在时发生反应:2SO2(g)+O2(g)2SO3(g)ΔH=-196.6KJ/mol。该反应过程为①SO2+V2O5
SO3+2VO2、②……下列有关该反应的说法不正确的是
A. 反应②是O2+4VO22V2O5
B. V2O5降低了反应的活化能
C. 增大O2浓度时该反应的ΔH不变
D. 当2v(O2)逆=v(SO3)正时加入V2O5,等式仍然成立,v(O2)逆、v(SO3)正值不变
高二化学单选题中等难度题查看答案及解析
2SO2(g)+O2(g)=2SO3(g) H= -198 kJ·mol-1反应过程的能量变化如图所示。请回答下列问题:
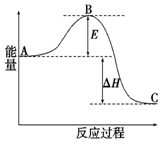
⑴E的大小对该反应的反应热有无影响?________。
该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________;
⑵图中H=________kJ·mol-1;
⑶如果反应速率v(SO2)为0.05 mol·L-1·min-1则v(O2)=________mol·L-1·min-1;
v(SO3)=________mol·L-1·min-1;
高二化学填空题简单题查看答案及解析
2SO2(g)+O2(g)2SO3(g) △H=-198kJ/mol,反应过程的能量变化如图所示。
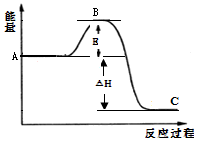
请回答下列问题:
(1)图中A表示__________,该反应加入V2O5作催化剂后E如何变化_______(填“升高”、“降低”或“不变”)。
(2)如果反应速率v(SO2)为0.05mol/(L·min),则v(O2)=_________ mol/(L·min)、v(SO3)=_____mol/(L·min)
(3)已知单质硫燃烧热的数值为296kJ/mol,则1molS(s)完全反应生成SO3(g)时放出的热量为________kJ。
(4)某人设想以如图所示装置用电化学原理生产硫酸,通入O2的一极为_______________(填写“正”或“负”)极;写出通入SO2一极的电极反应____________________。
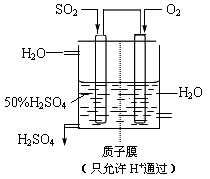
高二化学填空题困难题查看答案及解析
2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。下列说法错误的是( )
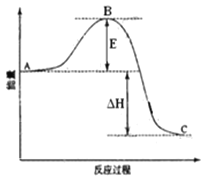
A.图中A表示反应物的总能量
B.图中E的大小对该反应的△H有影响
C.该反应通常用V2O5作催化剂,加V2O5会使图中B点降低
D.加入催化剂V2O5后,该反应的△H不变
高二化学单选题简单题查看答案及解析
反应2SO2(g)+O2(g)2SO3(g)的能量变化如图所示。已知2mol SO2(g)被氧化为2mol SO3(g)时的反应热-198kJ·mol-1
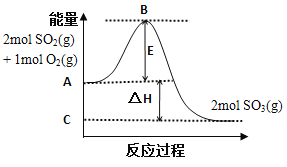
请回答下列问题:
(1)图中A点表示__________;C点表示2mol SO3(g)的总能量,E所代表的能量是__________;E的大小对该反应的反应热__________(填"有"或"无")影响
(2)图中△H=__________kJ·mol-1
高二化学填空题中等难度题查看答案及解析
工业氧化二氧化硫制三氧化硫反应的化学方程式为:2SO2(g)+ O2 (g) 2SO3(g) △H=—198kJ·mol-1假设这个反应处于平衡状态,在体积不变的条件下,下列措施会使化学平衡逆向移动的是
A.增加二氧化硫 B。升高温度 C。降低温度 D。移出三氧化硫
高二化学选择题简单题查看答案及解析
硫及其化合物对人类的生产和生活有着重要的作用.
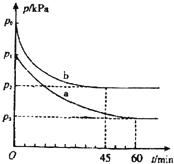
2SO2(g)+O2(g)⇌2SO3(g)△H=﹣198kJ•mol﹣1是制备硫酸的重要反应.
(1)在容积为V L的密闭容器中起始充入2mol SO2和1mol O2,反应在不同条件下进行,反应体系总压强随时间的变化如图所示.与实验a相比,实验b改变的条件是 ,判断的依据 .
(2)二氧化硫在一定条件下还可以发生如下反应:
SO2(g)+NO2(g)⇌SO3(g)+NO(g)△H=﹣42kJ•mol﹣1.
在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
| 实验编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
| N(SO2) | N(NO2) | N(NO) | ||
| 甲 | T1 | 0.80 | 0.20 | 0.18 |
| 乙 | T2 | 0.20 | 0.80 | 0.16 |
| 丙 | T3 | 0.20 | 0.30 | a |
①实验甲中,若2min时测得放出的热量是4.2kJ,则0~2min时间内,用SO2(g)表示的平均反应速率v(SO2)= ,该温度下的平衡常数 .
②实验丙中,达到平衡时,NO2的转化率为 .
③由表中数据可推知,Tl T2(填“>”“<’’或“=”),判断的理由是 .
高二化学填空题困难题查看答案及解析
硫及其化合物对人类的生产和生活有着重要的作用.
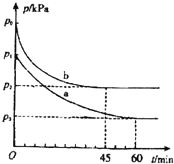
2SO2(g)+O2(g)⇌2SO3(g)△H=﹣198kJ•mol﹣1是制备硫酸的重要反应.
(1)在容积为V L的密闭容器中起始充入2mol SO2和1mol O2,反应在不同条件下进行,反应体系总压强随时间的变化如图所示.与实验a相比,实验b改变的条件是 ,判断的依据 .
(2)二氧化硫在一定条件下还可以发生如下反应:
SO2(g)+NO2(g)⇌SO3(g)+NO(g)△H=﹣42kJ•mol﹣1.
在1L恒容密闭容器中充入SO2(g)和NO2(g),所得实验数据如下:
| 实验编号 | 温度 | 起始时物质的量/mol | 平衡时物质的量/mol | |
| N(SO2) | N(NO2) | N(NO) | ||
| 甲 | T1 | 0.80 | 0.20 | 0.18 |
| 乙 | T2 | 0.20 | 0.80 | 0.16 |
| 丙 | T3 | 0.20 | 0.30 | a |
①实验甲中,若2min时测得放出的热量是4.2kJ,则0~2min时间内,用SO2(g)表示的平均反应速率v(SO2)= ,该温度下的平衡常数 .
②实验丙中,达到平衡时,NO2的转化率为 .
③由表中数据可推知,Tl T2(填“>”“<’’或“=”),判断的理由是 .
高二化学填空题困难题查看答案及解析
在硫酸工业中,通过下列反应使SO2氧化成SO3:2SO2(g)+O2(g) 2SO3(g)ΔH=-198kJ·mol-1。下表为不同温度和压强下SO2的转化率(%)
| | 1×105 | 5×105 | 1×106 | 5×106 | 1×107 |
| 450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
| 550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
(1)实际生产中,选定400~500℃作为操作温度,其原因是_______________________。
(2)实际生产中,采用的压强为常压,其原因是__________________________________。
高二化学填空题简单题查看答案及解析