-
(10分)某研究小组以CaCl2和H2为原料,试图制备 +1价Ca的化合物,结果发现产物中只有两种化合物(甲和乙)。元素组成分析表明化合物甲中钙、氯元素的质量分数分别为52.36%、46.33%;化合物乙的水溶液显酸性。请回答下列问题:
(1)生成甲的化学反应方程式为 。
(2)甲与水反应可得H2,其化学方程式是 。
(3)在加热条件下,乙的水溶液(浓)与MnO2反应的离子方程式是 ;乙的水溶液与Fe反应所得的溶液不稳定,保存该溶液的措施是 。
(4)请写出一个你认为可能得到CaCl的化学方程式(以CaCl2为原料) 。
高三化学填空题中等难度题查看答案及解析
-
某研究小组以CaCl2和H2为原料,试图制备 +1价Ca的化合物,结果发现产物中只有两种化合物(甲和乙)。元素组成分析表明化合物甲中钙、氯元素的质量分数分别为52.36%、46.33%;化合物乙的水溶液显酸性。请回答下列问题:
(1)该研究小组是否成功制得 +1价Ca的化合物? (填“是”或“否”)。甲的化学式是。
(2)甲与水反应可得H2,其化学方程式是。反应所得溶液经结晶后,可得到一种晶体,其化学式为CaCl2· xCa(OH)2· 12H2O。为确定x的值,请设计实验方案。
(3)在加热条件下,乙的水溶液(浓)与MnO2反应的离子方程式是;乙的水溶液与Fe反应所得的溶液不稳定,保存该溶液的措施是。
(4)请写出一个你认为可能得到CaCl的化学方程式(以CaCl2为原料)。
高三化学填空题中等难度题查看答案及解析
-
某研究小组以CaCl2和H2为原料,试图制备 +1价Ca的化合物,结果发现产物中只有两种化合物(甲和乙)。元素组成分析表明化合物甲中钙、氯元素的质量分数分别为52.36%、46.33%;化合物乙的水溶液显酸性。请回答下列问题:
(1)生成甲的化学反应方程式为
(2)甲与水反应可得H2,其化学方程式是 。
(3)在加热条件下,乙的水溶液(浓)与MnO2反应的离子方程式是 ;乙的水溶液与Fe反应所得的溶液不稳定,保存该溶液的措施是 。
(4)请写出一个你认为可能得到CaCl的化学方程式(以CaCl2为原料) 。
高三化学填空题困难题查看答案及解析
-
丙烯是化工合成中的重要原料,某化学小组以丙烯为初始原料制备某药物的中间体F,其合成路线如下图所示(部分产物及反应条件已经略去)。

(1)C不能使溴水褪色,核磁共振氢谱显示C中只有一类氢,则C的名称为_______,F中官能团名称为_______
(2)B能与氯化铁溶液发生显色反应,则由B生成D的反应类型为_______,反应的化学方程式为_______,已知A中有五种不同化学环境的氢,试写出由丙烯生成A的化学方程式为_______。
(3)D的同分异构体有多种,其中属于芳香族化合物、且与D同类的异构体,除D外还有_______种,其中能发生银镜反应,且核磁共振氢谱有四个峰的同分异构体的结构简式为_______。
(4)参照上述合成路线结合下面给出的信息,利用
为初始原料设计合成
的路线_______。已知:
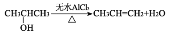 。
。高三化学推断题中等难度题查看答案及解析
-
K3Fe(A2B4)3·3H2O(M)是制备负载型活性铁催化制的主要原料,也是一些有机反应催化剂,因而具有工业生产价值。A、B均为常见短周期非金属元素。某研究小组将纯净的化合物M在一定条件下加热分解,对所得气体产物有固体产物的组成进行探究。
(1)经实验分析,所得气体产物由甲、乙和水蒸气组成。甲、乙均只含A、B两种元素,甲能使澄清的石灰水交浑浊,乙常用于工业炼铁。
①写出甲的电子式:_________。
②写出工业炼铁的化学反应方程式:_______________。
(2)该研究小组查阅资料后推知,固体产物中不存在+3价铁,盐也只有K2AB3。小组同学对固体产物进行进行如图所示定量分析。

①操作I的具体操作为____________;“固体增重”说明固体产物中定含有的物质的化学式为_____________。
②写出与酸性KMnO4溶液反府的金属阳离子的离子结构示意图:_____________;用酸性KMnO4溶液去滴定该溶液时,终点颜色变化为______________。
③已知在酸州条件下KMnO4的还原产物为Mn2+,以上实验数据分析计算固体产物中各物质及它们之间的物质的量之比为_____________。
(3)写出复盐M加热分解的化学方程式:_______________。
高三化学综合题中等难度题查看答案及解析
-
某研究性学习小组将实验室制备二氧化碳气体反应后的废物进行处理,目的是制取中性干燥剂CaCl2.得到固体后,他们对固体的成分进行了如下探究:
[提出猜想]
猜想一:只有CaCl2
猜想二:CaCl2和CaCO3
猜想三:CaCl2和HCl
通过讨论,大家认为“猜想三”不成立,理由是________.
[实验探究]
(1)写出有关反应的化学方程式:________操作 现象 结论 步骤一 
________
猜想二成立步骤二
________
(2)实验结束后,同学们根据复分解反应发生的条件,总结出得到CaCl2的不同途径,如:
①Ca(OH)2+YCla﹦CaCl2+Z↓,那么Z可能是________(填一种物质的化学式即可);
②CaXm+2YClb﹦CaCl2+H2O,则“YClb”属于________类物质.
(3)同学们又用类比的方法对CaCl2可能具有的化学性质进行了探究,总结出其能与下列物质中的________发生反应(填编号).
①HNO3 ②AgNO3 ③Na2CO3 ④Fe(OH)3 ⑤Mg ⑥BaCO3.高三化学填空题中等难度题查看答案及解析
-
化合物(NH4)xFey(SO4)m是一种重要的化工原料。某实验小组为探究该物质的组成,进行如下实验:
(1)探究铁元素化合价
A.甲同学认为铁可能只有+3价;
B.乙同学认为铁可能只有+2价;
C.丙同学认为铁的化合价________________________________。
请设计实验,证明丙同学的结论:______________________________________。
(2)三位同学通过实验证明,铁的化合价为+2价。为了进一步探究该化合物的组成,设计了如下实验:
①准确称取4.36g样品,配制成100.00mL溶液A;
②准确量取20.00mL溶液A,用0.0200 mol·L-1的酸性KMnO4标准溶液滴定其中的Fe2+离子,消耗标准溶液的体积为40.00 mL;
③测定NH4+的含量;另取20.00mL溶液A,加入足量的NaOH溶液并充分加热,用100mL0.10 mol/L的稀盐酸吸收,再用0.10mol/LNaOH标准溶液滴定吸收液,消耗NaOH的体积为60mL。
Ⅰ.写出步骤②中发生的离子方程式__________________________________。
Ⅱ.步骤③中,加入NaOH溶液发生的化学反应方程式______________________________;加入的指示剂是_____________________,判断滴定终点的现象为_____________________,若滴定管在使用前未用NaOH标准溶液润洗,测得的NH4+含量将_____________(填“偏高”、“偏低”或“不变”)。Ⅲ. (NH4)xFey(SO4)m的化学简式为_________________________。
高三化学实验题中等难度题查看答案及解析
-
某研究小组利用乳酸钙和FeCl2为原料生产乳酸亚铁([CH3CH(OH) COO]2Fe·3H2O) 和医用二水合氯化钙晶体(CaCl2·2H2O的质量分数为97.3% ~99.3%),制备流程如下:
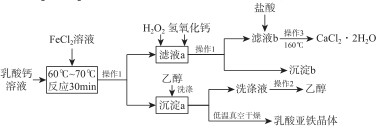
(1)实验室常用两种方案制备FeCl2,写出原子利用率为100%的反应的化学方程式 ;在FeCl2溶液中需要加
(2)制备乳酸亚铁晶体是向乳酸钙溶液中加入过量的FeCl2溶液,写出该反应的化学方程式 。
(3)操作1、操作2、操作3依次为 、 、 。
(4)向“滤液a”中先加H2O2溶,作用是 。然后再调节溶液
的 pH 约为5,目的是 。
(5)向“滤液b”加盐酸的目的是 。
(6)为测定样品中CaCl2·2H2O的含量,称取0.7600g样品并配成250mL 溶液,各取该溶液 25.00mL,分别置于三个锥形瓶中,用0.05000mol·L -1 AgNO3溶液进行三次滴定,消耗AgNO3溶液的平均体积为20.39mL。计算样品中CaCl2·2H2O的质量分数为 。
高三化学实验题中等难度题查看答案及解析
-
某科研小组采用电解锰粉(主要成分为Mn和少量含Fe、Ni、Pb、P、Si等元素的单质或其化合物)为原料制备高纯氯化锰。
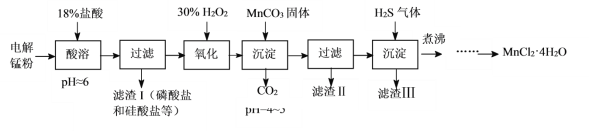
已知:①Mn是一种比Fe活泼的金属。
②H2S气体具有较强的还原性,如:H2S+H2O2=S↓+2H2O。
③相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)
Fe3+
Fe2+
Mn2+
Ni2+
Pb2+
开始沉淀的pH
1.1
5.8
8.6
6.7
8.0
沉淀完全的pH
3.2
8.8
10.1
9.2
8.8
(1)酸溶时盐酸要缓慢滴加的原因是___。
(2)加入MnCO3固体时发生反应的离子方程式为___。MnCO3固体也可用下列物质代替___。(填写编号)
A.MnO B.MnSO4 C.Mn(OH)2 D.MnCl2
(3)通入H2S气体可使Pb2+、Ni2+生成硫化物沉淀,如:H2S(aq)+Pb2+(aq)
PbS(s)+2H+(aq),该反应的平衡常数K=___[用Ka1(H2S)、Ka2(H2S)及Ksp(PbS)表示]。
(4)煮沸的目的是___。
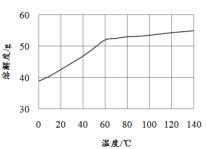
(5)已知MnCl2·4H2O在106℃时失去一分子结晶水,198℃失去全部结晶水。请补充完整由煮沸后的滤液获得高纯(>99.99%)MnCl2·4H2O晶体(MnCl2的溶解度曲线如图所示)的实验方案:将煮沸后的滤液冷却至室温,___(实验中须使用的试剂是:30%H2O2)。
高三化学工业流程中等难度题查看答案及解析
-
研究性学习小组进行了一系列化学实验后,发现高锰酸钾分解后的含锰元素的化合物都能和浓盐酸反应制得氯气,且锰化合物的还原产物都是MnCl2。他们将6.32gKMnO4粉末加热一段时间,也不知道高锰酸钾是否完全分解,收集到0.112L气体后便停止加热了,冷却后放入足量的浓盐酸再加热,又收集到气体体积是(上述气体体积都折合成标准状况)( )
A.0.448L B.2.240L
C.2.016L D.无法确定
高三化学选择题中等难度题查看答案及解析