-
某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验以下实验:将pH==2的两种酸溶液HA,HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
(1)HA为________酸,HB为________酸(填"强"或“弱")
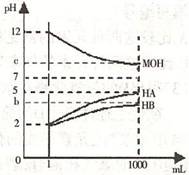 (2)若c=9,则稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为________(用酸、碱化学式表示);
(2)若c=9,则稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为________(用酸、碱化学式表示);
将稀释后的HA溶液利MOH溶液取等体积混合,则所得溶液中c(A-)与c(M+)的大小关系为________(填"大于"、"小于"或"等于")
(3)若b+c=14,则MQH为________碱(填"强"或"弱")。将稀释后的HB溶液和MOH溶液取等体积混合,所得很合溶液的pH________7(填"大于"、"小于"或"等于")
-
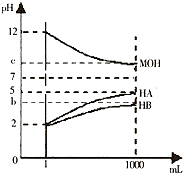
某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验以下实验:将pH═2的两种酸溶液HA,HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
(1)HA为______酸,HB为______酸;(填“强“或“弱“)
(2)若c=9,则稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为______(用酸、碱化学式表示);将稀释后的HA溶液利MOH溶液取等体积混合,则所得溶液中c(A-)与c(M+)的大小关系为______;(填“大于“、“小于“或“等于“)
(3)若b+c=14,则MQH为______碱(填“强“或“弱“).将稀释后的HB溶液和MOH溶液取等体积混合,所得很合溶液的pH______7(填“大于“、“小于“或“等于“)
-
某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验:常温下将pH=2的两种酸溶液HA、HB和pH=12的MOH碱溶液各1 mL,分别加水稀释到1 000 mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
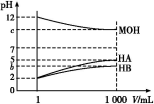
(1)HA为 酸,HB为 酸(填“强”或“弱”)。
(2)若c=9,则稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为 (用酸、碱化学式表示)。
(3)若c=9,将稀释后的HA溶液和MOH溶液取等体积混合,则所得溶液中c(A-)与c(M+)的大小关系为c(A-) (填“大于”、“小于”或“等于”)c(M+)。
(4)若b+c=14,则MOH为 碱(填“强”或“弱”)。将稀释后的HB溶液和MOH溶液取等体积混合,所得混合溶液的pH 7(填“大于”、“小于”或“等于”)。
-
为研究CH3COOH、HA和MOH的酸碱性的相对强弱,某兴趣小组设计了以下实验:室温下,将pH=2的两种酸溶液CH3COOH、HA和pH=12的碱MOH溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图1所示,根据所给数据,请回答下列问题:
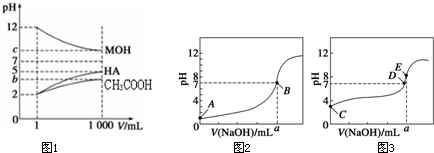
(1)HA为______酸 (填“强”或“弱”).稀释后 HA溶液中水电离出来的c(H+)______醋酸溶液中水电离出来c(H+)(填“大于”、“等于”或“小于”).
若b+c=14,则MOH为______碱(填“强”或“弱”).
(2)常温下0.10mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定变大的是______.
A.c(H+) B.c(H+)/c(CH3COOH)
C.c(H+)•c(OH-) D.c(OH-)/(H+)
(3)常温下,用0.10mol•L-1 NaOH溶液分别滴定20mL 0.10mol•L-1 HCl溶液和20mL 0.10 mol•L-1 CH3COOH溶液,得到两条滴定曲线,如图所示.如图中滴定醋酸溶液的曲线是______(填“图2”或“图3”);曲线上E点pH>8的原因是(用离子方程式表示)______.
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中离子浓度由大到小顺序为______.
-
某研究性学习小组设计了一组实验来探究元素周期律。甲同学一次性完成N、C、Si的非金属性强弱的比较;乙同学完成了氧元素的非金属性比硫强的实验。
(1)从以下所给物质中选出甲同学设计的实验所用到物质: 稀
稀 溶液
溶液 稀盐酸
稀盐酸 碳酸钙
碳酸钙 溶液
溶液
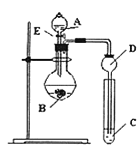
试剂A为______;试剂C为______ 填序号
填序号
(2)乙同学设计的实验所用到试剂A为______;装置C中反应的化学方程式为______。
-
下列是某同学学习氨和铵盐的性质总结,相关实验操作正确且能达到目的是( )
A.测定等浓度氨水和NaOH溶液的pH,比较氨水和NaOH碱性强弱
B.将NH3•H2O溶液缓慢滴入AlCl3溶液中,研究Al2O3的两性
C.将蘸有浓氨水和浓硫酸的玻璃棒靠近,观察产生的白烟
D.加热除去NH4Cl中的少量NaHCO3
-
实验法和比较法是研究物质性质的基本方法.以下实验设计中,不合理或不严密的是( )
A.钠和镁分别与冷水反应,判断钠和镁金属性强弱
B.测定相同温度下盐酸和醋酸溶液的pH,就可证明盐酸是强酸、醋酸是弱酸
C.铁分别与氯气和硫反应,判断氯气与硫的氧化性强弱
D.测定相同条件下Na2CO3溶液和Na2SO4溶液的pH,判断碳与硫的非金属性强弱
-
实验法和比较法是研究物质性质的基本方法.以下实验设计中,不合理或不严密的是( )
A.钠和镁分别与冷水反应,判断钠和镁金属性强弱
B.测定相同温度下盐酸和醋酸溶液的pH,就可证明盐酸是强酸、醋酸是弱酸
C.铁分别与氯气和硫反应,判断氯气与硫的氧化性强弱
D.测定相同条件下Na2CO3溶液和Na2SO4溶液的pH,判断碳与硫的非金属性强弱
-
实验法和比较法是研究物质性质的基本方法。以下实验设计中,不合理或不严密的是
A.钠和镁分别与冷水反应,判断钠和镁金属性强弱
B.测定相同温度下盐酸和醋酸溶液的pH,就可证明盐酸是强酸、醋酸是弱酸
C.铁分别与氯气和硫反应,判断氯气与硫的氧化性强弱
D.测定相同条件下Na2CO3溶液和Na2SO4溶液的pH,判断碳与硫的非金属性强弱
-
实验法和比较法是研究物质性质的基本方法.以下实验设计中,不合理或不严密的是
A.钠和镁分别与冷水反应,判断钠和镁金属性强弱
B.测定相同温度下盐酸和醋酸溶液的pH,就可证明盐酸是强酸、醋酸是弱酸
C.铁分别与氯气和硫反应,判断氯气与硫的氧化性强弱
D.测定相同条件下Na2CO3溶液和Na2SO4溶液的pH,判断碳与硫的非金属性强弱
 (2)若c=9,则稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为________(用酸、碱化学式表示);
(2)若c=9,则稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为________(用酸、碱化学式表示);


