-
(本题共12分)
铝是用途广泛的金属材料,目前工业上主要用铝土矿(主要成分含氧化铝、氧化铁)来制取铝,其常见的过程如下:

请回答下列问题:
39.沉淀B可作为化工产品出售,其用途为 ,溶液C中阴离子有 。
40.若在实验室模拟该生产,则操作IV将原料置于 中进行,确保该过程转化完全的方法是对产品(含容器)进行称量后 。
41.写出①过程中发生反应的离子方程式 ,生产过程中,NaOH、CO2、H2O和 都可循环使用。
42.有时操作Ⅱ得到的溶液为Na2CO3和NaHCO3的混合溶液。取样品溶液50.00mL加水稀释到1L,从中取出20mL。测量溶液体积的仪器事先进行洗涤的洗涤液依次为: ,对溶液体积读数的方法是读出 对应的刻度值。
43.用标准盐酸(0.2000mol/L)进行滴定:
①上述所取20.00mL溶液(酚酞做指示剂)消耗标准盐酸12.00mL。
②从1L稀释液中另取10.00mL(甲基橙做指示剂)消耗标准盐酸15.00mL。
则50.00mL原样品溶液中碳酸氢钠的浓度为 。
44.操作III进行时,为使D溶液中只有一种溶质,在每升溶液中需加入生石灰的质量为 。
-
铝是用途广泛的金属材料,目前工业上主要用铝土矿(主要成分含氧化铝、氧化铁)来制取铝,其常见的过程如下:

请回答下列问题:
(1)沉淀B的化学式为 ,溶液C中阴离子主要是 。
(2)操作Ⅰ是 (填操作名称)
(3)写出①过程中发生反应的离子方程式 。
(4)Al(OH)3沉淀必须进行洗涤才能通过操作Ⅳ获得纯净Al2O3,操作Ⅳ是 (填操作名称),简述洗涤沉淀的操作方法: 。
(5)生产过程中,除水、CaO和CO2可以循环使用外,还可循环使用的物质有 (填化学式)。
(6)电解Al2O3制取金属Al的阳极电极反应式为 。
-
(16分)铝是用途广泛的金属材料,目前工业上主要用铝土矿(主要成分含氧化铝、氧化铁)来制取铝,其常见的过程如下:

请回答下列问题:
(1)沉淀B的化学式为 ,溶液C中阴离子主要是 。
(2)操作Ⅰ是 (填操作名称)
(3)写出①过程中发生反应的离子方程式 。
(4)Al(OH)3沉淀必须进行洗涤才能通过操作Ⅳ获得纯净Al2O3,操作Ⅳ是 (填操作名称),简述洗涤沉淀的操作方法: 。
(5)生产过程中,除水、CaO和CO2可以循环使用外,还可循环使用的物质有 (填化学式)。
(6)电解Al2O3制取金属Al的阳极电极反应式为 。
-
镁铝合金在工业上有着广泛的用途,氧化铝是冶炼金属铝的主要原料。从铝土矿(主要成分是Al2O3,含有SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
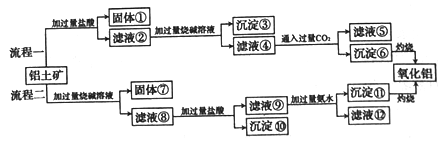
回答下列问题:
(1)Al2O3、SiO2、Fe2O3、MgO四种物质中,属于酸性氧化物的是______,属于碱性氧化物的是______。
(2)流程一中,沉淀③是_________(填化学式,下同),沉淀⑥是_________。
(3)流程二中,加入烧碱溶解SiO2的化学方程式为_________。
(4)滤液⑤中的可溶性盐是NaCl、______(填化学式),滤液⑨与过量氨水反应的离子方程式为_____。
(5)在电解氧化铝制取金属铝的反应中,氧化产物与还原产物的质量之比为______。
-
【化学——选修2:化学与技术】
元素铝是在生产、生活中应用广泛的金属元素。
(1)氧化铝是一种耐高温材料,也是工业上制取铝的原料。从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下图所示:

体A的主要成分是 (填化学式,下同),固体X的主要成分是 。
②滤液E中溶质的主要成分是 ,写出该溶质的一种用途: 。
③在滤液D中通入过量CO2时反应的离子方程式为 。
(2)工业上电解氧化铝冶炼铝时加入冰晶石(Na3AlF6)的作用是 。在电解池的工作过程中,需要不断补充阳极材料(石墨),原因是 。
(3)一种新型高效净水剂PAFC——聚合氯化铁铝[AlFe(OH)nCl6-n]m(n<5,m<10)可广泛应用于日常生活用水和工业污水的处理。下列有关PAFC的说法正确的是 (填序号)。
A.PAFC中铁元素显+2价
B.PAFC用于净水时,比用相同物质的量的氯化铝和氯化铁的pH改变小
C.PAFC可看作一定比例的氯化铁与氯化铝水解的中间产物
D.PAFC在强酸性或强碱性溶液中都能稳定存在
-
钛化合物常见价态有+2和+4。钛白粉(TiO2,两性氧化物)用途广泛。工业上由高钛渣(主要成分为Ti3O5,还含有TiO2、Fe2O3等)制取钛白粉的主要工艺过程如下:

(1)写出碱熔步骤所发生反应的化学方程式____________、____________。
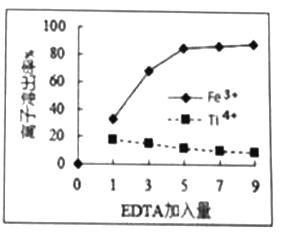
(2)实验测定EDTA加入量(EDTA和Fe3+的物质的量之比)对 Ti4+和Fe3+溶出率的影响如图所示。由图可知,EDTA的加入量为____________时除铁效率最佳,理由是____________。
(3)在实验室模拟除铁净化后的实验步骤:①向钛原料中加入稀硫酸生成偏钛酸(H2TiO3)沉淀,反应结束后过滤;②洗涤;③……;④在650℃下高温焙烧得到较纯的钛白粉固体。步骤③的实验目的是____________,需要用到的试剂有____________。
(4)测定钛白粉纯度:称取试样0.200g在CO2气氛下用金属铝将钛(IV)还原成钛(Ⅲ),还原后的溶液以NH4SCN为指示剂,用0.08mol/L的 NH4Fe(SO4)2标准液滴定,滴定终点时消耗标准液29.20mL,钛白粉的纯度为____________。(保留三位有效数字)
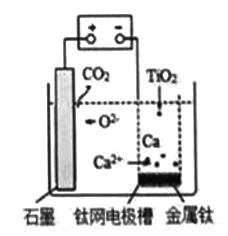
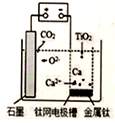
(5)最新研究发现也可以用图示装置由TiO2获得金属钛。装置中阳极的电极反应方程式为____________,在制备金属钛前后,整套装置中CaO的总量____________(填写“增大”、“减小”或者“不变”)。
-
钛化合物常见价态有+2和+4。钛白粉(TiO2,两性氧化物)用途广泛。工业上由高钛渣(主要成分为Ti3O5,还含有TiO2、Fe2O3等)制取钛白粉的主要工艺过程如下:
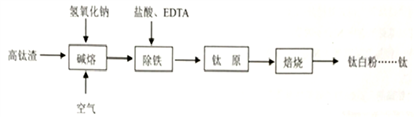
(1)写出碱熔步骤所发生反应的化学方程式____________、____________。
(2)实验测定EDTA加入量(EDTA和Fe3+的物质的量之比)对 Ti4+和Fe3+溶出率的影响如图所示。由图可知,EDTA的加入量为____________时除铁效率最佳,理由是____________。

(3)在实验室模拟除铁净化后的实验步骤:①向钛原料中加入稀硫酸生成偏钛酸(H2TiO3)沉淀,反应结束后过滤;②洗涤;③……;④在650℃下高温焙烧得到较纯的钛白粉固体。步骤③的实验目的是____________,需要用到的试剂有____________。
(4)测定钛白粉纯度:称取试样0.200g在CO2气氛下用金属铝将钛(IV)还原成钛(Ⅲ),还原后的溶液以NH4SCN为指示剂,用0.08mol/L的 NH4Fe(SO4)2标准液滴定,滴定终点时消耗标准液29.20mL,钛白粉的纯度为____________。(保留三位有效数字)
(5) 最新研究发现也可以用图示装置由TiO2获得金属钛。装置中阳极的电极反应方程式为____________,在制备金属钛前后,整套装置中CaO的总量____________(填写“增大”、“减小”或者“不变”)。
-
Na、Al、Fe是生活中常见的金属元素。
(1)工业上以铝土矿(主要成分Al2O3·3H2O)为原料生产铝,主要包括下列过程:
①将粉碎、筛选后的铝土矿溶解在氢氧化钠溶液中;
②通入过量二氧化碳使①所得溶液中析出氢氧化铝固体;③使氢氧化铝脱水生成氧化铝;④电解熔融氧化铝生成铝。
写出②所涉及离子反应方程式: ,蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与Al2O3·6H2O混合并加热,可得到无水AlCl3,用化学方程式解释: 。
(2)铁在地壳中的含量约占5%左右。铁矿石的种类很多,重要的有磁铁矿石、赤铁矿石等。红热的铁能跟水蒸气反应,则其反应的化学方程式为 。生成的黑色物质溶于酸后,加入KSCN溶液,见不到血红色产生,其原因是 、 (用离子方程式解释)。工业炼铁常用赤铁矿与Al在高温下反应制备,写出该反应的方程式: 。
(3)钠的化合物中,其中纯碱显碱性的原因是 (用离子方程式解释),向饱和的纯碱溶液中通入过量的二氧化碳所产生现象 ,该物质是 。(写化学式)
-
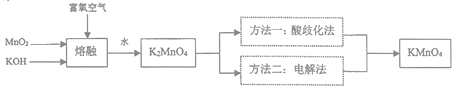
KMnO4是一种重要的氧化剂,广泛用于化学分析和化工生产以反水处理工业。工业上可由软锰矿(主要成分为MnO2)制备,目前有两种较为成熟的制法。其模拟流程如下图所示:
附表:不同温度下若干常见钾的化合物的溶解度(单位:g/(100g H2O))
| 化学式 | 20°C | 30°C | 40°C | 60°C | 80°C | 100°C |
| CH3COOK | 256 | 283 | 324 | 350 | 381 | |
| K2SO4 | 11.1 | 13 | 14.8 | 18.2 | 21.4 | 24.1 |
| KCl | 34.2 | 37.2 | 40.1 | 45.8 | 51.3 | 56.3 |
| KMnO4 | 6.34 | 9.03 | 12.6 | 22.1 | | |
| K2CO3 | 111 | 114 | 117 | 127 | 140 | 156 |
(1)“熔融”时,可用作坩锅材质的是________________(填序号)。
A.氧化铝 B.陶瓷 C.氧化镁 D.石英
(2)写出MnO2和KOH熔融物中通入富氧空气时获得K2MnO4的化学方程式______________________。
(3)“酸歧化法”是在pH<6的情况下K2MnO4即可转化为MnO2和KMnO4,过滤除去MnO2,将滤液经过蒸发浓缩、趁热过滤得到KMnO4粗晶体,再经过重结晶获得较纯净的KMnO4晶体;
①根据表中的溶解度数据以及上述操作的特点,“酸歧化法”不适宜选择的酸性物质是________。
A.稀硫酸 B.醋酸 C.稀盐酸 D.二氧化碳
②“蒸发浓缩”时,温度需控制在70℃,适宜的加热方式是________________。
③根据相关方程式,计算“酸歧化法”的理论产率为_________________。
(4)“电解法”克服了“酸歧化法”理论产率偏低的问题,同时副产品KOH可用于软锰矿的焙烧。电解法制备高锰酸钾的实验装置示意图如下(图中阳离子交换膜只允许K+离子通过)
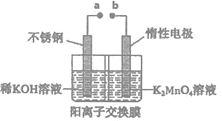
①a为______极 (填“正”或“负”),右室发生的电极反应方程式为_______________。
②若电解开始时阳极区溶液为1.0L 0.40 mol·L-1K2MnO4溶液,电解一段时间后,右室中n(K)/m(Mn)为6:5,阴极区生成KOH的质量为_________________。
-
二氧化钛是目前使用最广泛的白色颜料。工业上,以钛铁矿(主要成分为钛酸亚铁[FeTiO3],含有少量SiO2杂质)为原料制备二氧化钛的过程如下图所示。
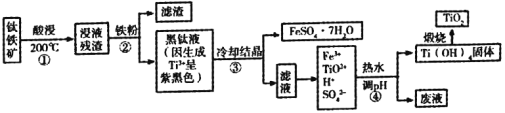
已知:①超过70℃TiO2+易水解;低于0℃ FeSO4·7H2O大量结晶。
②钛的化合价主要有+4价和+3价,其中Ti3+(紫黑色)还原性比Fe2+强
③有关氢氧化物开始沉淀的pH如下:
| 氢氧化物 | Ti(OH)4 | Ti(OH)3 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀时的pH | 0.5 | 3.0 | 1.5 | 7.6 |
根据相关信息回答下列问题;
(1)酸浸过程选用的酸是__________。
(2)步骤①中生成Fe2+和TiO2+的化学反应方程式为__________。
(3)以下相关描述正确的是__________。
A 步骤②中加入铁粉,在防止Fe2+转化成Fe3+的同时也将部分TiO2+氧化成了Ti3+
B 步骤③中的降温结晶过程可以选择冰水混合物
C ③中发生了反应Fe3++ Ti3++H2O== Fe2++ TiO2++2H+
D 废液成分中有硫酸,可以循环利用
(4)步④中生成Ti(OH)4的离子方程式为__________,选择的pH范围是__________。
(5)证明步骤④中Ti (OH)4固体已经洗涤干净的方法是__________。
(6)钛酸锂(Li4Ti5O12)是一种理想型嵌入材料,插入与脱嵌对材料结构几乎没影响。某新型钛酸锂电池总反应式为:LiXO2(s)+Li4Ti5O12(s)=Li1-aXO2+Li4+aTi5O12(s),则其负极反应式为__________。













