-
(14分)现有碳酸钠和氯化钠的固体混合物,为了测定样品中碳酸钠的含量,化学兴趣小组同学分两组进行了以下实验。
第一组
实验装置
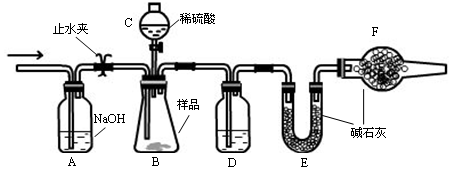
实验步骤
①连接好装置,检查气密性;
②盛装药品,其中样品a g,称量E的质量,连接好装置;
③关闭止水夹,向B中加入一定量稀硫酸;
④当B中充分反应后,打开止水夹,经过A装置,通入一定量的空气,将B、D中残余的气体全部赶入到E装置中;
⑤称量E,增重了b g 。
回答下列问题:
(1)仪器C的名称________,D中盛放的试剂是________。
(2)B中发生反应的化学方程式为________。
(3)A中反应的离子方程式为________。
(4)改变下列一个条件,导致测定样品中的碳酸钠的质量百分含量偏低的是________(选填字母)
A.实验后期不通入空气 B.将仪器C中的硫酸换成盐酸
C.撤走仪器D D.撤走仪器F
第二组
实验装置

实验步骤
①检查装置气密性
②装好试剂,其中样品b g,连接好装置,将注射器的活塞推到底,即0mL处
③加入20mL硫酸,
④待反应充分进行后,活塞不在移动,记下活塞前端对应的刻度为V mL
回答下列问题
(1) 检查该装置气密性的方法是:。
(2)对于产生气体的体积有两种观点,观点一:产生气体的体积为VmL;观点二:产生气体的体积为(V-20)mL,你认为________(填“观点一”“观点二”)正确。
(3)假如该实验在标准状况下进行,b=0.5g,V=76mL,则样品中碳酸钠的质量百分含量为________。
-
现有一份含有FeCl3和FeCl2的固体混合物,某化学兴趣小组为测定各成分的含量进行如下两个实验:
实验1 ①称取一定质量的样品,将样品溶解;
②向溶解后的溶液中加入足量的AgNO3溶液,产生沉淀;
③将沉淀过滤、洗涤、干燥得到白色固体28.7 g
实验2 ①称取与实验1中相同质量的样品,溶解;
②向溶解后的溶液中通入足量的Cl2;
③再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀;
④将沉淀过滤、洗涤后,加热灼烧到质量不再减少,得到固体Fe2O36.40g
根据实验回答下列问题:
(1)实验室保存FeCl2溶液时通常会向其中加入少量的铁粉,其作用是(用方程式表示)_______________________________________________________
(2)用方程式表示实验2的步骤②中通入足量Cl2的反应:_________________________
(3)若实验需要250mL 0.1mol/LNaOH溶液
①配制NaOH溶液除烧杯、胶头滴管外还需的玻璃仪器是_____________、___________
②下列有关配制过程中说法错误的是_________(填序号)。
A. 用托盘天平称量质量为1.0g的NaOH
B.将称量的NaOH放入烧杯中溶解,立即转移至容量瓶
C.洗涤溶解NaOH的烧杯,并将洗涤液转移至容量瓶中
D.摇匀后发现液面低于刻度线,重新定容
E.定容时,仰视容量瓶刻度线会使配制的NaOH溶液浓度偏低
(4)该小组取来的样品中含有FeCl2的质量为_________g
-
现有一份含有FeCl3和FeCl2的固体混合物,某化学兴趣小组为测定各成分的含量进行如下两个实验:
实验1:
①称取一定质量的样品,将样品溶解;②向溶解后的溶液中加入足量的AgNO3溶液,产生沉淀;③将沉淀过滤、洗涤、干燥得到白色固体28.7g.
实验2:
①称取与实验1中相同质量的样品,溶解;②向溶解后的溶液中通入足量的Cl2;③再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀;④将沉淀过滤、洗涤后,加热灼烧到质量不再减少,得到固体Fe2O36.40g.
根据实验回答下列问题:
(1)溶解过程中所用到的玻璃仪器有______.
(2)实验室保存FeCl2溶液时通常会向其中加入少量的铁粉,其作用是(用方程式表示)______.
(3)用化学方程式表示实验2的步骤②中通入足量Cl2的反应:______.
(4)用容量瓶配制实验所用的NaOH溶液,下列情况会使所配制溶液浓度偏高的是(填序号)______.
A.未冷却溶液直接转移
B.没用少量蒸馏水洗涤烧杯和玻璃棒2-3次并转入容量瓶
C.加蒸馏水时,不慎超过了刻度线
D.砝码上沾有杂质
E.容量瓶使用前内壁沾有水珠
(5)检验实验2的步骤④中沉淀洗涤干净的方法是______.
(6)该小组取来的样品中含有FeCl2的质量为______g.
-
实验室要配制80 mlL1.00 mol/LNaCl溶液,实验室现有含有少量碳酸钠的氯化钠固体。
Ⅰ.为了除去氯化钠样品中的杂质,某兴趣小组最初设计了如下方案进行实验:
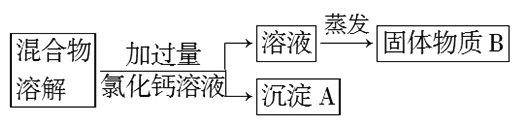
(1)沉淀A的化学式是_______________。
(2)在实验过程中,又发现了新的问题:此方案很容易引入新的杂质。则固体物质B的成分为_________________(用化学式表示)。
(3)继续探究后又提出了新的方案:将混合物溶解,先滴加足量_________________(填试剂名称),再蒸发结晶,有关反应的离子方程式为_______________________________。
Ⅱ.配制溶液:
(1)配制过程中需要使用的玻璃仪器除烧杯和玻璃棒外还有_________________。
(2)从所配溶液中取出10mL,与足量AgNO3溶液反应,经过滤、洗涤、干燥后得到白色沉淀1.50 g。则所配溶液的浓度________1.00 mol/L (填“>”、“<”或“=”),造成此误差的操作可能是_______________。
A.使用容量瓶前未干燥
B.用托盘天平称量氯化钠固体时将砝码错放在左盘
C.定容时俯视容量瓶的刻度线
D.定容后经震荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
-
化学兴趣小组的同学为测定某Na2CO3和NaCl的固体混合物样品中Na2CO3的质量分数进行了以下实验,请你参与并完成对有关问题的解答。
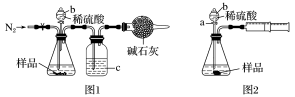
(1)甲同学用图1所示装置测定CO2的质量。实验时稀硫酸是与样品中的__________(填“Na2CO3”或“NaCl”)发生反应,仪器b的名称是__________,洗气瓶c中盛装的是 。实验开始前,打开止水夹,先通入N2,,通入N2的作用是_______________________________;一会后,连接上干燥管,打开b的活塞,滴下稀硫酸,充分反应后,再通入N2的目的 。
(2)乙同学用图2所示装置,取一定质量的样品(m g)和足量稀硫酸反应进行实验,完成样品中Na2CO3质量分数的测定。
①实验前,检查该装置气密性的方法是先打开活塞a,由b注入水至其下端玻璃管中形成一段水柱,再将针筒活塞向内推压,若b下端玻璃管中的__________,则装置气密性良好。
②在实验完成时,能直接测得的数据是CO2的______(填“体积”或“质量”)。
(3)丙同学用下图所示方法和步骤进行实验:
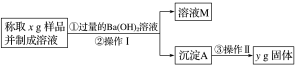
①操作Ⅰ涉及的实验名称有__________、洗涤;操作Ⅱ涉及的实验名称有干燥、__________。
②丙同学测得的样品中Na2CO3质量分数的计算式为__________。
-
化学兴趣小组的同学为测定某Na2CO3和NaCl的固体混合物样品中Na2CO3的质量分数进行了以下实验。请你参与并完成对有关问题的解答:
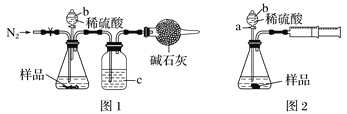
(1)甲同学用图1所示装置测定CO2的质量。实验时稀硫酸是与样品中的__________(填“Na2CO3”或“NaCl”)发生反应,仪器b的名称是__________,洗气瓶c中盛装的是浓硫酸,此浓硫酸的作用是____________________。
(2)乙同学用图2所示装置,取一定质量的样品m g和足量稀硫酸反应进行实验,完成样品中Na2CO3质量分数的测定。
①实验前,检查该装置气密性的方法是先打开活塞a,由b注入水至其下端玻璃管中形成一段水柱,再将针筒活塞向内推压,若b下端玻璃管中的___________________,则装置气密性良好。
②在实验完成时,能直接测得的数据是CO2的______(填“体积”或“质量”)。
(3)丙同学用下图所示方法和步骤进行实验:
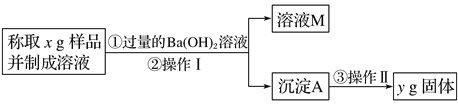
①操作Ⅰ涉及的实验名称有:__________、洗涤;操作Ⅱ涉及的实验名称有干燥、__________。
②丙同学测得样品中Na2CO3的质量分数为__________。
-
现有13.4g固体氯化钙样品(含杂质氯化钠),为了测定样品中氯化钙的含量,将此固体全部溶于96.6g水中,再向所得混合溶液中滴加一定质量分数的碳酸钠溶液,生成沉淀的质量与所加碳酸钠溶液质量的关系如图所示,回答下列问题:

(1)当氯化钙与碳酸钠恰好完全反应时,消耗碳酸钠溶液的质量是 g。
(2)氯化钙与碳酸钠恰好完全反应后所得溶液中,溶质的质量分数是多少?
-
化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中碳酸钠的质量分数。
[方案一]称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为____________。
(2)实验中,需加热至恒重的目的是_____________。
[方案二]称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量氢氧化钡溶液,过滤、洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-=BaCO3↓+H2O)。
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为__________。
(2)实验中判断沉淀是否完全的方法是__________。
[方案三]按如下图所示装置进行实验:
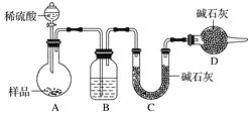
(1)D装置的作用是________,分液漏斗中_____(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重8.80g,则样品中碳酸钠的质量分数为________。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是_________。
-
化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中碳酸钠的质量分数。
[方案一]称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。则坩埚中发生反应的化学方程式为____________________________。
[方案二]称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量氢氧化钡溶液,过滤、洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3-=BaCO3↓+H2O)。
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为__________。
(2)实验中判断沉淀是否完全的方法是_________________________。
[方案三]按如下图所示装置进行实验:
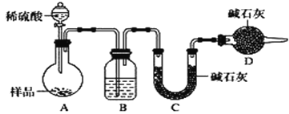
(1)D装置的作用是______________________,分液漏斗中__________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90g样品,实验后测得C装置增重8.80 g,则样品中碳酸钠的质量分数为_____。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是____________。
-
(12分)为了除去氯化钠样品中的杂质碳酸钠,某兴趣小组最初设计了如下所示方案进行实验。
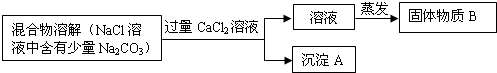
(1)沉淀A的化学式是________。
(2)加入过量氯化钙溶液后,分离除去沉淀A的实验操作过程是___________。
(3)他们在实验过程中,又发现了新的问题:此方案很容易引入新的杂质。固体物质B的成分为________(用化学式表示)。
(4)他们继续探究后又提出了新的方案:将混合物溶解,滴加盐酸至不再产生气泡为止,然后加热煮沸。有关反应的化学方程式为______________。










