-
(14分)下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
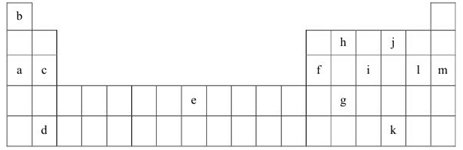
(1)上述元素的单质可能是电的良导体的是_______(填字母代号)。
(2)下表是一些气态原子的第一、二、三、四级电离能(kJ·mol-1):
| 锂 | X | Y |
| 第一电离能 | 519 | 502 | 580 |
| 第二电离能 | 7296 | 4570 | 1820 |
| 第三电离能 | 11799 | 6920 | 2750 |
| 第四电离能 | | 9550 | 11600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量: 。
②表中的Y可能为以上13种元素中的 (填元素符号)元素,用元素符号表示X和j按原子个数1:1形成化合物的电子式 。
(3)根据构造原理,用电子排布式表示e的核外电子排布式 。
(4)以上13种元素中, (填元素符号)元素原子失去核外第一个电子需要的能量最多。
(5)a、e、f三种元素的最高价氧化物的水化物显碱性,其碱性最强的为_______(用化学符号作答)。f的氧化物具有两性,写出其与NaOH溶液反应的离子方程式___________。
-
(14分)下图是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素:

(1)上述元素的单质中熔点最高的可能是________(填字母)。
(2)在一定条件下,a与e可形成一种简单化合物,其晶体类型为________,空间结构是________;a与d形成的简单化合物中含________键。(填“极性”或“非极性”)
(3)现有另一种元素X,其原子获得一个电子时所释放出的能量比表中所列元素中都要大,则X是________元素,属于周期表中________族元素。
(4)NH3·H2O的电离方程式为 试判断NH3溶于水后,形成的NH3·H2O的合理结构是________(填序号)。
试判断NH3溶于水后,形成的NH3·H2O的合理结构是________(填序号)。
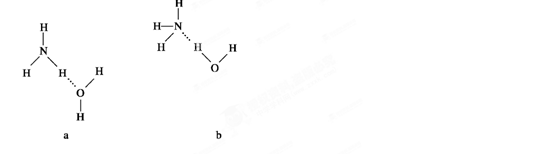
-
(8分)下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素
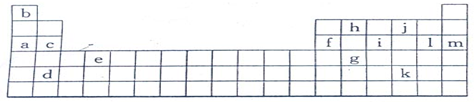
(1)下列________(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响。
原子核失去核外不同电子所需的能量(KJ·mol-1)
| 锂 | X | Y |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7 296 | 4 570 | 1 820 |
| 失去第三个电子 | 11 799 | 6 920 | 2 750 |
| 失去第四个电子 | | 9 550 | 11 600 |
①通过上述信息和表中的数据分析,为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量________。
②表中X可能为13种元素中的________(填写字母)元素。用元素符号表示X和j形成的化合物的化学式________ ________。
③Y是周期表中________族的元素。
④以上13种元素中,________(填写字母)元素原子失去核外第一个电子需要的能量最多。
(3)g元素原子基态时的核外电子排布式为______。
-
下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。

(1)下列________(填写编号)组元素的单质可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。
核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
A.原子核对核外电子的吸引力
B.形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1):
| 锂 | X | Y |
| 失去第一个电子 | 519 | 502 | 580 |
| 失去第二个电子 | 7 296 | 4 570 | 1 820 |
| 失去第三个电子 | 11 799 | 6 920 | 2 750 |
| 失去第四个电子 | —— | 9 550 | 11 600 |
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量__________________________________。
②表中X可能为以上13种元素中的(填写字母)____________元素。用元素符号表示X和j形成化合物的化学式________________。
③Y是元素周期表中第________族元素。
④以上13种元素中,________(填写字母)元素原子失去核外第一个电子需
要的能量最多。
-
下表是元素周期表中短周期的一部分,表中所列字母分别代表一种元素。

(1)上述元素的单质中熔点最高的可能是________(填字母);dh4比gh4稳定,其原因是______。
(2)f和a所形成的物质的沸点在f相应主族元素的同类型化合物中比较高,其原因是_____________。
(3)f的氢化物属于___晶体,a与d形成的化合物da4的立体构型是___,它的晶体属于_____晶体。
(4) c、i、j可组成离子化合物cxij6,其晶胞结构如下图所示,阳离子c+(用○表示)位于正方体棱的中点和正方体内部;阴离子ij6x-(用●表示)位于该正方体的顶点和面心。该化合物的化学式是________。

-
(4分)下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
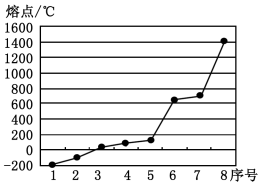
(1)元素b的基态原子电子排布式为 。
(2)第三周期8种元素按单质熔点高低的排列顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号)。
(3)元素a、c分别与元素d形成的化合物中,熔点较高的是(填化学式)。
-
下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
试回答下列问题
(1)元素“O”在周期表中的位置是 。
(2)画出“c”的简化电子排布式 。
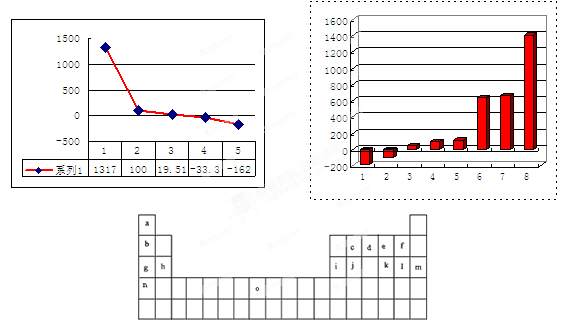
(3)第三周期8种元素按单质熔点大小顺序的柱形图如上,其中序列“1”代表 (填字母)。
(4)b、c、d、e、f的氢化物的沸点(℃)直角坐标图如右,序列“5”氢化物的化学式为: ;序列“1”氢化物的电子式为: 。
-
(8分)下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
(1)下列__________(填写编号)组元素的单质具有良好导电性。
①a、c、h ②b、g、k ③c、h、i ④d、e、f
(2)下表是一些气态原子失去核外不同电子所需的能量,(即电离能,单位为kJ·mol-1):
| 电离能 | 锂 | X | Y |
| I2 | 519 | 502 | 580 |
| I2 | 7 296 | 4 570 | 1 820 |
| I3 | 11 799 | 6 920 | 2 750 |
| I4 | | 9 550 | 11 600 |
①为什么锂原子的第二电离能远远大于第一电离能
________________________________________________________________________。
②表中X可能为以上13种元素中的__________(填写字母)元素。用元素符号表示X和j形成化合物的化学式_________________________________________________________。
③Y是周期表中__________族元素。
④以上13种元素中,_______(填写字母)元素原子失去核外第一个电子需要的能量最多。
-
下表是元素周期表的一部分。表中所列字母分别代表某一化学元素。

(1)下列 (填写编号)组元素的单质具有良好导电性。
①a、c、m ②b、g、k ③c、h、1 ④d、e、f
(2)电离能主要取决于原子核对核外电子的吸引力和形成稳定结构的倾向。下表是一些气态原子各级电离能的数据(kJ·mol-1):
| | 锂 | X | Y |
| 失去一个电子 | 519 | 502 | 580 |
| 失去二个电子 | 7296 | 4570 | 1820 |
| 失去三个电子 | 11799 | 6920 | 2750 |
| 失去四个电子 | | 9550 | 11600 |
①为什么锂原子的第二电离能远远大于第一电离能 。
②用电子式表示X和j以原子个数1比1形成的一种化合物 。
③Y在周期表中是 族元素。
④e元素的电子排布式为
-
元素周期表是学习化学的重要工具,下图所示为元素周期表中的一部分。表中所列的字母分别代表对应的化学元素。

(1)上述元素中,金属性最强的元素在周期表中的位置是______;最高价氧化物对应水化物中酸性最强的元素是___________(填元素符号)。常温下,其单质在浓硝酸中会发生钝化的元素是_______(填元素符号)。
(2)元素g的简单离子结构示意图为______,元素d的一种氢化物中两种原子的个数比为1: 1,则该物质的电子式为___________
(3)k元素可能的性质或应用有________。
A.是一种活泼的金属元素 B.其简单氢化物的热稳定性比h强
C.其单质可作为半导体材料 D.最高正化合价为+4
(4)下列说法正确的是________
A.简单离子半径的大小顺序: r(d>r(e>r(g)>r(f)
B.元素非金属性由强到弱的顺序:e>d>c
C.f、g、i最高价氧化物对应的水化物两两之间能发生反应
D.化合物f2d2中,阴、阳离子个数之比为1:1
(5)元素a与元素g有相似的化学性质。请写出元素a的氢氧化物与NaOH溶液反应的化学方程式:_____________。


 试判断NH3溶于水后,形成的NH3·H2O的合理结构是________(填序号)。
试判断NH3溶于水后,形成的NH3·H2O的合理结构是________(填序号)。








