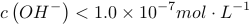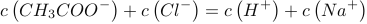-
(1)常温下某溶液中由水电离出的离子浓度符合c(H+)·c(OH﹣)=1×10﹣20的溶液,其pH为 ,此时水的电离受到 .
(2)在某温度下,H2O的离子积常数为1×10﹣13 mol2·L﹣2,则该温度下:100mL 0.1mol·L﹣1H2SO4溶液与100mL 0.4mol·L﹣1的KOH溶液混合后,pH= .
(3)已知一溶液有4种离子:X+、Y﹣、H+、OH﹣,下列分析结果肯定错误的是 .
A.c(Y﹣)>c(X+)>c(H+)>c(OH﹣)
B.c(X+)>c(Y﹣)>c(OH﹣)>c(H+)
C.c(H+)>c(Y﹣)>c(X+)>c(OH﹣)
D.c(OH﹣)>c(X+)>c(H+)>c(Y﹣)
(4)在25℃下,将a mol·L﹣1的氨水与0.01mol·L﹣1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl﹣).则溶液显 (填“酸”“碱”或“中”)性;用含a的代数式表示NH3·H2O的电离常数Kb= .
(5)水溶液中的行为是中学化学的重要内容.已知下列物质的电离常数值:HClO:Ka=3×10﹣8;H2CO3:Ka1=4.3×10﹣7;Ka2=5.6×10﹣11;84消毒液中通入少量的CO2,该反应的化学方程式为  .
.
-
(1)常温下某溶液中由水电离出的离子浓度符合c(H+)•c(OH-)=1×10-20的溶液,其pH为_________,此时水的电离受到________________。
(2)在某温度下,H2O的离子积常数为1×10-13 ,则该温度下:
①0.01mol•L-1NaOH溶液的pH=_________;
②100mL 0.1mol•L-1H2SO4溶液与100mL 0.4mol•L-1的KOH溶液混合后,pH=_________。
(3)已知一溶液有4种离子:X+、Y-、H+、OH-,下列分析结果肯定错误的是_________。
A.c(Y-)>c(X+)>c(H+)>c(OH-) B.c(X+)>c(Y-)>c(OH-)>c(H+)
C.c(H+)>c(Y-)>c(X+)>c(OH-) D.c(OH-)>c(X+)>c(H+)>c(Y-)
(4)在25℃下,将a mol•L-1的氨水与0.01mol•L-1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl-)。则溶液显_________(填“酸”“碱”或“中”)性;用含a的代数式表示NH3•H2O的电离常数Kb=___________。
-
(1)常温下某溶液中由水电离出的离子浓度符合c(H+)•c(OH﹣)=1×10﹣20的溶液,其pH为____________,此时水的电离受到______________.
(2)已知:2NO2(g) N2O4(g)△H=﹣57.20kJ•mol﹣1.一定温度下,在密闭容器中反应2NO2(g)
N2O4(g)△H=﹣57.20kJ•mol﹣1.一定温度下,在密闭容器中反应2NO2(g) N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2转化率的是_____________(填字母)
N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2转化率的是_____________(填字母)
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(3)在某温度下,H2O的离子积常数为1×10﹣13 mol2•L﹣2,则该温度下:
①0.01mol•L﹣1NaOH溶液的pH=__________;
②100mL 0.1mol•L﹣1H2SO4溶液与100mL 0.4mol•L﹣1的KOH溶液混合后,pH=_______.
(4)已知一溶液有4种离子:X+、Y﹣、H+、OH﹣,下列分析结果肯定错误的是_____.
A.c(Y﹣)>c(X+)>c(H+)>c(OH﹣)
B.c(X+)>c(Y﹣)>c(OH﹣)>c(H+)
C.c(H+)>c(Y﹣)>c(X+)>c(OH﹣)
D.c(OH﹣)>c(X+)>c(H+)>c(Y﹣)
(5)在25℃下,将a mol•L﹣1的氨水与0.01mol•L﹣1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl﹣).则溶液显_____(填“酸”“碱”或“中”)性;用含a的代数式表示NH3•H2O的电离常数Kb=______________.
-
下列溶液一定呈酸性的是
A.pH=6.8的溶液
B.常温下,由水电离的OH﹣离子浓度为1×10﹣13mol/L
C.加入酚酞,不显红色的溶液
D.常温下,溶液中的H+离子浓度为5×10﹣7mol/L
-
常温下,向20 mL 0.1 mol•L-1氨水溶液中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。
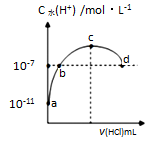
则下列说法正确的是
A. 常温下,0.1mol•L-1氨水的电离常数K约为1×10-5mol•L-1
B. a、b之间的点一定满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C. c点溶液中c(NH4+)=c(Cl-)
D. d点代表两溶液恰好完全反应
-
常温下,向20mL0.1mol/L氨水溶液中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。则下列说法正确的是( )
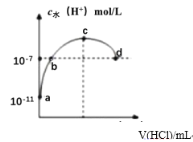
A.常温下,NH3·H2O的电离常数约为1×10-5
B.a、b之间的点一定满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C.c点溶液中:c(NH4+)= c(Cl-)
D.d点代表两溶液恰好完全反应
-
常温下,向纯水中加入NaOH使溶液的pH为11,则由NaOH电离出的OH 离子浓度和水电离出的OH离子浓度之比为 ( )
A.1:1 B.108 :1 C.5×109 :1 D.1010 :1
-
关于常温下0.1 醋酸钠溶液,下列说法正确的是( )
醋酸钠溶液,下列说法正确的是( )
A. 该溶液中水电离出来的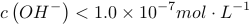
B. 溶液中离子浓度关系:
C. 该溶液的
D. 加入等浓度等体积的盐酸,溶液中: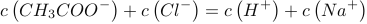
-
下列溶液一定呈酸性的是
A.pH=6.8的溶液
B.由水电离的OH-离子浓度为1×10-13 mol/L
C.加入酚酞,不显红色的溶液
D.常温下,溶液中的H+离子浓度为5×10-7 mol/L
-
常温下,下列说法不正确的是( )
A. 等体积、等物质的量浓度的NaCl(aq) 离子总数大于NaClO(aq)中离子总数
B. pH=3的硫酸溶液中水的电离程度等于pH=11的氨水溶液中水的电离程度
C. 0.1 mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A)
D. 向NH4HSO4溶液中滴加NaOH溶液至中性,所得混合液:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+)
.