-
已知强酸与强碱在稀溶液里发生中和反应生成1molH2O时放出57.3kJ热量。用500mL 0.6mol/L 的稀硫酸跟足量的NaOH溶液反应,放出的热量是( )
A. 68.76kJ B. 57.3kJ C. 34.38kJ D. 17.19kJ
高一化学单选题简单题查看答案及解析
-
已知强酸与强碱的中和热为57.3kJ/mol,用500mL 0.6mol/L的稀硫酸跟足量的NaOH溶液反应,放出的热量为
A.68.76 kJ B.57.3 kJ C.34.38 kJ D.17.19 kJ
高一化学选择题中等难度题查看答案及解析
-
强酸和强碱的稀溶液中和时,中和热为57.3kJ,试计算:
(1)浓度为0.1mol·L-1的NaOH溶液200mL,与足量酸反应时,能放出多少千焦的热量_____?
(2)浓度为5%的H2SO4溶液980g,与足量的NaOH溶液反应,能放出多少热量______ ?
(3)用浓度为0.2mol·L-1的HNO3 100mL,与足量的NaOH溶液反应,能放出多少热量_____ ?
高一化学计算题中等难度题查看答案及解析
-
(8分)用一定浓度的稀盐酸与稀NaOH溶液在左下图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。已知强酸与强碱的中和热为57.3KJ/mol,水的比热容为4.2J/(g·℃),有关热量与比热容的计算公式:Q=m×c×△t(Q为热量,m为物质的质量,c为比热容,△t物质温度的变化值)
回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是:
(2)将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。
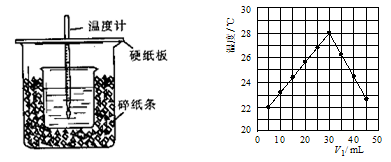
下列叙述正确的是________
A.做该实验时环境温度为22 ℃ B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约是1.00 mol/L D.该实验表明有水生成的反应都是放热反应
(3)V1=30mL时HCl和NaOH恰好反应,根据题中所给数据算出的温度变化值约为
(保留整数,计算时可将稀溶液的密度及比热容看成与水近似相同,且溶液混合时体积变化忽略不计);而根据上图的温度变化可读出温度变化值约7 ℃;两者相比所测结果偏低,造成如此现象的原因有:
________
高一化学实验题简单题查看答案及解析
-
已知:稀溶液中,强酸与强碱反应中和热的数值为57.3kJ/mol。
(1)用0.1molBa(OH)2配成的稀溶液跟足量的稀硝酸反应,放出______kJ的热量
(2)1L0.1mol/LNaOH溶液分别与①醋酸溶液②浓硫酸③稀硝酸恰好反应时,放出的热量分别为Q1 、Q2 、Q3(单位:kJ),则它们由大到小的顺序是_________________________
高一化学填空题中等难度题查看答案及解析
-
25 ℃,101 k Pa时,强酸与强碱的稀溶液发生中和反应生成1mol水时所放出的热量约为57.3 kJ/mol;辛烷的燃烧热为5518 kJ/mol。下列热化学方程式书写正确的是( )
A.CH3COOH(aq)+NaOH(aq)= CH3COONa(aq)+H2O(l)
H=
57.3kJ/mol
B.KOH(aq)+
H
SO4(aq)=
K2SO4(aq)+H2O(l)
H=
57.3kJ/mol
C.C8H18(l)+
O2 (g)=8CO2 (g)+ 9H2O(g)
H=
5518 kJ/mol
D.2C8H18(g)+25O2 (g)=16CO2 (g)+18H2O(1)
H=
5518 kJ/mol
高一化学选择题困难题查看答案及解析
-
强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(1) ⊿H=-57.3kJ/mol。向1L0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应⊿H1、⊿H2、⊿H3的关系正确的是
A.⊿H1>⊿H2>⊿H3 B.⊿H1<⊿H3<⊿H2
C.⊿H1<⊿H2<⊿H3 D.⊿H1>⊿H3>⊿H2
高一化学选择题中等难度题查看答案及解析
-
已知中和热的数值是57.3KJ/mol。下列反应物混合时,产生的热量等于57.3KJ的是( )
A.1mol/L盐酸和1mol/LNaOH溶液等体积混合
B.500mL1.0mol/L的硫酸和500mL1.0mol/L的Ba(OH)2溶液
C.500mL2.0mol/L的盐酸和500mL2.0mol/L的NaOH溶液
D.500mL2.0mol/L CH3COOH溶液和500mL2.0mol/L NaOH溶液
高一化学选择题简单题查看答案及解析
-
强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(1) ΔH=-57.3kJ/mol。向1L 0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应ΔH1、ΔH2、ΔH3的关系正确的是( )
A. ΔH1>ΔH2>ΔH3 B. ΔH1<ΔH3<ΔH2
C. ΔH1<ΔH2<ΔH3 D. ΔH1>ΔH3>ΔH2
高一化学单选题中等难度题查看答案及解析
-
强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJ•mol﹣1.分别向1L 0.5mol•L﹣1的NaOH溶液中加入①浓硫酸、②稀醋酸、③稀硝酸,恰好完全反应的焓变分别为△H1、△H2、△H3,下列关系正确的是( )
A. △H2>△H3>△H1 B. △H1<△H2<△H3
C. △H1>△H2=△H3 D. △H1=△H2<△H3
高一化学单选题简单题查看答案及解析