-
H2O2是重要的化学试剂,在实验室和生产实际中应用广泛.
Ⅰ.应用其不稳定性,H2O2可被用来研究催化剂对反应速率的影响.
(1)写出H2O2在MnO2催化下分解的化学方程式______ 2H2O+O2↑高三化学解答题中等难度题查看答案及解析
-
请根据化学动力学和化学热力学回答下列问题:
I.过氧化氢是一种重要的物质,在科学研究和生产生活中应用广泛。
利用H2O2和KbrO3反应研究瞬时反应速率(r),原理为在酸催化下,KBrO3+3H2O2==KBr+3O2↑+3H2O。资料显示:r=k·cx(KbrO3)·cy(H2O2),其中k为速率常数。在290K测得实验数据如下:
实验编号
1
2
3
4
c(H2O2)/(mol/L)
1
1
2
4
c(KBrO3)/(mol/L)
0.003
0.006
0.001
0.001
R/(mol·L-1·s-1)
3×10-4
6×10-4
8×10-4
6.4×10-3
(1)写出H2O2的电子式____________,H2O2 可以看成二元弱酸,写出其第二步电离方程式_________________________________。
(2)根据表格数据信息,写出瞬时反应速率表达式r=______(k保留两位有效数字); 如果减缓反应速率,可采用的方法有___________ (任写两点)。
II.(3)25℃,101kpa时乙烯酮CH2CO(g)和甲烷CH4的燃烧热分别为:ΔH=-1025.1kJ/mol,ΔH=-890. 3kJ/mol,则反应2CH4(g)+2O2(g)
CH2CO(g) +3H2O(l)的热化学方程式为__________________。
(4)在恒容容器中。通入2molCH4和2molO2,不能判断反应2CH4(g)+2O2(g)
CH2CO(g) +3H2O(l)处于平衡状态的是_________。
体系内压强保持不变 B.体系内气体密度保持不变
C.单位时间每消耗2molCH4,同时生成lmolO2
D.通入等物质的量的反应物,一段时间后反应物浓度之比不变
(5)对于反应2CH4(g)+2O2(g)
CH2CO(g) +3H2O(g),在恒容条件下,向容器内加入0.1molCH4和0.1molO2,反应达到平衡时CH2CO的物质的量百分含量为15%,则平衡时n(CH4)=______ mol。
高三化学综合题中等难度题查看答案及解析
-
(17分)H2O2是一种绿色氧化还原试剂,在化学研究中应用广泛。
(1)某小组拟在同浓度Fe3+的催化下,探究H2O2浓度对H2O2分解反应速率的影响。限选试剂与仪器:30% H2O2、0.1mol∙L-1Fe2(SO4)3、蒸馏水、锥形瓶、双孔塞、水槽、胶管、玻璃导管、量筒、秒表、恒温水浴槽、注射器
①写出本实验H2O2分解反应方程式并标明电子转移的方向和数目:____________
②设计实验方案:在不同H2O2浓度下,测定 ____________________________________(要求所测得的数据能直接体现反应速率大小)。
③设计实验装置,完成下图的装置示意图。
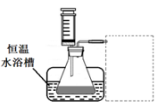
④参照下表格式,拟定实验表格,完整体现实验方案(列出所选试剂体积、需记录的待测物理量和所拟定的数据;数据用字母表示)。

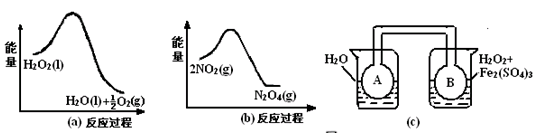
(2)利用图21(a)和21(b)中的信息,按图21(c)装置(连能的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的_________(填“深”或“浅”),其原因是______________________________________________________。
高三化学填空题中等难度题查看答案及解析
-
H2O2是一种绿色的氧化剂和漂白剂,不稳定,易分解。研究不同条件对同体积同浓度的H2O2分解速率的影响,得到如下结果:
序号
I
II
III
pH
7
7
11
温度/℃
95
95
50
反应时间/h
1
3
1
催化剂(等量)
无
Cu2+
Fe3+
无
Cu2+
Fe3+
无
Cu2+
Fe3+
分解百分率(%)
0.8
57.4
2.6
1.1
96.3
4.8
35.5
100
95.0
由此不能得出的结论是:
A. Cu2+与Fe3+对H2O2分解都有催化作用,但Cu2+催化效果更好
B. 由I与II可知其它条件相同时,浓度越大,H2O2分解越快
C. 由I与III可知其它条件相同时,pH越大,H2O2分解越快
D. 由I与III可知其它条件相同时,温度越高,H2O2分解越快
高三化学选择题中等难度题查看答案及解析
-
(10分)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
实验编号
反应物
催化剂
①
10 mL 2% H2O2溶液
无
②
10 mL 5% H2O2溶液
无
③
10 mL 5% H2O2溶液
1 mL 0.1 mol·L-1 FeCl3溶液
④
10 mL 5% H2O2溶液+少量HCl溶液
1 mL 0.1 mol·L-1 FeCl3溶液
⑤
10 mL 5% H2O2溶液+少量NaOH溶液
1 mL 0.1 mol·L-1 FeCl3溶液
(1)催化剂能加快化学反应速率的原因是__________________________________。
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为___________________。
(3)实验①和②的目的是___________________________________________________。
实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是______________________________。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。

分析上图能够得出的实验结论是_____________________________________________。
高三化学实验题简单题查看答案及解析
-
(10分)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
实验编号
反应物
催化剂
①
10 mL 2% H2O2溶液
无
②
10 mL 5% H2O2溶液
无
③
10 mL 5% H2O2溶液
1 mL 0.1 mol·L-1 FeCl3溶液
④
10 mL 5% H2O2溶液+少量HCl溶液
1 mL 0.1 mol·L-1 FeCl3溶液
⑤
10 mL 5% H2O2溶液+少量NaOH溶液
1 mL 0.1 mol·L-1 FeCl3溶液
(1)催化剂能加快化学反应速率的原因是__________________________________。
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为___________________。
(3)实验①和②的目的是___________________________________________________。
实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是______________________________。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。
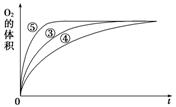
分析上图能够得出的实验结论是_____________________________________________。
高三化学实验题简单题查看答案及解析
-
(10分)某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
实验编号
反应物
催化剂
①
10 mL 2% H2O2溶液
无
②
10 mL 5% H2O2溶液
无
③
10 mL 5% H2O2溶液
1 mL 0.1 mol·L-1 FeCl3溶液
④
10 mL 5% H2O2溶液+少量HCl溶液
1 mL 0.1 mol·L-1 FeCl3溶液
⑤
10 mL 5% H2O2溶液+少量NaOH溶液
1 mL 0.1 mol·L-1 FeCl3溶液
(1)催化剂能加快化学反应速率的原因是__________________________________。
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为___________________。
(3)实验①和②的目的是___________________________________________________。
实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是______________________________。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图。
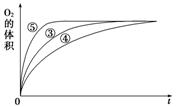
分析上图能够得出的实验结论是_____________________________________________。
高三化学实验题简单题查看答案及解析
-
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
(1)催化剂能加快化学反应速率的原因是______.实验编号 反应物 催化剂 ① 10mL2% H2O2溶液 无 ② 10mL5% H2O2溶液 无 ③ 10mL5% H2O2溶液 1mL0.1mol•L-1FeCl3溶液 ④ 10mL5% H2O2溶液+少量HCl溶液 1mL0.1mol•L-1FeCl3溶液 ⑤ 10mL5% H2O2溶液+少量NaOH溶液 1mL0.1mol•L-1FeCl3溶液
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为______.
(3)实验①和②的目的是______.实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是______.
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.
分析上图能够得出的实验结论是______.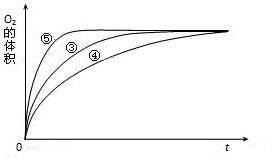
高三化学解答题中等难度题查看答案及解析
-
硫氰酸盐在化学工业中有广泛的应用。如 NH4SCN在有机工业用于聚合反应的催化剂,医药工业用于抗生素生产,印染工业用作印染扩散剂等。Co(SCN)2可以用来检验可卡因的存在。
(1)Co(SCN)2可以用CoSO4(aq)+Ba(SCN)2(aq)=BaSO4(s)+Co(SCN)2(aq)来制备,也可用CoCO3与足量HSCN制备,请写出反应方程式___________。
(2)某小组为探究NH4SCN的热分解产物,按如图所示装置进行实验。
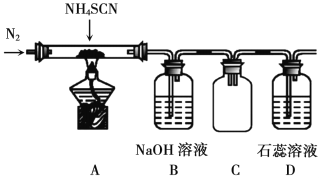
①图中盛放NH4SCN的装置名称是___________,通入氮气的作用___________。
②反应一段时间后,发现B瓶中溶液分层,分液后取下层液体,该液体可将硫磺溶解,由此判断分解产物中有___________。
③D瓶中的石蕊溶液由紫色变为蓝色,证明分解产物生成___________,C瓶装置的作用___________。
④反应完成后,取一定量B瓶上层溶液用盐酸酸化,然后滴入到0.1mol·L-1CuSO4溶液中,立即析出黑色沉淀,请写该反应的离子方程式___________。
⑤某同学指出该实验装置存在不足,请写出改进措施___________。
高三化学实验题困难题查看答案及解析
-
H2O2广泛应用于医疗卫生、化学合成等领域。
(1)H2O2的电子式是___________。
(2)趣味实验“大象牙膏”的实验原理是H2O2溶液在KI催化作用下分解,反应的机理可表示为:i.H2O2(l)+I-(aq)==== H2O(l)+IO-(aq) △H1 = +a kJ/moL(a > 0)
ii.H2O2(l)+________________________________。
① 2H2O2(l)=2H2O(l)+O2(g) △H=-196kJ/mol,补全反应ii_______________(用热化学方程式表示)。
② 某小组在研究影响H2O2分解速率的因素时得到图1的数据关系,由此得出的结论是________。
③ 已知:i的反应速率小于ii的反应速率,在图2画出H2O2溶液中加入KI后,“反应过程—能量”示意图。_________

(3)为分析不同试剂是否对H2O2分解有催化作用,该小组向四支盛有10mL5% H2O2的试管中滴加不同溶液,实验记录如下:
试管
Ⅰ
Ⅱ
Ⅲ
Ⅳ
滴加试剂
2滴1mol/L
NaCl
2滴1mol/L
CuSO4
2滴1mol/L CuSO4
和2滴1mol/L
NaCl
2滴1mol/L CuSO4
和4滴1mol/L
NaCl
产生气泡情况
无气泡产生
均产生气泡,且气泡速率从Ⅱ到Ⅳ依次加快
实验Ⅰ的目的是______________,由实验(3)可得出的结论是________________。
高三化学综合题中等难度题查看答案及解析