-
(15分)某废金属屑中主要成分为Cu、Fe、Al,还含有少量的铜锈[Cu2(OH)2CO3]、少量的铁锈和少量的氧化铝,用上述废金属屑制取胆矾(CuSO4·5H2O)、无水AlCl3和铁红的过程如下图所示:

请回答:
(1)在废金属屑粉末中加入试剂A,生成气体1的反应的离子方程式是________________________。
(2)溶液2中含有的金属阳离子是__________;气体2的成分是__________。
(3)溶液2转化为固体3的反应的离子方程式是__________________________________。
(4)利用固体2制取CuSO4溶液有多种方法。
①在固体2中加入浓H2SO4并加热,使固体2全部溶解得CuSO4溶液,反应的化学方程式是___________________________________________________________________。
②在固体2中加入稀H2SO4后,通入O2并加热,使固体2全部溶解得CuSO4溶液,反应的离子方程式是_________________________________________________________。
(5)溶液1转化为溶液4过程中,不在溶液1中直接加入试剂C,理由是_________________________
(6)直接加热AlCl3·6H2O不能得到无水AlCl3。SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体。AlCl3·6H2O与SOCl2混合加热制取无水AlCl3,反应的化学方程式是_________________。
-
某废金属屑中主要成分为Cu、Fe、Al,还含有少量的铜锈[Cu2(OH)2CO3]、少量的铁锈和少量的氧化铝,用上述废金属屑制取胆矾(CuSO4·5H2O)、无水AlCl3和铁红的过程如下图所示:

已知: ①Al3+、Al(OH)3、AlO2-有如下转化关系:

②碳酸不能溶解Al(OH)3。
请回答:
(1)在废金属屑粉末中加入试剂A,生成气体1的反应的离子方程式是。
(2)溶液2中含有的金属阳离子是________;气体2的成分是________。
(3)溶液2转化为固体3的反应的离子方程式是________。
(4)固体2制取CuSO4溶液有多种方法。
①在固体2中加入浓H2SO4,并加热,使固体2全部溶解得CuSO4溶液,反应的化学方程式是________。
②在固体2中加入稀H2SO4后,通入O2并加热,使固体2全部溶解得CuSO4溶液,反应的离子方程式是________。
(5)溶液1转化为溶液4过程中,不在溶液1中直接加入试剂C,理由是________。
(6)直接加热AlCl3·6H2O不能得到无水AlCl3。SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体。AlCl3·6H2O与SOCl2混合加热制取无水AlCl3,反应的化学方程式是________。
-
某废金属屑中主要成分为Cu、Fe、Al,还含有少量的铜锈[Cu2(OH)2CO3]、少量的铁锈和少量的氧化铝,用上述废金属屑制取胆矾(CuSO4·5H2O)、无水AlCl3和铁红的过程如下图所示:

请回答:
(1)在废金属屑粉末中加入试剂A,生成气体1的反应的离子方程式是_________________。
(2)溶液2中含有的金属阳离子是__________;气体2的成分是______________。
(3)溶液2转化为固体3的反应的离子方程式是____________________________。
(4)利用固体2制取CuSO4溶液有多种方法。
①在固体2中加入浓H2SO4并加热,使固体2全部溶解得CuSO4溶液,反应的化学方程式是___________。
②在固体2中加入稀H2SO4后,通入O2并加热,使固体2全部溶解得CuSO4溶液,反应的离子方程式是_____________________________。
(5)溶液1转化为溶液4过程中,不在溶液1中直接加入试剂C,理由是__________________
(6)直接加热AlCl3·6H2O不能得到无水AlCl3。SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体。AlCl3·6H2O与SOCl2混合加热制取无水AlCl3,反应的化学方程式是______________。
-
某废金属屑中主要成分为Cu、Fe、Al,还含有少量的铜锈[Cu2(OH)2CO3]、少量的铁锈和少量的氧化铝,用上述废金属屑制取胆矾(CuSO4·5H2O)、无水AlCl3和铁红的过程如下图所示:

(1)在废金属屑粉末中加入试剂A,生成气体1的反应的离子方程式是________。
(2)溶液2中含有的金属阳离子是________;气体2的成分是________。
(3)溶液2转化为固体3的反应的离子方程式是________。
(4)固体2制取CuSO4溶液有多种。 如在固体2中加入稀H2SO4后,通入O2并加热,使固体2全部溶解得CuSO4溶液,反应的离子方程式是________。
(5)溶液1转化为溶液4的一系列过程,不能简化为“向溶液1中+加试剂C→溶液4”,理由是________。
(6)直接加热AlCl3·6H2O不能得到无水AlCl3。SOCl2为无色液体,极易与水反应生成HCl和一种具有漂白性的气体。AlCl3·6H2O与SOCl2混合加热制取无水AlCl3,反应的化学方程式是________。
-
(9分)氮的氧化物对人体危害极大,实验时应防止其对空气的污染。
实验一:某同学利用下列装置实现铜与浓硝酸、稀硝酸的反应。
Ⅰ、取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
Ⅱ、将洗涤后的铜丝做成匝数较多的螺旋状。
Ⅲ、按如图所示装置连接仪器、检查气密性、装入化学试剂。

(1)请完成过程Ⅰ发生反应的离子方程式:
Cu2(OH)2CO3+4H+= 。
(2)过程Ⅲ的后续操作如下:
① 为使浓硝酸与铜丝接触,操作是打开止水夹a和b, ,当红棕色气体较多时,轻抽注射器使反应停止,关闭a,取下注射器。生成红棕色气体的化学方程式是 。
② 控制b与分液漏斗活塞,玻璃管充满稀硝酸时,关闭b打开a,可见有无色气体产生。稀硝酸充满玻璃管的目的是 。
实验二:NO2与水反应的实验研究。
(3)将3支充满红棕色气体的小试管分倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示(忽略温度对气体体积的影响):

① 根据上表得出的结论是温度越 (填“高”或“低“),进入试管中的溶液越多。
② 查阅材料:a.NO2与水反应的实际过程为:2NO2+ H2O=HNO3+ HNO2,3 HNO2= HNO3+2NO↑+H2O;b. HNO2不稳定。则产生上述现象的原因是 。
-
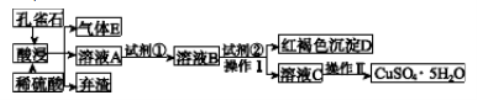
某工厂以孔雀石[主要成分为Cu2(OH)2CO3,含有少量Fe、Si的氧化物]为主要原料制备蓝矾晶体(CuSO4·5H2O),其生产流程如图所示:
已知该条件下,通过调节溶液的酸碱性而使Fe3+、Fe2+、Cu2+生成沉淀的pH分别如下表所示:
| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe(OH)3 | 2.2 | 3.2 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 4.7 | 6.4 |
回答下列问题:
(1)弃渣的主要成分是____________,Ⅱ中有“洗涤”的操作,其目的是_____________________。
(2)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。试剂①是一种氧化剂,则试剂①最好为下列中的____________,反应的离子方程式为______________________。
a.Na2O2 b.H2O2 c.Cl2 d.KSCN
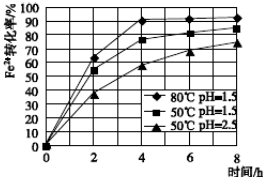
(3)根据下图有关数据,你认为工业上氧化操作时应采取措施将反应温度及溶液pH分别控制在_________________,氧化时间为________h左右。
(4)操作Ⅰ中溶液的pH应控制在________范围内。
(5)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液进行滴定,则KMnO4溶液应置于________(填“酸”或“碱”)式滴定管中。若滴定20.00mLA的溶液,用去0.0240mol·L-1KMnO4溶液16.00mL时恰好达到滴定终点,则A溶液中Fe2+的浓度为________________。
-
某同学利用下面装置实现铜与浓、稀硝酸反应,过程如下:
Ⅰ、取一段铜丝,用稀硫酸除去铜锈〔主要成分是 Cu2(OH)2CO3〕
Ⅱ、将洗涤后的铜丝做成匝数很多的螺旋状
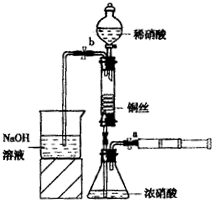
Ⅲ、按如图所示连接仪器、检查气密性、装入化学试剂
(1)过程Ⅰ发生反应的离子方程式是______;
(2)过程Ⅱ将铜丝做成螺旋状的目的是______;
(3)过程Ⅲ的后续操作如下:
①为使浓硝酸与铜丝接触,操作是______.当红棕色气体较多时,轻抽注射器使反应停止,关闭a,取下注射器.生成红棕色气体的化学方程式是______.
②控制b和分液漏斗活塞,玻璃管充满稀硝酸时,关闭b打开a,可见无色气体.稀硝酸充满玻璃管的实验目的是______.
(4)将3支盛满红棕色气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致.结果如下表所示:
| 实验编号 | 水温/C | 液面上升高度 |
| 1 | 25 | 超过试管 |
| 2 | 50 | 不足试管 |
| 3 | | 液面上升超过实验1 |
①根据上表得出的结论是______;
②查阅资料:
a.NO2与水反应的实际过程为:2NO2+H2O═HNO2+HNO3 3HNO2═HNO3+2NO↑+H2O
b.HNO2不稳定.
产生上述现象的原因是______.
-
某同学利用下面装置实现铜与浓、稀硝酸反应,过程如下:
Ⅰ、取一段铜丝,用稀硫酸除去铜锈〔主要成分是 Cu2(OH)2CO3〕
Ⅱ、将洗涤后的铜丝做成匝数很多的螺旋状
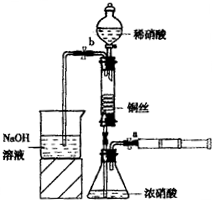
Ⅲ、按如图所示连接仪器、检查气密性、装入化学试剂
(1)过程Ⅰ发生反应的离子方程式是______;
(2)过程Ⅱ将铜丝做成螺旋状的目的是______;
(3)过程Ⅲ的后续操作如下:
①为使浓硝酸与铜丝接触,操作是______.当红棕色气体较多时,轻抽注射器使反应停止,关闭a,取下注射器.生成红棕色气体的化学方程式是______.
②控制b和分液漏斗活塞,玻璃管充满稀硝酸时,关闭b打开a,可见无色气体.稀硝酸充满玻璃管的实验目的是______.
(4)将3支盛满红棕色气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致.结果如下表所示:
| 实验编号 | 水温/C | 液面上升高度 |
| 1 | 25 | 超过试管 |
| 2 | 50 | 不足试管 |
| 3 | | 液面上升超过实验1 |
①根据上表得出的结论是______;
②查阅资料:
a.NO2与水反应的实际过程为:2NO2+H2O═HNO2+HNO3 3HNO2═HNO3+2NO↑+H2O
b.HNO2不稳定.
产生上述现象的原因是______.
-
(16分)某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如下:
I. 取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状。
III.按如图所示装置连接仪器、检查气密性、装入化学试剂。
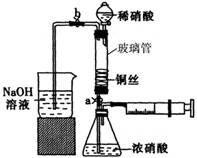
(1)过程I发生反应的离子方程式是________。
(2)写出过程III中检查气密性的方法________。
⑶过程III的后续操作如下:
①打开止水夹a和b,轻推注射器,使浓硝酸与铜丝接触,观察到的现象是________,一段时间后使反应停止的操作是________,关闭a,取下注射器。
②打开b和分液漏斗活塞,当玻璃管充满稀硝酸后,关闭b和分液漏斗活塞,打开a,观察到有气泡产生。稀硝酸充满玻璃管的实验目是________,该反应的离子方程式是________。
(4)另取3支盛满NO2气体的小试管分别倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示(忽略温度对气体体积的影响):
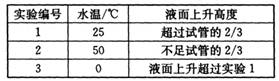
①根据上表得出的结论是温度越________(填“高”或“低”),进入试管中的溶液越多。
②查阅资料:
a.NO2与水反应的实际过程为:2NO2+H2O=HNO3+HNO2 3HNO2 =HNO3+2NO+H2O;
b.HNO2不稳定。
则产生上述现象的原因是。
-
(10分)某同学用下面装置实现铜与浓、稀硝酸反应,过程如下:
I.取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
Ⅱ.将洗涤后的铜丝做成匝数较多的螺旋状。
Ⅲ.按下图所示连接仪器、检查气密性、装入化学试剂。

(1)过程I发生反应的离子方程式是______________________。
(2)过程Ⅱ将铜丝做成螺旋状的目的是______________________。
(3)过程Ⅲ的后续操作如下:
①为使浓硝酸与铜丝接触.操作是______________________。当红棕色气体较多时,轻抽注射器使反应停止,关闭a,取下注射器。
②换入另一注射器后,打开b和分液漏斗活塞,玻璃管充满稀硝酸时,关闭b打开a,可见无色气体产生。稀硝酸充满玻璃管的实验目的是______________________。
(4)已知:NO+NO2+2NaOH 2NaNO2+H2O;2NO2+2NaOH NaNO3+NaNO2+H2O,NO和NO2的混合气体的组成可表示为NOx。将该混合气体通人NaOH溶液被完全吸收时,x的取值范围应为______________。













