-
下表为元素周期表的一部分,a、b、c…为元素周期表中前4周期的部分元素。
回答下列问题:
a
e
f
g
b
hh
c
d
[
d
(1)d3+的未成对电子数为________ 个;
(2)请比较e、f、g三种元素的第一电离能由大到小的顺序________(写元素符号)
(3)请写出h元素原子价电子轨道表示式________;
(4)ea3分子的电子式是________,其分子的空间构型是________,分子中e原子的杂化类型是________。
高二化学填空题中等难度题查看答案及解析
-
下表为周期表的一部分,其中的字母代表对应的元素,请针对这些元素回答下列问题.
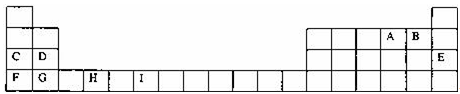
请回答下列问题:
(1)元素I的元素符号 ;已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的 周期 族.
(2)表中元素第一电离能最小的是 (填元素符号,下同),电负性最大的是 ,化学性质最稳定的是 .
(3)表中元素处于d区的是 (填元素符号).
(4)请举出F的金属性比C强的实验事实: ,并用原子结构理论解释其原因: .
高二化学填空题中等难度题查看答案及解析
-
表为周期表的一部分,其中的字母代表对应的元素,请针对这些元素回答下列问题.
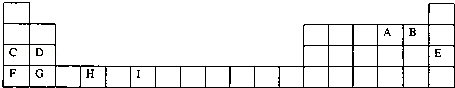
请回答下列问题:
(1)元素I的元素符号 ;已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的 周期 族.
(2)表中元素第一电离能最小的是 (填元素符号,下同),电负性最大的是 ,化学性质最稳定的是 .
(3)表中元素处于d区的是 (填元素符号).
(4)请举出F的金属性比C强的实验事实: ,并用原子结构理论解释其原因: .
高二化学推断题中等难度题查看答案及解析
-
下表为元素周期表中的一部分,列出了10种元素在元素周期表中的位置。用化学符号回答下列各问题。
主族
周期
IA
IIA
IIIA
IVA
VA
VIA
VIIA
0
2
⑥
⑦
3
①
③
⑤
⑧
⑩
4
②
④
⑨
(1)10种元素中,第一电离能最大的是_______;电负性最小的金属是________。
(2)①、③、⑤三种元素最高价氧化物对应的水化物中,碱性最强的是________。
(3)②、③、④三种元素形成的离子,离子半径由大到小的顺序是:______>_______>_______。
(4)①和⑧的最高价氧化物对应水化物的化学式为________和________。①和⑨两元素形成化合物的化学 式为______ _;该化合物灼烧时的焰色________色;该化合物的溶液与元素⑧的单质反应的化学方程式为 。
(5)①和⑤最高价氧化物对应水化物相互反应的化学方程式为 ;离子方程式为 。
(6)用电子式表示第三周期元素中由电负性最小的元素和电负性最大的元素形成化合物的形成过程 。
高二化学填空题困难题查看答案及解析
-
(7分)下表为元素周期表短周期的一部分请回答下列问题:
(1)A与B形成的阴离子可能有----------------------------------。(填化学式)
(2)五种元素形成的气态氢化物中 最稳定。(填化学式)
(3)写出D的氢化物在过量的B中燃烧的化学方程式___________________________。
(4)写出由A、B两种元素形成的非极性分子的电子式 。A、E两元素形成化合物的空间构型为_____________。
高二化学填空题简单题查看答案及解析
-
下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
a
b
c
d
e
f
g
h
(1)请画出上述元素h的原子结构示意图_______;元素h位于元素周期表的第_____区。
(2)e、g两种元素的气态氢化物中更稳定的是_______(写化学式);
(3)b2a2分子的电子式是________ ,该分子中存在的σ键与π键的个数比为_______。
(4)c、d两种元素中第一电离能较大的是_________(写元素符号)。
(5)f和g两种元素形成的化合物是______(填“离子化合物”“共价化合物”)。a2d分子是_________分子(填极性分子或者非极性分子)。
高二化学填空题中等难度题查看答案及解析
-
(9分)下表为元素周期表的一部分,a、b、c……为部分元素。回答下列问题:
a
f
h
i
b
e
j
c
d
g
k
l
(1)请写出d在元素周期表中的位置 ;
(2)请写出上述元素k的核外电子排布式 ;
(3)b、e、j三种元素的电负性由大到小的顺序 (写元素符号);此三种元素的第一电离能由大到小的顺序 (写元素符号);
(4)g、e两种元素的最高价氧化物对应的水合物的化学性质相似,请写出e元素最高价氧化物对应的水化物与a、c、h三种元素形成的化合物反应的离子方程式 ;
(5)j、k、l三种元素之间能以原子个数比1∶1两两形成互化物,这些互化物的性质类似于这些元素单质的性质。请写出k、l的互化物的电子式 ,它是由 键形成的 化合物(填“离子”或“共价”)。
高二化学填空题中等难度题查看答案及解析
-
下表为长式周期表的一部分,其中的编号代表对应的元素。
①
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
请回答下列问题:
(1)按电子排布,可把周期表中的元素划分成5个区,请在上图中划出区域并注明。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为 ;③和⑦形成的一种常见溶剂的化学式为 ,其立体构型为__________,键角为______。
(3)某元素原子的价电子排布式为nsnnpn+1,该元素原子的最外电子层上孤电子对数为 ;该元素与元素①形成的最简单分子X属于 分子(填“极性”或“非极性”)。
(4)元素④的第一电离能 元素⑤(选填“>”、“=”、“<”)的第一电离能;元素⑥的电负性 元素⑦(选填“>”、“=”、“<”)的电负性。
(5)元素⑥和①形成的化合物的结构式为 ; 元素⑨的基态原子核外电子排布式是 。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式
高二化学填空题困难题查看答案及解析
-
下表为元素周期表的一部分,列出了10种元素在元素周期表中的位置。试回答下列问题:
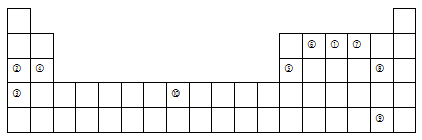
(1)写出表中⑥含有8个中子的原子的化学符号 ,元素⑦的氢化物与⑧的单质反应的离子方程式为 。
(2)元素⑩的核外电子排布式 。
(3) 根据元素周期表来比较④和Cs的金属性,要通过另一种元素作中介或桥梁进行比较, 这种元素是 (填元素符号)。
(4)据报道,美国科学家卡尔·克里斯特于1998年11月根据①合成了一种名为“N5”的物质,由于其极强的爆炸性,又称“盐粒炸弹”。迄今为止,人们对它的结构尚不清楚,只知道“N5”实际上是带正电荷的分子碎片,其结构是对称的,5个N排列成V形。如果5个N结合后都达到8电子结构,且含有2个N≡N键,则“N5”分子碎片的电子式为:__________________。
高二化学填空题简单题查看答案及解析
-
(11 分)下表为元素周期表的一部分,列出了7种元素在元素周期表中的位置:
族
周期
ⅠA
0
1
①
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2
②
③
④
3
⑤
⑥
⑦
请按要求回答下列问题:
(1)写出③的元素符号 。
(2)7种元素中,原子半径最小的是 (填序号)。
(3)元素④的氢化物与元素⑦的单质反应的离子方程式为 。
(4)元素⑤和元素⑥最高价氧化物的水化物碱性由强到弱关系为 (用化学式表示)。
(5)元素②形成的最简单氢化物的空间结构为 。
高二化学填空题中等难度题查看答案及解析