-
根据事实,写出298K时下列反应的热化学方程式:
(1)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,该反应的热化学方程式为__。
(2)1mol碳与适量水蒸气完全反应,生成一氧化碳气体和氢气,吸收131.3kJ热量。___。
(3)家用液化气中主要成分之一是丁烷。当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50kJ。试写出丁烷燃烧反应的热化学方程式___。
(4)1molHgO(s)分解为液态汞和氧气,吸热90.7kJ。__。
高二化学填空题简单题查看答案及解析
-
0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ的热量。
(1)写出反应的热化学方程式。
(2)已知H2O(l)转化为H2O(g)的△H=44kJ·mol-1,试计算11.2L(标准状况)气态乙硼烷完全燃烧生成气态水时放出的热量。
高二化学填空题中等难度题查看答案及解析
-
(8分)将0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5KJ的热量。
(1)写出上述反应的热化学方程式。
(2)已知H2O(l)转化为H2O(g)的△H=44KJ.mol_1,试计算11.2L(标准状况下)气态乙硼烷完全燃烧生成气态水时放出的热量。(请写出计算过程)
高二化学计算题中等难度题查看答案及解析
-
已知0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放
出649.5KJ的热量。
(1)写出反应的热化学方程式________
(2)已知H2O(l)转化为H2O(g)的△H=44KJ/mol,计算11.2L(标准状况)气态乙硼烷完全燃烧生成气态水时放出的热量为________。
高二化学填空题中等难度题查看答案及解析
-
0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学方程式是 。又已知:H2O(l)=H2O(g) △H=-44kJ/mol,则11.2升(标准状况下)乙硼完全燃烧时生成气态水时放出的热量为 。
高二化学填空题中等难度题查看答案及解析
-
(1)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学反应方程式为 ;
又知H2O(l)=H2O(g);△H=+44kJ/mol,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时,放出的热量是 kJ
(2)发射卫星时可用肼(N2H4)为燃料和NO2作氧化剂,这两者反应生成N2和水蒸气.又已知: ①N2(气)+2O2(气)=2NO2(气) △H=+67.7kJ/mol ②N2H4(气)+O2(气)=N2(气)+2H2O(气) △H=-534kJ/mol 试写出肼与NO2反应的热化学方程式:
(3)甲烷燃料电池:碱性电解质(铂为两极、电解液KOH溶液)
正极:___________ _____
负极:__________
总反应方程式: CH4+ 2O2 + 2OH- = CO32- + 3H2O
高二化学填空题困难题查看答案及解析
-
(1)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出热量649.5 中kJ,则表示乙硼烷燃烧热的热化学方程为 .
又已知:H2O(l)═H2O(g);△H=+44.0kJ/mol.则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量为 .
(2)恒温、恒压(1.01×105Pa)下,将2.0molSO2与amolO2的混合气体通入一个容积可变的密闭容器中,发生如下反应:2SO2(g)+O2(g)⇌2SO3(g);△H<0,T1℃下反应达平衡时,测得容器内n(SO3)=1.3mol,n(O2)=3.0mol,则a= .
高二化学填空题中等难度题查看答案及解析
-
(1)将0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,则乙硼烷的燃烧热的热化学方程式为______________。
(2)盖斯定律认为:不管化学过程是一步完成或分为数步完成,这个过程的热效应是相同的。某化学过程如图所示,
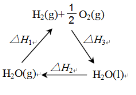
ΔH1、ΔH2、ΔH3三者之间的关系式为___________。
高二化学填空题中等难度题查看答案及解析
-
0.3moL气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态B2O3和液态水,放出649.5KJ热量,请写出乙硼烷燃烧的热化学方程式________;又已知:H2O(l)→H2O(g);△H=+44kJ/moL,则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量是________.
高二化学填空题中等难度题查看答案及解析
-
(1)0.3 mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出649.5 kJ热量,其热化学方程式为____。
(2)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式为2NO+2CO
2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间/s
0
1
2
c(NO)/ mol·L-1
1.00×10-3
4.50×10-4
2.50×10-4
c(CO)/mol·L-1
3.60×10-3
3.05×10-3
2.85×10-3
时间/s
3
4
5
c(NO)/ mol·L-1
1.50×10-4
1.00×10-4
1.00×10-4
c(CO)/ mol·L-1
2.75×10-3
2.70×10-3
2.70×10-3
请回答下列问题:
①前2s内的平均反应速率υ(N2)=____;
②上述条件下,该反应的平衡常数为____;
③上述条件下,测得某时刻反应体系中各物质的物质的量浓度均为0.01 mol/L,则此时反应处于____状态。(填“平衡”或“向右进行”或“向左进行”)
(3)实验室常用0.10 mol/L KMnO4标准酸性溶液来测定H2C2O4样品的纯度(标准液滴待测液),其反应原理为:5H2C2O4+2MnO4-+6H+=10CO2↑+2Mn2++8H2O。
① KMnO4标准液应装在____(填“酸式”或“碱式”)滴定管;
② 清水洗净滴定管后直接装入标准液,则测定结果会____;(填“偏大”或“偏小”或“不变”)
③ 滴定过程中发现一段时间后反应速率明显加快,除去温度的影响,你认为最有可能的原因是____。
高二化学综合题中等难度题查看答案及解析