-
铝及其化合物在生产、生活中用途广泛。
(1)航母升降机可用铝镁合金制造,销镁合金在焊接前应先用氢氧化钠溶液处理表面的氧化膜,发生反应的化学方程式为________。
(2)实验室欲以铝屑为起点制备氢氧化铝,如按Al→Al3+→Al(OH)3流程制备,使用最合适的药品是铝屑、稀硫酸、氨水,不用氢氧化钠溶液代替氨水的原因是________。写出该制备方案中第二步反应的离子方程式________。
(3)氢氧化铝是医用胃酸中和剂的一种,选用其作为胃酸中和剂的两个主要原因是________,________。
高一化学简答题中等难度题查看答案及解析
-
铝及其化合物在生产、生活中用途广泛。
(1)航母升降机可用铝镁合金制造,铝镁合金在焊接前应先用氢氧化钠溶液处理表面的氧化膜,发生反应的化学方程式为__________________________________________。
(2)实验室欲以铝屑为起点制备氢氧化铝,如按Al→Al3+→Al(OH)3流程制备,使用最合适的药品是铝屑、稀硫酸、氨水,不用氢氧化钠溶液代替氨水的原因是__________________________________________________________。写出该制备方案中第二步反应的离子方程式___________________________________________________________。
(3)氢氧化铝是医用胃酸中和剂的一种,选用其作为胃酸中和剂的两个主要原因是_____________________________________________。
(4)铝与NaOH溶液反应的离子方程式为____________________________________;同温同压下,在体积和浓度均为100 mL 2 mol·L-1的盐酸和NaOH溶液中各加入等质量的Al,产生气体的体积之比为5∶6,则所加Al的质量为________。
高一化学填空题中等难度题查看答案及解析
-
(14分)铝是应用最广泛的金属之一,铝的化合物在生产和生活中也有许多用途。
(1)铝在反应中容易失去电子,发生 反应(填氧化或还原),生成铝离子,铝离子的结构示意图是 。
(2)生产中曾用铝热反应焊接钢轨,写出铝与氧化铁发生反应的化学方程式为并标出电子转移的方向和数目: 。
(3)胃舒平是治疗胃酸过多的常用药物,其中含有的有效成分是氢氧化铝,其治疗原理是(用离子方程式表示): ;
(4)在同温同压下,等质量的铝分别投入足量的稀盐酸和NaOH溶液中,产生气体的体积之比为 。
(5)铝合金在空气中很稳定,可以制造多种建筑型材。向一只小烧杯里加入少量CuSO4溶液,把一小块铝合金浸入溶液中,1~2分钟后将铝合金取出,无明显现象。将另一小块铝合金先放入NaOH溶液里,片刻后取出,用蒸馏水冲洗后浸入CuSO4溶液里,1~2分钟后将铝片取出,发现铝片表面有亮红色的固体附着,NaOH溶液的作用是 。
高一化学填空题中等难度题查看答案及解析
-
铝合金在日常生活、航空航天和汽车制造等方面均有广泛用途,下列说法不正确的是
A.铝元素在地壳中的含量高,储量丰富
B.铝的表面容易形成致密的氧化膜,抗腐蚀性能好
C.铝的氧化膜熔点高,难溶于水,常温下不与任何酸、碱反应
D.镁、铝合金密度小,强度大
高一化学选择题中等难度题查看答案及解析
-
铝合金在日常生活、航空航天和汽车制造等方面均有广泛用途。下列关于铝的说法不正确的是 ( )
A.铝的表面容易形成致密的氧化膜,抗腐蚀性能好
B.工业上可以用电解法冶炼铝
C.铝元素在地壳中的含量高,储量丰富
D.常温下不与任何酸、碱反应
高一化学选择题简单题查看答案及解析
-
铝合金在日常生活、航空航天和汽车制造等方面均有广泛用途.下列关于铝的说法不正确的是( )
A.铝的表面容易形成致密的氧化膜,抗腐蚀性能好
B.工业上可以用电解法冶炼铝
C.铝元素在地壳中的含量高,储量丰富
D.常温下不与任何酸、碱反应高一化学选择题中等难度题查看答案及解析
-
铝合金在日常生活、航空航天和汽车制造等方面均有广泛用途。下列关于铝的说法不正确的是
A.铝的表面容易形成致密的氧化膜,抗腐蚀性能好
B.常温下不与任何碱反应
C.铝元素在地壳中的含量高,储量丰富
D.工业上可以用电解法冶炼铝
高一化学选择题简单题查看答案及解析
-
(10分)铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。
(1)铝粉和铁的氧化物(FeO·Fe2O3)可配成铝热剂用于焊接钢轨,反应的化学方程式是 。
(2)NaOH溶液可以除去铝表面的氧化膜,在处理过程中常会产生H2,产生H2的离子方程式是 。
(3)工业上以铝土矿(Al2O3·H2O)为原料生产铝,主要包括下列过程:
i.将粉粹、筛选后的铝土矿溶解在NaOH溶液中;
ii.加入过量的试剂A使所得溶液中析出Al(OH)3固体;
iii.使Al(OH)3脱水生成Al2O3;
iv.电解熔融Al2O3生成Al。
铝土矿粉粹的目的是 ,试剂A的化学式是 ,电解熔融Al2O3时,加入冰晶石,其作用是 。
(4)明矾化学式为KAl(SO4)2·12H2O,向明矾溶液中加入Ba(OH)2溶液,当溶液中的SO42-恰好沉淀时,铝元素的存在形式是 。
(5)美国普度大学研究开发出一种利用铝镓(镓:Ga)合金制取氢气的新工艺(如下图所示)。
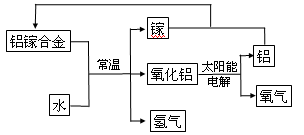
i.写出常温下铝镓合金产生氢气的化学方程式 。
ii.下列有关该工艺的说法正确的是 。
A.该过程中,能量的转化形式只有两种
B.铝镓合金可以循环使用
C.铝镓合金的熔点比金属铝低
D.该工艺可利用太阳能分解水
高一化学简答题极难题查看答案及解析
-
下列关于物质的用途,叙述不正确的是
A.过氧化钠可用作供氧剂 B.三氧化二铁可用做漆料
C.镁铝合金可用作制造飞机的材料 D.高纯硅用来制造光导纤维
高一化学选择题简单题查看答案及解析
-
铝合金在日常生活、建筑装潢、航空航天和汽车制造等方面均有着广泛的用途.下列关于铝合金具有广泛用途的分析不正确的是( )
A.铝元素在地壳中的含量高,储量丰富
B.铝容易形成致密的氧化膜,抗腐蚀性能好
C.铝化学性质稳定,常温下不与任何酸碱反应
D.铝的冶炼技术基本成熟,可以大量生产
高一化学选择题简单题查看答案及解析