-
已知 2Fe3++2I﹣═2Fe2++I2,Br2+2Fe2+═2Br﹣+2Fe3+。往含有 FeBr2、FeI2 的混合液中通 入一定量的氯气后,再滴加少量的 KSCN 溶液,溶液变为红色,则下列说法不正确的是
A. 按 I﹣、Fe2+、Br﹣的顺序还原性逐渐减弱
B. 通入氯气后原溶液中 Fe2+一定被氧化
C. 原溶液中 Br﹣一定被氧化
D. 不能确定通入氯气后的溶液中是否还存在 Fe2+
高二化学单选题中等难度题查看答案及解析
-
已知 2Fe3++2I﹣═2Fe2++I2,Br2+2Fe2+═2Br﹣+2Fe3+。往含有 FeBr2、FeI2 的混合液中通 入一定量的氯气后,再滴加少量的 KSCN 溶液,溶液变为红色,则下列说法不正确的是
A. 按 I﹣、Fe2+、Br﹣的顺序还原性逐渐减弱
B. 通入氯气后原溶液中 Fe2+一定被氧化
C. 原溶液中 Br﹣一定被氧化
D. 不能确定通入氯气后的溶液中是否还存在 Fe2+
高二化学单选题中等难度题查看答案及解析
-
已知:2Fe3++2I-===2Fe2++I2,2Fe2++Br2===2Fe3++2Br-。现向含有FeBr2、FeI2的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色,则下列叙述中不正确的是( )
A. 两个反应转移电子数之比是1:1
B. 原溶液中I-一定被氧化,Br-可能被氧化
C. 若向反应后的溶液中滴加少量K3[ Fe(CN)6]溶液,没有任何现象,则Br-一定被氧化
D. 若向含有FeBr2、FeI2的溶液中加入一定量的溴水,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色,说明原溶液中Fe2+、I-均被氧化
高二化学单选题中等难度题查看答案及解析
-
已知2Fe3++2I-===I2+2Fe2+、2Fe2++Br2===2Br-+2Fe3+。现向含有FeBr2、FeI2的溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色,则下列叙述中正确的是( )
①氧化性:Br2>Fe3+>I2
②原溶液中Br-一定被氧化
③通入氯气后,原溶液中的Fe2+一定被氧化
④不能确定通入氯气后的溶液中是否还存在Fe2+
⑤若取少量所得溶液,加入CCl4后静置,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中Fe2+、Br-均被完全氧化
A. ①②③④ B. ①③④⑤ C. ②④⑤ D. ①②③④⑤
高二化学单选题中等难度题查看答案及解析
-
已知2Fe3++2I-=2Fe2++I2,Br2+2Fe2+=2Br-+2Fe3+。往含有等物质的量的FeBr2、FeI2的混合液中通入一定量的氯气后,再滴加少量的KSCN溶液,溶液变为红色,则下列方程式书写不合理的是
A.2I-+2Fe2++2Cl2=I2+4Cl-+2Fe3+
B.2Br-+4I-+2Fe2++4Cl2=2I2+Br2+8Cl-+2Fe3+
C.2Br-+2I-+2Fe2++3Cl2=I2+Br2+6Cl-+2Fe3+
D.4I-+2Fe2++3Cl2=2I2+6Cl-+2Fe3+
高二化学选择题困难题查看答案及解析
-
已知2Fe3++2I﹣═2Fe2++I2、Br2+2Fe2+═2Br﹣+2Fe3+。现向含有FeBr2、FeI2的某溶液中通入一定量的氯气,再向反应后的溶液中滴加少量的KSCN溶液,结果溶液变为红色,则下列叙述中正确的是
①按I
﹣、Fe2+、Br﹣的顺序还原性逐渐减弱;
②原溶液中Br﹣一定被氧化;
③通入氯气后原溶液中Fe2+一定被氧化;
④不能确定通入氯气后的溶液中是否还存在Fe2+;
⑤若取少量所得溶液,加入CCl4充分振荡后静置,向上层溶液中加入足量的AgNO3溶液,只产生白色沉淀,说明原溶液中Fe2+、Br﹣均被完全氧化.
A.①②③④ B.①③④⑤ C.②④⑤ D.①②③
④⑤
高二化学选择题简单题查看答案及解析
-
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示。已知:2Fe2++Br2===2Fe3++2Br- 2Fe3++2I-===2Fe2++I2 ,则下列有关说法中,不正确的是
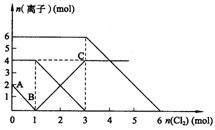
A.还原性:
B.原混合溶液中FeBr2的物质的量为6mol
C.当通入2molCl2时,溶液中已发生的离子反应可表示为:
2Fe2++2I-+2Cl2==2Fe3++I2+4Cl-
D.原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3
高二化学选择题中等难度题查看答案及解析
-
已知:2Fe2++Br2=2Fe3++2Br-,2Fe3++2I-=2Fe2++I2。向FeI2、FeBr2的混合溶液中通入适量Cl2,溶液中某些离子的物质的量变化如图所示,下列说法正确的是( )
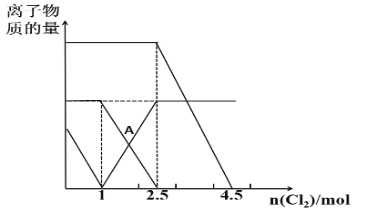
A.三种离子的还原性强弱关系是:Br->Fe2+>I-
B.A点表示Fe2+正好反应了一半
C.原溶液中:n(Fe2+)︰n(I-)︰n(Br-)=2︰1︰3
D.当通入2.5molCl2时,溶液中已发生的离子反应可表示为:6Fe2++4I-+5Cl2=6Fe3++2I2+10Cl-
高二化学多选题困难题查看答案及解析
-
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示.已知:2Fe2++Br2═2Fe3++2Br﹣、2Fe3++2I﹣═2Fe2++I2,则下列有关说法中不正确的是( )
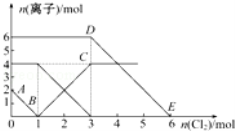
A.还原性:I﹣>Fe2+>Br﹣
B.线段AB表示Fe2+被氯气氧化
C.线段BC表示生成4 mol Fe3+
D.原溶液中n(Br﹣)=6 mol
高二化学选择题困难题查看答案及解析
-
已知:2Fe2++Br2=2Fe3++2Br-,2Fe3++2I-=2Fe2++I2。向FeI2、FeBr2的混合溶液中通入适量Cl2,溶液中某些离子的物质的量变化如下图所示。下列说法中,不正确的是
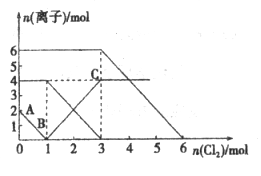
A. 还原性:I->Fe2+>Br-
B. 原混合溶液中FeBr2的物质的量为6 mol
C. 原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3
D. 当通入2mol Cl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
高二化学单选题困难题查看答案及解析