-
下列有关说法中正确的是( )
A. 已知25 ℃时NH4CN溶液显碱性,则25 ℃时的电离常数K(NH3·H2O)>K(HCN)
B. 室温时, 相同体积、相同pH的盐酸和醋酸溶液中由水电离出的c(H+):盐酸小于醋酸溶液
C. 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,向含有Cl-、CrO42-且浓度均为0.010 mol·L-1溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时, CrO42-先产生沉淀
D. 常温下pH=7的CH3COOH和NaOH混合溶液中,c(Na+)>c(CH3COO-)
高二化学单选题中等难度题查看答案及解析
-
下列说法中,正确的是
A. 已知25℃时NH4CN水溶液显碱性,则25℃时的电离平衡常数K(NH3·H2O)>K(HCN)
B. 25℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL0.01 mol·L-1NH4Cl溶液中的Ksp小
C. pH试纸测得新制氯水的pH为4.5
D. FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3
高二化学单选题中等难度题查看答案及解析
-
下列判断中,正确的是( )
A. 已知25 ℃时NH4CN显碱性,则25 ℃时的电离常数K(NH3·H2O)>K(HCN)
B. 25 ℃时,Mg(OH)2固体在20 mL0.01 mol·L-1氨水中的Ksp比在20 mL0.01 mol·L-1 NH4Cl溶液中的Ksp小
C. pH试纸测得新制氯水的pH为4
D. FeCl3溶液和Fe2(SO4)3溶液加热蒸干.灼烧都得到Fe2O3
高二化学单选题中等难度题查看答案及解析
-
下列判断中,正确的是
A.已知25 ℃时NH4CN显碱性,则25 ℃时的电离常数K(NH3·H2O)>K(HCN)
B.25 ℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1 NH4Cl溶液中的Ksp小
C.pH试纸测得新制氯水的pH为4
D.FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3
高二化学选择题中等难度题查看答案及解析
-
下列判断中,正确的是
A.已知25 ℃时NH4CN显碱性,则25 ℃时的电离常数K(NH3·H2O)>K(HCN)
B.25 ℃时,Mg(OH)2固体在20 mL0.01 mol·L-1氨水中的Ksp比在20 mL0.01 mol·L-1 NH4Cl溶液中的Ksp小
C.pH试纸测得新制氯水的pH为4
D.FeCl3溶液和Fe2(SO4)3溶液加热蒸干.灼烧都得到Fe2O3
高二化学选择题中等难度题查看答案及解析
-
已知,常温下CH3COOH和NH3·H2O的电离常数均为1.8×10-5。某小组进行如图三组实验且实验II、III中Mg(OH)2固体均溶解。下列说法正确的是
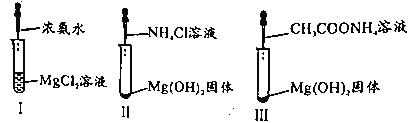
A.I中现象说明NH3·H2O碱性强于Mg(OH)2
B.II中总反应为2H++Mg(OH)2=Mg2++2H2O
C.实验II、III研究NH4+对Mg(OH)2溶解的作用原理
D.III中CH3COONH4浓度越小,越有利于沉淀的溶解
高二化学单选题中等难度题查看答案及解析
-
已知,常温下CH3COOH和NH3·H2O的电离常数均为1.8×10-5。某小组进行如图三组实验且实验II、III中Mg(OH)2固体均溶解。下列说法正确的是

A.I中现象说明NH3·H2O碱性强于Mg(OH)2
B.II中总反应为2H++Mg(OH)2=Mg2++2H2O
C.实验II、III研究NH4+对Mg(OH)2溶解的作用原理
D.III中CH3COONH4浓度越小,越有利于沉淀的溶解
高二化学单选题中等难度题查看答案及解析
-
常温下,向20mL0.1mol/L氨水溶液中滴加一定浓度的稀盐酸,溶液中由水电离的氢离子浓度随加入盐酸体积的变化如图所示。则下列说法正确的是( )
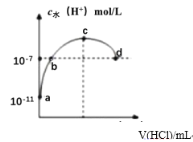
A.常温下,NH3·H2O的电离常数约为1×10-5
B.a、b之间的点一定满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+)
C.c点溶液中:c(NH4+)= c(Cl-)
D.d点代表两溶液恰好完全反应
高二化学单选题中等难度题查看答案及解析
-
下列有关叙述正确的是
A. NH3·H2O的电离平衡常数随着温度升高而减小
B.在0.10 mol·L-1 CH3COOH溶液中,加入少量CH3COONa晶体后,溶液的pH减小
C.强酸、强碱和大部分盐类都是强电解质,其他化合物都是弱电解质
D.相同温度下,醋酸溶液的导电能力可能比稀硫酸强
高二化学选择题中等难度题查看答案及解析
-
25℃时,将1 mol NH4NO3溶于水,向该溶液滴加b L氨水后溶液呈中性,据此判断下列说法中不正确的是(NH3·H2O的电离平衡常数取Kb=2×10-5mol·L-1)
A.滴加氨水的过程中,水的电离平衡将正向移动
B.滴加b L氨水后的溶液中,n(NH4+) = 200 n(NH3·H2O) = 1 mol
C.所滴加氨水的浓度为0.005 / b mol·L-1
D.滴加b L氨水后的溶液中各离子浓度大小是:c(NH4+) = c(NO3-) > c(H+) = c(OH-)
高二化学选择题困难题查看答案及解析