-
(10分)
(1)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液
(假设无损失),
①__________和_________两种粒子的物质的量之和等于0.1mol。
②_________和_________两种粒子的物质的量之和比OH―多0.05mol。
(2)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中
各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
①若溶液中只溶解了一种溶质,该溶质的名称是________,上述离子浓度大小
顺序关系中正确的是(选填序号)________。
②若上述关系中C是正确的,则溶液中溶质的化学式是________。
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前
c(HCl)________c(NH3·H2O)(填“>”、“<”、或“=”,下同),混合后
溶液中c(NH4+)与c(Cl-)的关系c(NH4+)________c(Cl-)
高三化学填空题中等难度题查看答案及解析
-
(1)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失)
①________和________两种粒子的物质的量之和等于0.1mol.
②________和________两种粒子的物质的量之和比OH-多0.05mol.
(2)已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中
各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
①若溶液中只溶解了一种溶质,该溶质的名称是________,上述离子浓度大小顺序关系中正确的是(选填序号)________.
②若上述关系中C是正确的,则溶液中溶质的化学式是________.
③若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________c(填“>”、“<”、或“=”,下同),混合后溶液中c(NH4+)与c(Cl-)的关系c(NH4+)________c(Cl-)高三化学填空题中等难度题查看答案及解析
-
实验室将NH4Cl和Ca(OH)2各0.1mol固体混合共热,反应后的残渣溶于足量的蒸馏水中,得到的溶液中氨和Ca(OH)2皆为0.05mol (假设没有氨气逸出),在溶液中滴加一定浓度的盐酸,若Ca(OH)2为强碱,下列说法正确的是
A. n(HCl)=0.1mol,c(H+)+c(NH4+)>c(OH-)
B. n(HCl)=0.15mol,2c(H+)+2c(NH4+)=c(Ca2+)+2c(OH-)
C. n(HCl)=0.20mol,c(H+)+c(NH4+)=c(Ca2+)+c(OH-)
D. 残渣的组成为:n[(Ca(OH)2]=0.05 mol,n(CaCl2)=0.05 mol
高三化学多选题困难题查看答案及解析
-
室温下有下列四种溶液:①0.1 mol/L氨水 ②0.1 mol/L NH4Cl溶液 ③混合溶液:盐酸和NH4Cl的浓度均为0.1 mol/L ④混合溶液:NaOH和氨水的浓度均为0.1 mol/L。四种溶液中c(NH4+)由大到小排列正确的是
A.②③④① B.②①③④ C.③②④① D.③②①④
高三化学单选题中等难度题查看答案及解析
-
室温下有下列四种溶液:①0.1 mol/L氨水 ②0.1 mol/L NH4Cl溶液 ③混合溶液:盐酸和NH4Cl的浓度均为0.1 mol/L ④混合溶液:NaOH和氨水的浓度均为0.1 mol/L。四种溶液中c(NH4+)由大到小排列正确的是
A.②③④① B.②①③④ C.③②④① D.③②①④
高三化学单选题中等难度题查看答案及解析
-
室温下有下列四种溶液:①0.1 mol/L氨水 ②0.1 mol/L NH4Cl溶液 ③混合溶液:盐酸和NH4Cl的浓度均为0.1 mol/L ④混合溶液:NaOH和氨水的浓度均为0.1 mol/L。四种溶液中c(NH4+)由大到小排列正确的是
A.②③④① B.②①③④ C.③②④① D.③②①④
高三化学选择题中等难度题查看答案及解析
-
室温下有下列四种溶液:①0.1 mol/L氨水 ②0.1 mol/L NH4Cl溶液 ③混合溶液:盐酸和NH4Cl的浓度均为0.1 mol/L ④混合溶液:NaOH和氨水的浓度均为0.1 mol/L。四种溶液中c(NH4+)由大到小排列正确的是
A.②③④① B.②①③④ C.③②④① D.③②①④
高三化学选择题中等难度题查看答案及解析
-
下列有关溶液中微粒的物质的量浓度的关系,正确的是
A.0.1 mol·L-1的NH4Cl溶液与0.05 mol·L-1的NaOH溶液等体积混合的溶液:c(Cl-)>c(Na+)>c(
)>c(OH-)>c(H+)
B.等物质的量的NaClO、NaHCO3混合溶液:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(
)
C.pH=2的HA溶液与pH=12的MOH溶液等体积混合:c(M+)=c(A-)>c(OH-)=c(H+)
D.某二元弱酸的酸式盐NaHA溶液:c(OH-)+c(H2A)=c(H+)+2c(A2-)
高三化学选择题困难题查看答案及解析
-
室温时,向20 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生,且混合溶液的体积可看成混合前两溶液的体积之和),下列说法不正确的是:
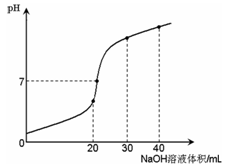
A.PH=7时,溶液中c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
B.当V(NaOH)=20mL时,溶液中水的电离程度比纯水大
C.当V(NaOH)=30mL时,溶液中 c(SO42-)+ c(H+)== c(NH3·H2O) + c(OH-)
D.滴加NaOH溶液从30mL至40mL,溶液中Na+与SO42-浓度之和始终为0.1 mol·L-1
高三化学选择题困难题查看答案及解析
-
室温时,向20 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生,且混合溶液的体积可看成混合前两溶液的体积之和),下列说法不正确的是:

PH=7时,溶液中c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
当V(NaOH)=20mL时,溶液中水的电离程度比纯水大
当V(NaOH)=30mL时,溶液中 c(SO42-)+ c(H+)=c(NH3·H2O) + c(OH-)
滴加NaOH溶液从30mL至40mL,溶液中Na+与SO42-浓度之和始终为0.1 mol·L-1
高三化学选择题困难题查看答案及解析