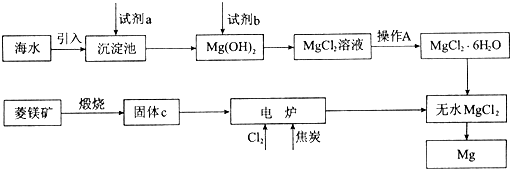
回答下列问题:
(1)试剂a的化学式是______.
(2)加入试剂b发生反应的离子方程式是______.
(3)操作A是蒸发浓缩、冷却结晶、______.
(4)在电炉中参加反应的n(Cl2):n(焦炭)=1:1,则该反应的化学方程式是______ MgCl2+CO
高一化学解答题中等难度题

高一化学解答题中等难度题
(7分)金属镁的制取主要有两种途径,大约60%的镁是从海水中提取的,其余来自于含镁丰富的矿石,比如菱镁矿(主要成分为MgCO3)。从不同途径获得镁的流程如下:
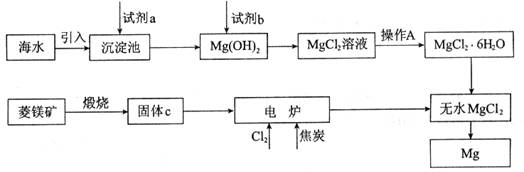
回答下列问题:
(1)试剂a的化学式是__________。
(2)加入试剂b发生反应的离子方程式是__________。
(3)操作A是蒸发浓缩、冷却结晶、__________。
(4)在电炉中参加反应的n(Cl2):n(焦炭)=1:1,则该反应的化学方程式是__________。
(5)上述制镁的流程中,为降低成本、减少污染可采取的措施是__________。(写出一种即可)
高一化学填空题简单题查看答案及解析

高一化学解答题中等难度题查看答案及解析
高一化学解答题中等难度题查看答案及解析
硫酸镁晶体(MgSO4·7H2O)是一种重要的化工原料。以菱镁矿(主要成分是MgCO3,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体的流程如下:

(1)MgCO3溶于稀硫酸的离子方程式是_________________________。
(2)加入H2O2溶液的目的是____________________(用离子方程式表示)。
(3)已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Mg2+ | Fe2+ | Fe3+ |
| 开始沉淀 | 9.1 | 7.6 | 1.9 |
| 完全沉淀 | 11.1 | 9.7 | 3.2 |
“沉淀”步骤中,用氨水调节溶液pH的范围是______________________________。
(4)“过滤”所得滤液中存在大量的阳离子有Mg2+、____________。
(5)“结晶”步骤中需蒸发浓缩滤液,使用的仪器有铁架台、酒精灯和_________________。
高一化学综合题中等难度题查看答案及解析
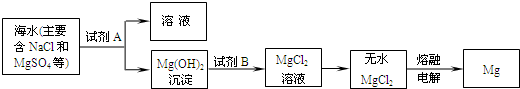
(10分)镁及其合金是一种用途很广的金属材料,海水中镁的含量为1.10 mg·L-1,目前世界上60%的镁是从海水中提取的。主要步骤如下:
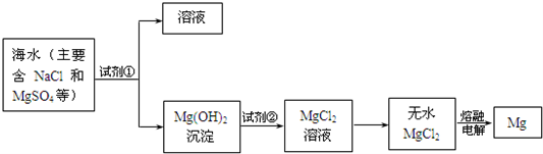
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用 ,要使完全转化为沉淀,加入试剂①的量应 ;
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是 ;
(3)试剂②可以选用 ;
(4)无水MgCl2在熔融状态下通电会产生Mg和Cl2,写出该反应的化学方程式 ;
(5)假设海水中镁元素全部存在于MgSO4中,则海水中MgSO4的含量为 mg·L-1,若某工厂每天生产1.00 t镁,则每天需要海水的体积为 L。
高一化学实验题极难题查看答案及解析
高一化学填空题中等难度题查看答案及解析
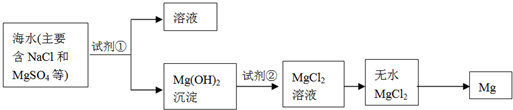
(10分)镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
(1)为了使转化为
,试剂①可以选用,要使
完全转化为沉淀,加入试剂①的量应;
(2)加入试剂①后,能够分离得到沉淀的方法是;
(3)试剂②可以选用;
(4)无水在熔融状态下,通电后会产生
和
,该反应的化学方程式为:
。
高一化学实验题简单题查看答案及解析
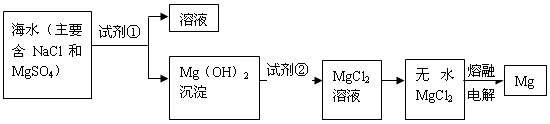
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
(1)为了使MgS04转化为Mg(OH)2,试剂①可以选用____(填化学式)。
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是____。
(3)试剂②可以选用 ___(填化学式)。
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为:_________________。
高一化学填空题中等难度题查看答案及解析
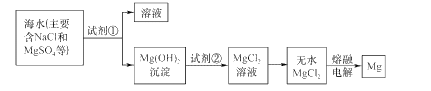
镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
试回答下列问题:
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用______(填试剂名称),反应的离子方程式为_____;
(2)加入试剂①后,能够分离得到Mg(OH)2沉淀的方法是______;
(3)试剂②可以选用______;
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,写出该反应的化学方程式______.
高一化学实验题简单题查看答案及解析
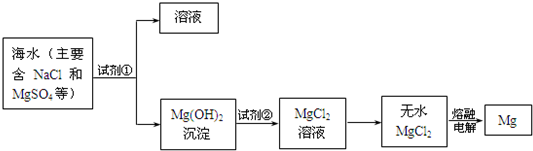
镁及其合金是用途很广的金属材料,目前世界上60%的镁是从海水中提取的。主要步骤如下:
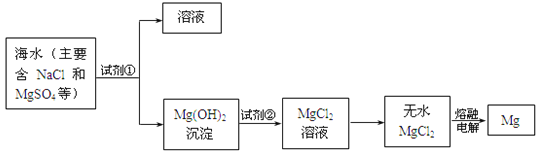
(1)为了使MgSO4转化为Mg(OH)2,试剂①可以选用_________;
(2)无水MgCl2在熔融状态下,通电后产生镁和氯气,该反应的化学方程式为__________________;
(3)电解后产生的副产物氯气可用于工业制漂白粉。某兴趣小组模拟工业制漂白粉,设计了下图的实验装置。
已知:①氯气和碱反应放出热量。②6Cl2+6Ca(OH)25CaCl2+Ca(ClO3)2+6H2O
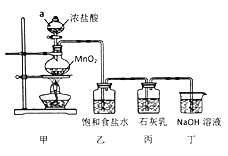
回答下列问题:
①甲装置中仪器a的名称是____________________;
②装置乙中饱和食盐水的作用是__________________________________;
③制取漂白粉的化学方程式是_____________________________________;
④该小组制得的漂白粉中n(CaCl2)远大于n(Ca(ClO)2],其主要原因是_________;
⑤为提高丙中Ca(ClO)2的含量,可采取的措施是_______________(任写一种即可)。
高一化学实验题中等难度题查看答案及解析