-
工业制硫酸的关键步骤之一为SO2的接触氧化:2SO2(g)+O2(g) 2SO3(g);△H=-196.6kJ/mol
2SO3(g);△H=-196.6kJ/mol
现在一容积为2 L的密闭容器中充入2 mol SO2、1 molO2,加入固体催化剂,保持温度在450℃使之发生反应,5 min时达到平衡,测得平衡时体系的压强减小了30%。下列说法正确的是
A.SO2的转化率为30%
B.反应共放出了196.6 kJ的热量
C.用SO2表示的5 min内的平均反应速率为0.36 mol·L—1.min—1
D.相同条件下,起始时若加入2 molSO3,达到的平衡状态完全相同
-
(9分)工业上以黄铁矿为原料生产硫酸,其中重要的一步是催化氧化(生产中保持恒温恒容条件):2SO2(g)+O2(g) 2SO3(g) △H=-196.6 kJ·mol-1
2SO3(g) △H=-196.6 kJ·mol-1
(1)生产中为提高反应速率和SO2的转化率,下列措施可行的是。
A.向装置中充入O2 B.升高温度
C.向装置中充入N2 D.向装置中充入过量的SO2
(2)恒温恒压,通入3mol SO2 和2mol O2 及固体催化剂,平衡时容器内气体体积为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为 5mol SO2(g)、3.5 mol O2(g)、1mol SO3(g),下列说法正确的是________
A.第一次平衡时反应放出的热量为294.9kJ
B.两次平衡SO2的转化率相等
C.两次平衡时的O2体积分数相等
D.第二次平衡时SO3的体积分数等于2/9
(3)500 ℃时将10 mol SO2和5.0 mol O2置于体积为1L的恒容密闭容器中,SO2转化为SO3的平衡转化率为0.95。则500℃时的平衡常数K=。
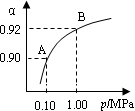
(4)550 ℃,A、B表示不同压强下的平衡转化率(如图),通常工业生产中采用常压的原因是 ,
并比较不同压强下的平衡常数:K(0.10 MPa)________K(1.0 MPa)。
-
(8分)硫酸生产中,SO2催化氧化生成SO3:2SO2 (g)+O2(g) 2SO3(g) ΔH= —196.6Kj/mol
2SO3(g) ΔH= —196.6Kj/mol
(1)t1℃时,若将2.0mol SO2和1.0mol O2置于10L恒温恒容密闭容器中,8min后反应达到平衡,SO2的平衡转化率为80%,则这段时间内SO3的平均反应速率为 ,该温度下上述反应的平衡常数K为
(2)该反应达到化学平衡后,以下操作将使平衡正向移动并能提高SO2转化率的是
A.向容器中通入少量O2
B.向容器中通入少量SO2
C.使用催化剂
D.降低温度
E.向容器中通入少量氦气
(3)下列叙述能证明该反应已达到化学平衡状态的是
A.容器内压强不再发生变化
B.SO2的体积分数不再发生变化
C.容器内气体原子总数不再发生变化
D.相同时间内消耗2n molSO2的同时生成2n molSO3
E.反应体系中SO2、O2、SO3的体积比为2:1:2
-
(10分)硫酸是工业生产中最为重要的产品之一。在催化反应室里进行的反应为:
2SO2(g)+O2(g) 2SO3(g) ΔH= –196.6 kJ·mol-1
2SO3(g) ΔH= –196.6 kJ·mol-1
(1)该反应发生的条件通常是400~500℃、和。
(2)SO3在(填设备名称)中用(填试剂名称)吸收。
(3)研究SO2 、NO2、CO等大气污染气体的处理具有重要意义。
已知: 2NO(g)+O2(g) 2NO2(g) ΔH= –113.0 kJ·mol-1
2NO2(g) ΔH= –113.0 kJ·mol-1
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=________kJ·mol-1。
SO3(g)+NO(g)的ΔH=________kJ·mol-1。
一定条件下,将NO2与SO2以物质的量之比1:2置于恒容密闭容器中发生上述反应,下列能说明反应达到平衡状态的是。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2的物质的量之比为1:6,则平衡常数K=________。
-
硫酸工业中接触氧化是最重要的一个反应:2SO2(g) + O2(g)  2SO3(g) △H= -197kJ/mol。为了研究这一反应,在体积为2L的密闭容积中,投入2mol SO2,1molO2,然后控制反应温度,在反应进行至20min时加入一定的催化剂,测定并记录一定时间内容器内SO3的物质的量,得到下表:
2SO3(g) △H= -197kJ/mol。为了研究这一反应,在体积为2L的密闭容积中,投入2mol SO2,1molO2,然后控制反应温度,在反应进行至20min时加入一定的催化剂,测定并记录一定时间内容器内SO3的物质的量,得到下表:
| 时间/min | 10 | 20 | 30 | 40 | 50 |
| N(SO3)/mol | 0.4 | 0.6 | 1.2 | 1.6 | 1.6 |
(1)反应前10 min,用O2表示该反应的反应速率v(O2)= 。
(2)该温度下,该反应的平衡常数为 。
(3)在反应进行至50min时,再向容器中充入2molSO2和1molO2,达到新平衡后,SO2的转化率将 。(填“增大”、“减小”或“不变”)
(4)保持温度不变,若在该容器中只投入2mol SO3,达到平衡时,反应吸收的热量为 kJ。
-
工业制硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。
(1)某温度下,2SO2(g)+O2(g) 2SO3(g) △H= -197 kJ/mol。开始时在10 L的密闭容器中加入4.0 molSO2(g)和10.0 molO2(g),当反应达到平衡时共放出197kJ的热量,该温度下的平衡常数K=_________,升高温度K将_____________(增大、减小或不变)。
2SO3(g) △H= -197 kJ/mol。开始时在10 L的密闭容器中加入4.0 molSO2(g)和10.0 molO2(g),当反应达到平衡时共放出197kJ的热量,该温度下的平衡常数K=_________,升高温度K将_____________(增大、减小或不变)。
(2)一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2,发生下列反应:2SO2(g)+O2(g) 2SO3(g),达到平衡后,改变下述条件,SO2、O2、SO3的平衡浓度都比原来增大的是__________________(填字母)。
2SO3(g),达到平衡后,改变下述条件,SO2、O2、SO3的平衡浓度都比原来增大的是__________________(填字母)。
A.恒温恒容,充入2mol SO3 B.恒温恒容,充入2mol N2
C.恒温恒压,充入1 mol SO3 D.升高温度
(3)在一密闭容器中进行下列反应:2SO2(g)+O2(g) 2SO3(g),化学兴趣小组的同学探究了其他条件不变时,改变某一条件时对上述反应的影响,并根据实验数据作出了下列关系图。下列判断中正确的是 ____________(填字母)。
2SO3(g),化学兴趣小组的同学探究了其他条件不变时,改变某一条件时对上述反应的影响,并根据实验数据作出了下列关系图。下列判断中正确的是 ____________(填字母)。
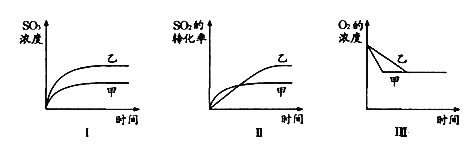
A.图Ⅰ研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高
C.图Ⅱ研究的是温度对反应的影响,且乙的温度较低
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
(4)某实验小组设想如右图所示装置用电化学原理生产硫酸,写出通入SO2的电极的电极反应式:___________。

(5)焙烧产生的SO2可用于制硫酸。已知25℃、101 kPa时:① 2SO2(g)+O2(g) 2SO3(g)△H1= —197 kJ/mol;② H2O(g)=H2O(l)△H2= —44 kJ/mol;③ 2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) △H3= —545 kJ/mol。写出SO3(g)与H2O(l)反应的热化学方程式是_____________________________。
2SO3(g)△H1= —197 kJ/mol;② H2O(g)=H2O(l)△H2= —44 kJ/mol;③ 2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) △H3= —545 kJ/mol。写出SO3(g)与H2O(l)反应的热化学方程式是_____________________________。
(6)由硫酸可制得硫酸盐,在一定温度下,向K2SO4溶液中滴加Na2CO3溶液和BaCl2溶液,当两种沉淀共存时,SO42-和CO32-的浓度之比___________________________。 (已知该温度时,Ksp(BaSO4)=1.3×10-10,Ksp(BaCO3)= 5.2×10-9。)
-
氮和硫的氧化物的综合利用是目前研究的热点之一。已知:
i.N2(g)+O2(g)=2NO(g) △H=+180.0 kJ·mol-1
ii.2SO2(g)+O2(g)=2SO3(g) △H=-196.6 kJ·mol-1
iii.2NO(g)+O2(g)=2NO2(g) △H=-113.0 kJ·mol-1
(1)反应iV:2NO2(g)+2SO2(g)=2SO3(g)+N2(g)+O2(g)的 △H=________;该反应在密闭容器中达到平衡后,只改变下列条件,一定能使N2的平衡体积分数增大的是______(填选项字母)。
A 缩小容器容积 B 再充入SO2 C 降低温度 D 分离出SO3
(2)T1°C时,容积相等的密闭容器中分别充入NO2和SO2的混合气体4 mol,发生反应iV。NO2或SO2的平衡转化率(a)与起始充入的 关系如图1所示。
关系如图1所示。
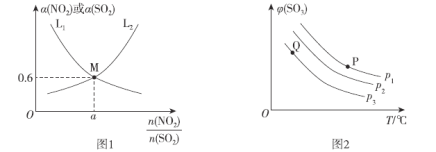
①图中能表示平衡时a(SO2)与起始充入的 关系的曲线为_____(填“L1”或“L2”)。
关系的曲线为_____(填“L1”或“L2”)。
②反应的平衡常数K=________。
(3)向密闭容器中充入一定量SO2和O2,发生反应ii。SO3的平衡体积分数(φ)与温度(T)和压强(p)的关系如图2所示。
①P1、P2 、P3由大到小的顺序为__________。
②P、Q两点对应状态下,单位体积内反应物活化分子数目:P__________Q(填“>”、“<”或“=”)。
-
二氧化硫催化氧化反应(接触法制硫酸):2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
△H=-196kJ·mol-1 有关叙述错误的是( )
A.一定温度下,增大压强,转化率增大,平衡常数不变
B.2molSO2和1molO2反应放出热量小于196kJ
C.反应物键能之和小于生成物键能之和
D.焓变△H和熵变△S都有利于反应正向进行
-
根据以下事实,回答下列问题
(1)工业接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g)⇌2SO3(g)△H=-190kJ•mol-1该热化学反应方程式的意义是______.
(2)在25℃、101kPa下,1g甲醇[CH3OH(l)]燃烧生成CO2和液态水时放热.22.68kJ.则表示甲醇燃烧热的热化学方程式为______.
(3)已知25℃、l01kPa时下列反应的热化学方程式为:
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H=-870.3kJ/mol
②C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
③H2(g)+ O2(g)=H2O(l)△H=-285.8kJ/mol,则C(s)与H2(g)、O2(g)反应生成CH3COOH(l)在该条件下的热化学方程式为______.
O2(g)=H2O(l)△H=-285.8kJ/mol,则C(s)与H2(g)、O2(g)反应生成CH3COOH(l)在该条件下的热化学方程式为______.
(4)由N2和H2合成1molNH3时可放出46.2kJ的热量.从手册上查出N≡N键的键能是948.9kJ/mol,H-H键的键能是436.0kJ/mol,则N-H键的键能是______.
-
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。T℃时反应
2SO2(g)+O2(g) 2SO3(g)过程中的能量变化如图所示,回答下列问题。
2SO3(g)过程中的能量变化如图所示,回答下列问题。
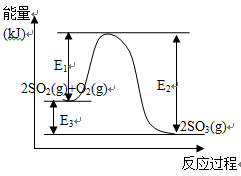
(1)T℃时将3molSO2和1molO2通入体积为2L的恒温恒容密闭容器中,发生反应。2min时反应达到平衡,此时测得反应物O2还剩余0.1mol,则达到平衡时SO2的转化率为_______,反应放出_____________热量。(用E1、E2或E3表示)
(2)下列叙述能证明该反应已达化学平衡状态的是__________________(填序号)
①SO2的体积分数不再发生变化 ②容器内压强不再发生变化 ③容器内气体原子总数不再发生变化 ④相同时间内消耗2n molSO2的同时生成n molO2 ⑤相同时间内消耗2n molSO2的同时生成2n molSO3
(3)在反应体系中加入催化剂,反应速率增大, E3的变化是: E3 ____________(填“增大”“减小”或“不变”)
(4)若以下图所示装置,用电化学原理生产硫酸,将SO2、O2以一定压强喷到活性电极上反应。写出通SO2电极的电极反应式:______________________________________________。

(5) SOCl2是一种无色液体,可与碳共同构成锂电池的正极材料,且其放电时也有SO2气体产生。写出SOCl2在电池中放电时的电极反应式_________________。
2SO3(g);△H=-196.6kJ/mol





