-
氮、磷、砷(As)等VA族元素的化合物在研究和生产中有许多重要用途。
(1)写出基态As原子的核外电子排布式___________________。
(2)NH3、PH3、AsH3熔沸点由高到低的顺序为______。
(3)水合肼(N2H4·H2O)又名水合联氨,是一种重要的化工试剂。利用尿素法生产水合肼的原理为:CO(NH2)2+ 2NaOH+NaClO=Na2CO3+N2H4·H2O+NaCL,该反应中所涉及的第二周期元素第一电离能大小顺序是________。晶体N2H4·H2O中各种微粒间的作用力不涉及__(填字母)。
a:离子键 b.共价键 c.金属键 d.氢键 e.范德华力
(4)NO3-的VSEPR模型是____,H3AsO3分子中As的杂化方式为____。
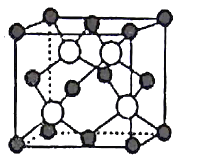
(5)GaAs以第三代半导体著称,性能比硅更优良,广泛用于电子计算机、人造卫星等尖端技术。它的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。GaAs为___ 晶体,晶胞结构与NaCl晶胞____(填“相同”或“不同”)。Ga和As的摩尔质量分别为MGag·mol-l和MAsg·mol-l,原子半径分别为rGapm和rAspm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为___ 。
-
“张亭栋研究小组”受民间中医启发,发现As2O3对白血病有明显的治疗作用。氮(N)、磷(P)、砷(As)为第VA族元素,该族元素的化合物在研究和生产中有着许多重要用途。
(1)N原子的价电子排布式为______,N、P、As原子的第一电离能由大到小的顺序为______。
(2)NH3的沸点比AsH3的沸点高,原因是____________。
(3)立方氮化硼晶体(BN),是一种超硬材料,有优异的耐磨性,其晶胞如图所示。
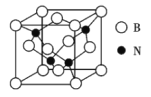
①立方氮化硼是_________晶体,晶体中N原子的杂化轨道类型为_________,A,B原子的配位数为_________。
②立方氮化硼晶体中“一般共价键”与配位键的数目之比为_________。
(4)若立方氮化硼晶胞的边长为362 pm,则立方氮化硼的密度为_________g/cm3(只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA)。
-
氮(N)、磷(P)、砷(As)等都是VA族元素,该族元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)As原子的价电子排布式为____________。
(2)P和S是同一周期的两种元素,P的第一电离能比S大,原因是________________。
(3)NH4+中H—N—H的键角比NH3分子中的键角________(填“大”或“小”),原因是____________。
(4)NaAsO4中含有的化学键类型包括__________;AsO43-的空间构型为_____________;As4O6的分子结构如下图所示,则在该化合物中As原子的杂化方式是____________。

(5)2017年1月27日,我国科学家在《Science》杂质上发表论文,在全氮阴离子盐合成上取得重大进展,首次制得试问下稳定,含有N5-离子的盐(具有超高能量密度的化合物),N5-离子中氮元素的平均化合价为_____。
(6)白磷(P)的晶体属于分子晶体,其晶胞结构如下图(小圆圈表示白磷分子)。该晶胞中含有的P原子数为_______;已知该晶胞的边长为a cm,阿伏加德罗常数为NAmol-1,则该晶体的密度为_____g·cm-3(用含有NA的式子表示)

-
我国科学家受中医启发,发现As2O3(俗称砒霜)对白血病有疗效。氮、磷、砷(As)是VA族、第二至第四周期的元素,这些元素的化合物在研究和生产中有许多重要用途。
完成下列填空:
(1)As原子最外层电子的轨道表示式为_____________;砷蒸气的分子式:As4,其分子结构与白磷(P4)相似,也是正四面体,则As4中砷砷键的键角是__________。
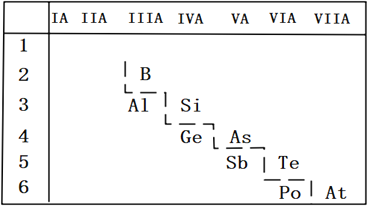
(2)P的非金属性比As强,从原子结构的角度解释其原因_______;如图是元素周期表的一部分,请推测砷的单质或其化合物可能具有的性质_______________(写出两条即可)
(3)NH4NO3可做化肥,但易爆,300℃发生爆炸:2NH4NO3→2N2↑+O2↑+4H2O。每生成2molN2,反应中转移的电子为_____mol,氧化产物与还原产物的质量之比为_____。
(4)发电厂常用氨气吸收烟气中的CO2。常温下,当CO2不断通入pH=11的氨水中时会产生微量的新离子:NH2COO-。
(i)写出NH2COO-的电子式___________。
(ii)计算原氨水中c(NH4+)=_______mol/L。
-
[化学—选修3:物质结构与性质]第ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含第ⅤA族元素的化合物在研究和生产中有许多重要用途。
(1)砷元素的基态原子价电子排布图为___________________。
(2)氮元素的单质除了N2外,还有N4,则N4中的N原子的轨道杂化方式为________________。
(3)对氨基苯甲醛与邻氨基苯甲醛相比,沸点较高的是_________(填空“前者”或“后者”),原因是_____________。
(4)汽车安全气囊的产生药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质,在NaN3固体中,阴离子的立体构型为_____________。
(5)王水溶解黄金的反应如下:Au+HNO3+4HCl=H[AuCl4]+NO+2H2O,产物中的H[AuCl4]是配合物,它的配位体是____________。
(6)砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是变通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措.已知砷化镓的晶胞结构如图,晶胞参数α=565pm。
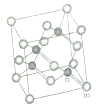
①砷化镓的化学式_________________,镓原子的配位数为________。
②砷化镓的晶胞密度=_____________g/cm3(列式并计算),m位置Ga原子与n位置As原子之间的距离为_________pm(列式表示)。
-
第ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含第ⅤA族元素的化合物在研究和生产中有许多重要用途。
(1)砷元素的基态原子价电子排布图为______________。
(2)科学家发现氮元素的单质除了N2外,还有N4,则N4中的N原子的轨道杂化方式为______________。
(3)汽车安全气囊的产生药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质,在NaN3固体中阴离子的立体构型______________。
(4)王水溶解黄金的反应如下:Au+HNO3+4HCl=H[AuCl4]+NO↑+2H2O,产物中的H[AuCl4]是配合物,它的配位体是______________。
(5)砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是变通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明是节能减排的有效举措,已知砷化镓的晶胞结构如图,晶胞棱长为apm。

①砷化镓的化学式______________,镓原子的配位数为______________。
②砷化镓的晶胞中m位置Ga原子与n位置As原子之间的距离为________pm (用含“a”的表达式表示)
-
含第VA族的磷、砷(As)等元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)基态P原子的核外电子排布式为____,有____个未成对电子。
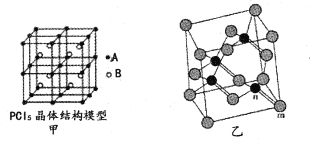
(2)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图甲所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CC14、SF6互为等电子体,则A为____,其中心原子杂化轨道类型为____,B为____。
(3)PO43-的空间构型为____,其等电子体有____(请写出一种)。
(4)砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。已知砷化镓的晶胞结构如图乙,晶胞参数a= 565pm。

①砷化镓的化学式为____,镓原子的配位数为____。
②砷化镓的晶胞密度=____g/cm3(列式并计算,精确到小数点后两位),m位置Ga原子与n位置As原子之间的距离为____pm(列式表示)。
-
含第VA族的磷、砷(As)等元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)基态P原子的核外电子排布式为____,有____个未成对电子。
(2)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图甲所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CC14、SF6互为等电子体,则A为____,其中心原子杂化轨道类型为____,B为____。
(3)PO43-的空间构型为____,其等电子体有____(请写出一种)。
(4)砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。已知砷化镓的晶胞结构如图乙,晶胞参数a= 565pm。
①砷化镓的化学式为____,镓原子的配位数为____。
②砷化镓的晶胞密度=____g/cm3(列式并计算,精确到小数点后两位),m位置Ga原子与n位置As原子之间的距离为____pm(列式表示)。
-
氮(N)、磷(P)、砷(As)等都是ⅤA族的元素,该族元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)化合物N2H4的电子式为___________________。
(2)As原子的核外电子排布式为_______________________。
(3)P和S是同一周期的两种元素,P的第一电离能比S大,原因是_______________。
(4)NH4+中H-N-H的健角比NH3中H-N-H的键角大,原因是_________________。
(5)Na3AsO4中含有的化学键类型包括________;AsO43-空间构型为________,As4O6的分子结构如图所示,则在该化合物中As的杂化方式是________________。

(6)白磷(P4)的晶体属于分子晶体,其晶胞结构如图(小圆圈表示白磷分子)。己知晶胞的边长为acm,阿伏加德罗常数为NAmol-1,则该晶胞中含有的P原子的个数为_________,该晶体的密度为_______g·cm-3(用含NA、a的式子表示)。

-
VA族的氮、磷、砷(As)等元素的化合物在科研和生产中有许多重要用途,请回答下列问题。
(1)砷的基态原子的电子排布式为 。
(2)N、P、As原子的第一电离能由大到小的顺序为 。
(3)NH3的沸点比PH3高,原因是 ;PO43-离子的立体构型为 。
(4)PH3分子中P原子采用 杂化。
(5)H3AsO4和H3AsO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3 酸性强的原因 。
(6)CuCl2与氨水反应可形成配合物[Cu(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。










