-
肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池等方面,NO2的二聚体N2O4是火箭中常用的氧化剂。请回答下列问题:
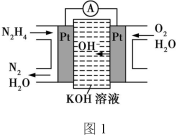
(1)肼燃料电池的原理如图1所示,左边电极上发生反应的电极反应式为 。
(2)火箭常用N2O4作氧化剂,肼作燃料,已知:
① N2(g)+2O2(g) 2NO2(g) ΔH1=−67.7 kJ·mol−1;
2NO2(g) ΔH1=−67.7 kJ·mol−1;
② N2H4(g)+O2(g) N2(g)+2H2O(g) ΔH2=−534.0 kJ·mol−1;
N2(g)+2H2O(g) ΔH2=−534.0 kJ·mol−1;
③2NO2(g) N2O4(g) ΔH3=−52.7 kJ·mol−1。
N2O4(g) ΔH3=−52.7 kJ·mol−1。
气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式为 。
(3)联氨在工业生产中常以氨和次氯酸钠为原料获得,也可在高锰酸钾作催化剂条件下,用尿素[CO(NH2)2]和次氯酸钠、氢氧化钠溶液反应获得,尿素法反应的离子方程式为 。
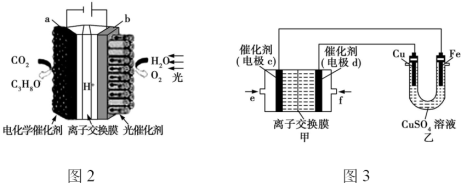
(4)某模拟“人工树叶”的电化学实验装置如图2所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。该装置工作时,H+从 (填字母,后同)极区向 极区迁移,将电能转化为 能,每生成1 mol O2,有 g CO2被还原(小数点后保留1位数字)。
(5)图3中甲装置为C3H8O的燃料电池(电解质溶液为KOH溶液)装置,该同学想在乙装置中实现铁上镀铜,则f处通 ,写出电极c上的电极反应式: 。
-
( N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池, NO2 的二聚体 N2O4 则是火箭中常用氧化剂。试回答下列问题
(1)肼的结构式为____________。
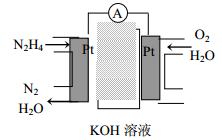
(2)肼燃料电池原理如图所示,左边电极上发生的电极反应式为_________________。
(3)火箭常用 N2O4 作氧化剂,肼作燃料,已知:
N2(g)+2O2(g)=2NO2(g) △H=-67.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534.0kJ·mol-1
2NO2(g)  N2O4(g) △H=-52.7kJ·mol-1
N2O4(g) △H=-52.7kJ·mol-1
写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:_________________。
(4)联氨的工业生产常用氨和次氯酸钠为原料获得,也可在催化剂作用下,用尿素[CO(NH2)2]和次氯酸钠与氢氧化钠的混合溶液反应获得,尿素法反应的离子方程式为_________________。
-
肼(N2H4)又称联氨,广泛用于火箭推进剂、有机合成及燃料电池,NO2的二聚体N2O4则是火箭中常用的氧化剂,请回答下列问题:
(1)肼燃料电池原理如图所示,左边电极上发生反应的电极反应式为________
(2)火箭常用N2O4作氧化剂,肼作燃料,已知:
①N2(g)+2O2(g)═2NO2(g)△H=-67.7kJ/mol
②N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.0kJ/mol
③2NO2(g⇌N2O4(g)△H=-52.7kJ/mol
试写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:________
(3)联氨的工业生产常用氨和次氯酸钠为原料获得,也可在高锰酸钾催化下,用尿素[CO(NH2)2]和次氯酸钠一氢氧化钠溶液反应获得,尿素法反应的离子方程式为________.
-
肼(N2H4)又称联氨,广泛用于火箭推进剂、化工原料及燃料电池等方面。请回答下列问题:
(1)肼是火箭的高能燃料,该物质燃烧时生成水蒸气和氮气,已知某些化学键能如下:
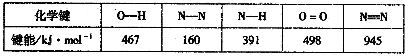
①N2H4中氮元素的化合价为__________。
②气态N2H4在氧气中燃烧的热化学方程式为__________。
(2)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液,该反应的离子方程式为__________。
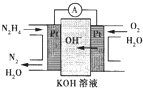
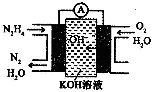
(3)肼燃料电池原理如图所示,左边电极上发生反应的电极反应式为__________.
(4)盐酸肼(N2H6Cl2)是一种化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4 Cl类似,但分步水解。
①写出盐酸肼第一步水解的离子方程式__________。
②盐酸肼水溶液中离子浓度的关系为__________ (填序号)。
A.c(Cl-)>c([N2H5·H2O+])> c(H+)>c(OH-)
B.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
C.c(N2H62+)+ c([N2H5·H2O+]) +c(H+)= c(Cl-)+c(OH-)
(5〕常温下,将0.2 mol/L盐酸与0.2 mol/L肼的溶液等体积混合(忽略混合后溶液体积变化〕。若测定混合液的pH=6,混合液中水电离出的H+与0.1mol/L盐酸中水电离出的H+浓度之比为__________。
-
肼(N2H4)与N2O4是火箭发射中最常用的燃料与助燃剂,回答下列问题:
(1)T℃时,将一定量的NO2或N2O4充入一个容积为2L的恒容密闭容器中,发生反应2NO2(g) N2O4(g),保持温度不变,各物质的浓度随时间变化关系如下表:
N2O4(g),保持温度不变,各物质的浓度随时间变化关系如下表:
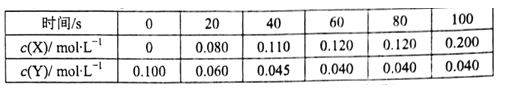
①c(Y)代表___________(填化学式)的浓度,20~40s内,用NO2表示的化学反应速率为___________。
②该反应的平衡常数K=___________。
③60s时容器内混合气体的密度为_____g·L-1。
④100s时改变的条件是___________,重新达到平衡时,与原平衡比较,NO2的体积分数将___________(填“增大”“减小”或“不变”)。
(2)①已知2N2H4(g)+N2O4(g) 3N2(g)+4H2O(g) △H=-QkJ·mol-1,相关化学键的键能如表所示。
3N2(g)+4H2O(g) △H=-QkJ·mol-1,相关化学键的键能如表所示。
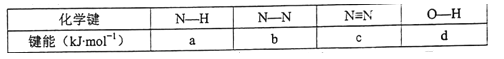
使 1molN2O4(g)完全分解成相应的原子时需要吸收的能量是___________kJ(用代数式表示)
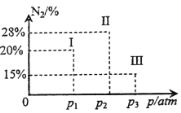
②相同温度下,向Ⅰ、Ⅱ、Ⅲ三个恒压密闭容器中均充入1molN2H4(g)和1molN2O4(g),三个容器的反应压强分别为p1、p2、p3。在其它条件相同的情况下,反应进行到tmin时,N2的体积分数如图所示,此时容器I___________(填“处于”或“不处于”)化学平衡状态,原因是___________。
-
(10分)发射航天火箭常用氮的氢化物肼(N2H4)作燃料。试回答下列有关问题:
(1)N2H4燃烧时用NO2作氧化剂,它们相互反应生成氮气和水蒸气。

则N2H4和NO2反应生成氮气和水蒸气的热化学方程式为________。
(2)利用肼、氧气与KOH溶液组成碱性燃料电池,氮元素被氧化后只生成氮气,请写出该电池工作时负极的电极反应________;电池工作时,________极pH升高。
(3)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液。该反应的化学方程式________。
(4)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。写出盐酸肼第一步水解反应的离子方程式________。
-
工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等。
(1)火箭常用N2H4作燃料,N2O4作氧化剂。已知:
N2(g) + 2O2(g) =2NO2(g) △H = +67.7 kJ·mol-1
N2H4(g) + O2(g) =N2(g) + 2H2O(g) △H = -534.0 kJ·mol-1
NO2(g)  1/2N2O4(g) △H = -26.35 kJ·mol-1
1/2N2O4(g) △H = -26.35 kJ·mol-1
试写出气态联氨在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:
。
 (2)联氨——空气燃料电池是一种碱性燃料电池,电
(2)联氨——空气燃料电池是一种碱性燃料电池,电
解质溶液是20%~30%的氢氧化钾溶液。该电
池放电时,正极的电极反应式为 。
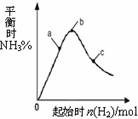
(3)在300℃时,改变起始反应物中氢气的物质的量
对反应N2(g) + 3H2(g)  2NH3(g) △H<0
2NH3(g) △H<0
的影响如右图所示。
①请在图中画出400℃时对应的图像。
②在a、b、c三点中,H2 的转化率最高的是 (填字母)。
-
(13分)近年来我国的航天事业取得了巨大的成就,在航天发射时,常用肼(N2H4)及其衍生物作火箭推进剂。
(1)液态肼作火箭燃料时,与液态N2O4混合发生氧化还原反应,已知每克肼充分反应后生成氮气和气态水放出热量为a KJ,试写出该反应的热化学方程式 ;
(2)在实验室中,用N2H4·H2O与NaOH颗粒一起蒸馏,收集114~116℃的馏分即为无水肼。在蒸馏过程中需要的仪器有酒精灯、锥形瓶、冷凝管、牛角管(接液管)、蒸馏烧瓶,除上述必需的仪器外,还缺少的玻璃仪器是 ;
(3)肼能使锅炉内壁的铁锈(主要成分Fe2O3)变成磁性氧化铁(Fe3O4)层,可减缓锅炉锈蚀。若反应过程中肼转化为氮气,则每生成1molFe3O4,需要消耗肼的质量为 g。
(4)磁性氧化铁(Fe3O4)的组成可写成FeO·Fe2O3。某化学实验小组通过实验来探究一黑色粉末是否由Fe3O4、CuO组成(不含有其它黑色物质)。探究过程如下:
提出假设:假设1. 黑色粉末是CuO; 假设2. 黑色粉末是Fe3O4;
假设3. 。
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂。
①若溶液显蓝色,则假设1成立。
②若所得溶液显血红色,则假设 成立。
③为进一步探究,继续向②所得溶液加入足量铁粉,若有红色固体析出的现象,则假设3成立。
有另一小组同学提出,若混合物中CuO含量较少,可能加入铁粉后实验现象不明显。
查阅资料:Cu2+与足量氨水反应生成深蓝色溶液,Cu2++4NH3·H2O=Cu(NH3)42++4H2O。
④为探究是假设2还是假设3成立,另取少量粉末加稀硫酸充分溶解后,再加入足量氨水,若假设2成立,则产生 现象;若假设3成立,则产生红褐色沉淀,同时溶液呈深蓝色。
-
肼(N2H4)又称联氨,是一种可燃性液体,与氧气或氮氧化物反应均可生成氮气和水,用作火箭燃料.
(1)写出肼与一氧化氮反应的化学方程式______.
(2)肼--空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液.该电池放电时,电极反应式:负极______.
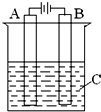
(3)如图是一个电化学装置示意图.用肼--空气燃料电池做此装置的电源.
①如果A为含有铁、银、金、碳等杂质的粗铜,B为纯铜,C为CuSO4溶液.通电一段时间后,______极的质量增大.(填“阴极”、“阳极”).
②如果A是铂电极,B是石墨电极,C是CuSO4溶液,阳极的电极反应式是______.若产生1mol气体则消耗肼为______g.
-
肼(N2H4)是一种可用于火箭或原电池的燃料。已知:
N2(g) + 2O2(g) =2 NO2(g) ΔH = +67.7kJ/mol ①
N2H4(g) + O2(g) = N2(g) + 2H2O(g) ΔH = -534 kJ/mol ②
下列说法正确的是
A.反应①中反应物所具有的总能量大于生成物所具有的总能量
B.2N2H4(g) + 2NO2(g) = 3N2(g)+ 4H2O (g) ΔH = -1000.3kJ/mol
C.铂做电极,KOH溶液做电解质溶液,由反应②设计的燃料电池其负极反应式:N2H4-4e-+4OH-=N2+4H2O
D.铂做电极,KOH溶液做电解质溶液,由反应②设计的燃料,工作一段时间后,KOH溶液的pH将增大










 (2)联氨——空气燃料电池是一种碱性燃料电池,电
(2)联氨——空气燃料电池是一种碱性燃料电池,电