-
硫的多种化合物在工业中有重要应用。
(1)Na2S2可以做制革工业中原皮的脱毛剂,写出Na2S2的电子式______________。
(2)连二亚硫酸钠(Na2S2O4)又称保险粉,可作木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性。
①Na2S2O4中S元素的化合价为_____________
②将甲酸(HCOOH)和NaOH溶液混合,再通入SO2气体,会得到保险粉,此时甲酸被氧化为CO2,该反应的化学方程式为_________________。
③Na2SO4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为1:2时,反应的化学方程式为____________。
(3)铬会造成环境污染,某酸性废水中含有Cr2O72-,处理时可用焦亚硫酸钠(Na2S2O5)将Cr2O72-转化为毒性较低的Cr3+,再调节pH至8,使铬元素沉降,分离出污泥后测得废水中Cr3+浓度为0.52mg/L,达到排放标准。
①写出Na2SO5参加反应的离子方程式_______________________。
②处理后的废水中Cr3+的物质的量浓度为____________________。
(4)氢硫酸和亚硫酸是两种弱酸,回答下列问题
①0.1mol/L H2SO4与0.2mol/L H2S溶液等体积混合,所得溶液中S2-浓度为_____mol/L。(已知氢硫酸Ka1=1.0×10-8、Ka2=1.0×10-15,忽略H2S和H2O电离产生的H+)
②已知亚硫酸的Ka1=1.0×10-2、Ka2=6.0×10-13,设计实验证明亚硫酸第一步不完全电离。(可用实验用品:0.1mol/L亚硫酸、0.1mol/L NaHSO3溶液、0.1mol/L Na2SO3溶液,广泛pH试纸、pH计)
操作简述
______________
现象或数据
______________
结论
H2SO3第一步不完全电离
高三化学填空题中等难度题查看答案及解析
-
Na与S反应可以生成多种产物:Na2S,Na2S2……Na2S5。已知Na2S2的电子式为
则S32-的电子式为________。已知Na2S3+2HCl = 2NaCl+H2S↑+2S↓,试写出Na2S5与醋酸反应的离子方程式:________。工业上常用电解熔融NaCl制Na,事实上电解许多熔融的钠的化合物也能制备Na,如NaOH、Na2CO3。试写出电解熔融NaOH的反应方程式:________,若电解熔融Na2CO3时有CO2气体产生,则阳极电极反应式为________。
高三化学填空题中等难度题查看答案及解析
-
烯烃中碳碳双键是重要的官能团,在不同条件下能发生多种变化。异松油烯是应用广泛的工业原料,它与水反应(摩尔比1:1)可得到γ-松油醇(结构见右图)。
(1)写出γ-松油醇的分子式_______,该物质所属的物质类别为_______(填编号);
a.烯烃 b.环烃 c.醇
(2)下列反应中,γ-松油醇不能发生是___________(填编号);
a.与HCl发生取代反应 b.与HCl发生加成反应
c.在灼热铜丝催化下发生氧化反应 d.聚合反应
(3)已知异松油烯分子中有3个甲基,则其结构简式为__________________;
(4)异松油烯的同分异构体中,能与溴水发生1,4 –加成的共有_____种(仅考虑官能团位置异构),写出其中一种的结构简式________;
高三化学填空题困难题查看答案及解析
-
NH3在工业生产上有重要的应用
(1)写出用浓氨水检验氯气管道泄漏的化学反应方程式
(2)若将少量氨气与过量氯气混合,则生成一种酸和另一种化合物A,A中所有原子均满足8电子稳定结构,试写出A的电子式 ;A在一定条件下能与水反应,可用于饮用水的消毒,试写出此反应的化学反应方程式 .
高三化学填空题中等难度题查看答案及解析
-
硅是重要的半导体材料,是构成现代电子工业的基础。硅及其化合物在工业中应用广泛,在工业上,高纯硅可以通过下列流程制取:

完成下列填空:
(1)氯原子核外有_______种不同能量的电子,硅原子的核外电子排布式是_______________。
(2)碳与硅属于同主族元素,熔沸点SiO2 ________CO2 (填写“>”、“<”或“=”),其原因是_____________________________________________________。
(3)流程中由SiO2制粗硅的反应不能说明碳的非金属性强于硅,原因是_________________;请写出一个能说明碳的非金属性强于硅的化学方程式______________________________。
(4)SiHCl3(g) + H2(g)
Si(s) + 3HCl(g) -Q (Q>0)
①上述反应的平衡常数表达式K=_____________;能使K增大的措施是_______________。
②一定条件下,在固定容积的密闭容器中,能表示上述反应达到平衡状态的是________(选填编号)。
a.3v逆(SiHCl3)=v正(HCl) b.混合气体的压强不变
c.K保持不变 d.c(SiHCl3)∶c(H2)∶c(HCl)=1∶1∶3
③一定温度下,在2L密闭容器中进行上述反应,5min后达到平衡,此过程中固体质量增加0.28g,此时HCl的化学反应速率为 ________________ 。
高三化学综合题中等难度题查看答案及解析
-
(18分)I.NH3在工业生产上有重要的应用
(1)写出用浓氨水检验氯气管道泄漏的化学反应方程式
(2)若将少量氨气与过量氯气混合,则生成一种酸和另一种化合物A,A中所有原子均满足8电子稳定结构,试写出A的电子式 ;A在一定条件下能与水反应,可用于饮用水的消毒,试写出此反应的化学反应方程式
II.某白色固体甲常用于织物的漂白,也能将污水中的某些重金属离子还原为单质除去。为研究其组成,某小组同学进行了如下实验。
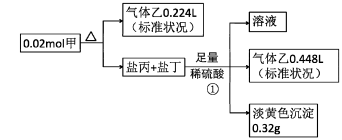
又知,甲的焰色为黄色,盐丙和丁的组成元素和甲相同,乙能使品红溶液褪色,①处气体体积在充分加热挥发后经干燥测定
(1)甲中所含阳离子的结构示意图 ,甲的化学式
(2)写出①中产生黄色沉淀的反应的离子反应方程式
(3)乙能使品红溶液褪色的原因是
(4)甲的溶液还可用作分析化学中的吸氧剂,假设其溶液与少量氧气反应产生等物质的量的两种酸式盐,试写出该反应的化学反应方程式
(5)下列物质中可能在溶液中与甲反应的是
A.NaI B.Cl2 C.AgNO3 D.NaOH
高三化学推断题困难题查看答案及解析
-
多硫化钠(Na2SX)在制革工业中常用作皮毛的脱毛剂,农业上可作杀虫剂,也是分析化学中的常用试剂。在碱性溶液中,Na2SX与NaBrO3发生反应生成Na2SO4与NaBr。
(1)、上述反应中发生氧化反应的物质是________,被还原的元素是________(填写元素符号或化学式)。
(2)、若Na2SX与NaBrO3反应的物质的量之比为3:10,则x = ________。
(3)、NaBrO3也可以在酸性条件下与NaBr反应生成Br2。若生成6mol Br2,则反应中转移电子的物质的量为________。
(4)、根据上述两个反应,可推知Na2SX、 Br2、NaBr还原性由强到弱的顺序是________(填写化学式)。
高三化学填空题简单题查看答案及解析
-
硫的化合物在科研、生活及化学工业中具有重要的应用。
(1)在废水处理领域中,H2S或Na2S能使某些金属离子生成极难溶的硫化物而除去。25℃,在0.10 mol•L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如下表(忽略溶液体积的变化、H2S的挥发)。
pH
3
5
7
9
11
c(S2-)/ mol•L-1
1.4×10-15
1.4×10-11
6.8×10-8
1.3×10-5
1.3×10-3
某溶液含0.020 mol•L-1Mn2+、0.1 mol•L-1H2S,当溶液的pH=5时,Mn2+开始沉淀,则MnS的溶度积=________________。
(2)工业上采用高温分解H2S制取氢气,其反应为2H2S(g)
2H2(g)+S2(g) △H1,在膜反应器中分离出H2。
①已知:H2S(g)
H2(g)+S(g) △H2,2S(g)
S2(g)△H3。则△H1=_______(用含△H2、△H3的式子表示。
②在密闭容器中,充入0.10molH2S(g),发生反应2H2S(g)
2H2(g)+S2(g),控制不同的温度和压强进行实验。结果如图所示。

图中压强p1、p2、p3由大到小的顺序为_______________,理由是_________________。若容器的容积为2.0L,则压强为p3,温度为950℃时,反应经3h达到平衡,则达到平衡时v(S2)=__________;若压强p2=7.2MPa,温度为975℃时,该反应的平衡常数Kp=_____________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),若保持压强不变,升温到1000℃时,则该反应的平衡常数___________(填“增大”“不变”或“减小”)。
(3)工业上用惰性电极电解KHSO4饱和溶液制取H2O2,示意图如图所示:
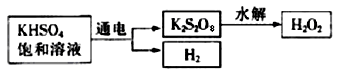
①低温电解饱和KHSO4溶液时阳极的电极反应式为_________________。
②K2S2O8水解时生成H2O2和KHSO4,该反应的化学方程式为_________________。
高三化学填空题困难题查看答案及解析
-
铬及其化合物在现代工业上的应用广泛,可用于电镀,鞣制羊毛,皮革;铬还用于照相材料,胶版印刷及化工触媒剂等。但化工废料铬渣对人体健康有很大危害。
Ⅰ:某工厂对制革工业污泥中Cr(III)回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):
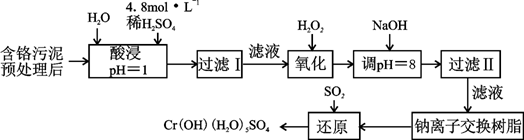
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
阳离子
Fe3+
Fe2+
Mg2+
Al3+
Cu2+
Cr3+
开始沉淀时的pH
1.9
7.0
——
——
4.7
——
沉淀完全时的pH
3.2
9.0
11.1
8
6.7
9 (>9溶解)
(1)实验室用18.4 mol·L-1的浓硫酸配制250 mL 4.8 mol·L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需 ________。
(2)酸浸时,为了提高浸取率可采取的措施是________(至少答一点)。
(3)调节溶液的pH=8是为了除去离子。钠离子交换树脂的原理为:
Mn++nNaR→MRn+nNa+,被交换的的杂质离子是________。
(4)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)
Cr3+(aq)+3OH-(aq)
常温下,Cr(OH)
的溶度积Ksp= c(Cr3+)• c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至________。
(5)还原过程发生以下反应(请配平):________Na2Cr2O7+________ SO2+________ ________
=________ Cr(OH) (H2O)5SO4+________Na2SO4;
Ⅱ:工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理。
其中一种处理方法为电解法:该法用Fe做电极,电解含Cr2O72-的酸性废水,随着电解进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀。用Fe做电极的原因为
________
在阴极附近溶液pH升高的原因是(用电极反应解释)________。
高三化学填空题中等难度题查看答案及解析
-
Na2S溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构和化学性质相似的物质Na2S2,其溶液显黄色.
(1)该反应中的Na2S表现了______性,当生成1mol Na2S2时,转移电子数目为______.
(2)完成该反应的化学方程式:______.
(3)Na2S2的溶液与稀硫酸反应产生的现象为______.
(4)在碱性溶液中,多硫化钠Na2Sx(x≥2),可被NaClO氧化为硫酸钠,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1:16,则x的值为______.
A.5 B.4 C.3 D.2.高三化学解答题中等难度题查看答案及解析