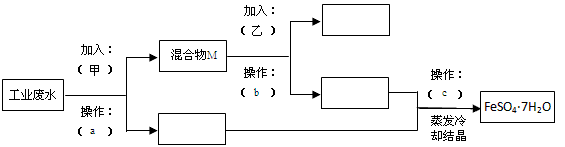-
Ⅰ.某工厂的工业废水中含有大量的FeSO4 和较多的Fe3+和Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。实验室模拟该工业流程如图:
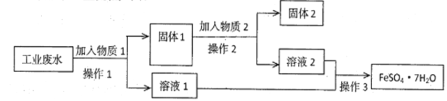
(1)检验废水中的Fe2+,实验室中用酸性KMnO4溶液检验,发生反应的离子方程式为________。
(2)加入过量物质1后,发生反应的离子方程式为___________________________。
(3)固体2是__________,实验室为长期保存硫酸亚铁溶液往往向其溶液中加入__________。
Ⅱ.工业上冶炼铝的原料是铝土矿( 主要成分是Al2O3,杂质为Fe2O3、FeO、SiO2等)。某研究小组设计的提纯Al2O3的方案如下:

(1)加入过量的NaOH溶液,过滤后的滤液中含有的溶质有________(填化学式)。
(2)加入过量NaOH溶液过滤后,若滤渣中Fe(OH)2也被氧化,写出其被氧化的化学方程式______________。
(3)写出通入过量CO2生成沉淀A时反应的离子方程式为_________________________。
-
Ⅰ.某工厂的工业废水中含有大量的FeSO4 和较多的Fe3+和Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。实验室模拟该工业流程如图:
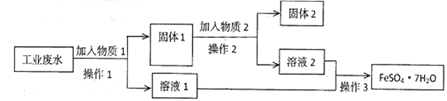
(1)检验废水中的Fe2+,实验室中用酸性KMnO4溶液检验,发生反应的离子方程式为________________________。
(2)加入过量物质1后,发生反应的离子方程式为___________________________。
(3)固体2是_____________________,实验室为长期保存硫酸亚铁溶液往往向其溶液中加入_______________________。
Ⅱ.工业上冶炼铝的原料是铝土矿( 主要成分是Al2O3,杂质为Fe2O3、FeO、SiO2等)。某研究小组设计的提纯Al2O3的方案如下:

(1)加入过量的NaOH 溶液,过滤后的滤液中含有的溶质有________ (填化学式)。
(2)加入过量NaOH溶液过滤后,若滤渣中Fe(OH)2也被氧化,写出其被氧化的化学方程式__________________________。
(3)写出通入过量CO2生成沉淀A时反应的离子方程式为_________________________。
-
Ⅰ.某工厂的工业废水中含有大量的FeSO4 和较多的Fe3+和Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。实验室模拟该工业流程如图:
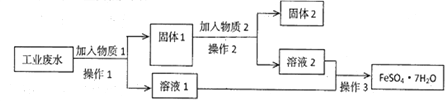
(1)检验废水中的Fe2+,实验室中用酸性KMnO4溶液检验,发生反应的离子方程式为________________________。
(2)加入过量物质1后,发生反应的离子方程式为___________________________。
(3)固体2是_____________________,实验室为长期保存硫酸亚铁溶液往往向其溶液中加入_______________________。
Ⅱ.工业上冶炼铝的原料是铝土矿( 主要成分是Al2O3,杂质为Fe2O3、FeO、SiO2等)。某研究小组设计的提纯Al2O3的方案如下:

(1)加入过量的NaOH 溶液,过滤后的滤液中含有的溶质有________ (填化学式)。
(2)加入过量NaOH溶液过滤后,若滤渣中Fe(OH)2也被氧化,写出其被氧化的化学方程式__________________________。
(3)写出通入过量CO2生成沉淀A时反应的离子方程式为_________________________。
-
Ⅰ.某工厂的工业废水中含有大量的FeSO4 和较多的Fe3+和Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。实验室模拟该工业流程如图:
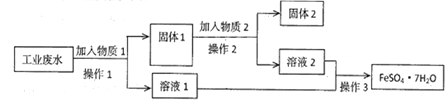
(1)检验废水中的Fe2+,实验室中用酸性KMnO4溶液检验,发生反应的离子方程式为________________________。
(2)加入过量物质1后,发生反应的离子方程式为___________________________。
(3)固体2是_____________________,实验室为长期保存硫酸亚铁溶液往往向其溶液中加入_______________________。
Ⅱ.工业上冶炼铝的原料是铝土矿( 主要成分是Al2O3,杂质为Fe2O3、FeO、SiO2等)。某研究小组设计的提纯Al2O3的方案如下:

(1)加入过量的NaOH 溶液,过滤后的滤液中含有的溶质有________ (填化学式)。
(2)加入过量NaOH溶液过滤后,若滤渣中Fe(OH)2也被氧化,写出其被氧化的化学方程式__________________________。
(3)写出通入过量CO2生成沉淀A时反应的离子方程式为_________________________。
-
某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和金属铜。请根据以下流程图,回答下列问题。
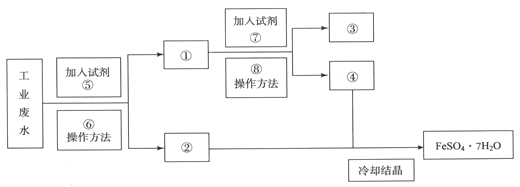
(1)写出下列标号所代表的物质的名称(注意用量)或操作方法③_____,⑥_____。
(2)鉴别溶液④中的金属阳离子时,应滴加的试剂依次是______,现象依次是_______,并写出对应反应的离子方程式:_______,______。
(3)若取2mL溶液④加入试管中,然后滴加氢氧化钠溶液,此过程涉及的氧化还原反应的化学方程式是__________。
-
某工厂的工业废水中含有大量的“FeSO4”、较多的Cu2+和少量的Na+。为了减少污染变废为宝,工厂计划从该废水中回收硫酸亚铁和铜。根据流程图,完成回收硫酸亚铁和铜的简单实验方案。回答下列问题:
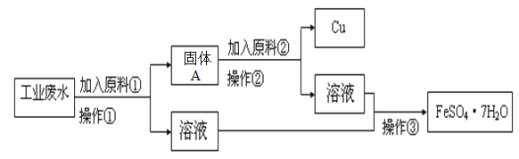
(1)加入原料①为____________;操作②为___________;
(2)固体A为____________;
(3)写出有关反应的化学方程式__________________。
-
某工厂的工业废水中含有大量的“FeSO4”、较多的Cu2+和少量的Na+。为了减少污染变废为宝,工厂计划从该废水中回收硫酸亚铁和铜。根据流程图,完成回收硫酸亚铁和铜的简单实验方案。回答下列问题:
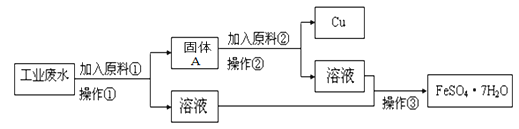
(1)加入原料①为____________;操作②的名称为___________,该操作所用到的玻璃仪器主要有______。
(2)固体A为____________;
(3)写出加入原料①和②有关反应的离子方程式__________________、________________________。
(4)操作③获得FeSO4·7H2O,需要经过_____、_____、过滤等操作。
-
某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,工厂计划从废水中回收硫酸亚铁和金属铜。请根据流程图回答下列问题,完成回收的简单实验方案。
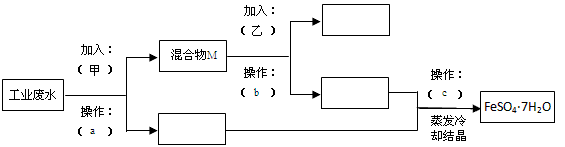
(1)操作a的名称为__________。
(2)加入的甲、乙物质分别为________、_________。
A.浓H2SO4 B.稀H2SO4 C.Fe粉 D.稀HCl
(3)操作c过程中用到的仪器是_______________。
A.坩埚 B.蒸发皿 C.玻璃棒 D.酒精灯
(4)Fe2+具有较强的还原性,易变质,检验产品FeSO4∙7H2O变质的方法是_____________________。
(5)为方便处理废液,检测人员取废水样10mL,做相应如图流程处理。加入加入甲物质质量为4.2g,最终得到FeSO4∙7H2O27.8g(不考虑处理过程中的损失),则原试样中c(Fe2+)=__________。
-
某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。某工厂设计下列流程图,完成回收硫酸亚铁和铜的简单实验方案。
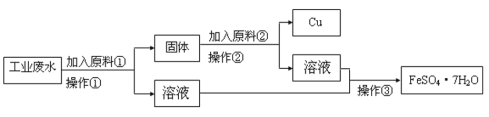
(1)操作①的名称为______,该操作所需要的玻璃仪器为______、_____、烧杯。
(2)原料②的化学式为__________,发生的离子方程式为_________________。
(3)为验证上述流程图中的溶液中含有SO42-:取少量的溶液于试管中,先加入______,再加入________,若观察到有__________,则说明溶液中含有SO42-。
-
某工厂的工业废水中含有大量的FeSO4 、较多的Cu2+ 、H+和少量的Na+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。其一种生产工艺如下:
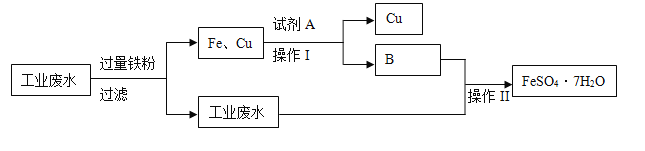
回答下列问题:
(1)写出工业废水中加入过量铁粉发生化学反应离子方程式,并用“单线桥”表示电子转
移方向和数目_________________________。
(2)试剂A化学式___________;生成物B化学式__________。
(3)操作I的名称________,操作II的名称______________。