-
下列说法正确的是
A. 由电负性数值:铍—1.5;氯—3.0可推知氯化氨中是离子键
B. 根据对角线规可知Li在空气中燃烧会生成Li3N和Li2O
C. H—O键能为QkJ/mol,则1molH2分解生成和O2需要吸收2QkJ能量
D. 稀有气体一般很难参与反应,是因为其分子内的键能很大,很难断裂
高二化学单选题中等难度题查看答案及解析
-
C、Be、Cl、Fe等元素及其化合物有重要的应用。
(1)查表得知,Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为 (填离子或共价)化合物;根据铍元素和铝元素在周期表中的位置,推测BeCl2应与 (填MgCl2或AlCl3)化学性质更相似。
(2)上述四种元素的原子中,未成对电子数最多的元素是_________________。
(3)①试根据原子核外电子排布所遵循的原理解释Fe2+具有较的强还原性,易被氧化为Fe3+的原因 。②当然Fe3+也有氧化性,在印刷行业中就用氯化铁溶液腐蚀铜板,写出离子方程式 。
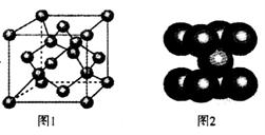
(4)一定条件下,C元素可形成多种晶体。下图1是其中某种晶体的一个晶胞,该晶胞中含有________个C原子。
(5)下图2为金属铁某种晶体的晶胞结构,已知铁的摩尔质量是56g•mol-1,该晶体的密度为a g•cm-3,NA为阿伏加德罗常数的值,则该晶胞的体积为_________cm3。
高二化学填空题困难题查看答案及解析
-
C、Be、Cl、Fe等元素及其化合物有重要的应用。
(1)查表得知,Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为 (填离子或共价)化合物;根据铍元素和铝元素在周期表中的位置,推测BeCl2应与 (填MgCl2或AlCl3)化学性质更相似。
(2)上述四种元素的原子中,未成对电子数最多的元素是_________________。
(3)①试根据原子核外电子排布所遵循的原理解释Fe2+具有较的强还原性,易被氧化为Fe3+的原因 。②当然Fe3+也有氧化性,在印刷行业中就用氯化铁溶液腐蚀铜板,写出离子方程式 。
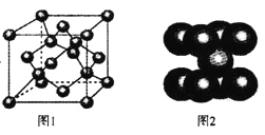
(4)一定条件下,C元素可形成多种晶体。下图1是其中某种晶体的一个晶胞,该晶胞中含有________个C原子。
(5)下图2为金属铁某种晶体的晶胞结构,已知铁的摩尔质量是56g•mol-1,该晶体的密度为a g•cm-3,NA为阿伏加德罗常数的值,则该晶胞的体积为_________cm3。
高二化学填空题困难题查看答案及解析
-
在元素周期表中的某些元素之间存在着特殊的“对角线关系”,下列有关说法不正确的是(
A.氢氧化铍是两性氢氧化物
B.B,Si的电负性数值相似
C.Li和Mg的原子半径相近,且核外电子排布相近
D.铍与盐酸或氢氧化钠溶液反应均能产生气体
高二化学单选题中等难度题查看答案及解析
-
根据表中的数据,从电负性的角度判断下列元素之间易形成共价键的一组是( )
元素
Na
Mg
Al
H
C
O
Cl
电负性
0.9
1.2
1.5
2.1
2.5
3.5
3.0
①Na和Cl ②Mg和Cl ③Al和Cl ④H和O ⑤Al和O ⑥C和Cl
A. ①②⑤ B. ③④⑥ C. ④⑤⑥ D. 全部
高二化学单选题中等难度题查看答案及解析
-
根据表中的数据,从电负性的角度判断下列元素之间易形成共价键的一组是( )
元素
Na
Mg
Al
H
C
O
Cl
电负性
0.9
1.2
1.5
2.1
2.5
3.5
3.0
①Na和Cl ②Mg和Cl ③Al和Cl ④H和O ⑤Al和O ⑥C和Cl
A. ①②⑤ B. ③④⑥ C. ④⑤⑥ D. 全部
高二化学选择题中等难度题查看答案及解析
-
某班学生对BeCl2是离子化合物还是共价化合物进行集体探究,从经验看铍是金属元素,易失去电子,氯元素易得到电子,请回答以下问题:
(1)Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为 化合物。
(2)工业上制取BeCl2方法是:将得到的BeCl2溶液在HCl气流中蒸干灼烧,防止BeCl2水解,请写出BeCl2水解的化学方程式 。
(3)经实验验证,熔融的BeCl2不能导电,说明它是 化合物;BeCl2能溶于水,水溶液能导电,因它在溶液中能电离,写出它的电离方程式 。
(4)在周期表中,铍元素和铝元素恰好处于对角线位置,根据对角线法则,判断BeCl2应与 (填MgCl2或AlCl3)化学性质更相似。
(5)0.1mol氢氧化铍恰好能和100mL0.2mol/L的氢氧化钠溶液发生反应,写出反应的化学方程式 。
高二化学填空题中等难度题查看答案及解析
-
下列说法不正确的是( )
A.根据对角线规则,推出铍的氢氧化物能与氢氧化钠溶液反应
B.根据同周期元素的电负性变化趋势,推出Mg的电负性比Al大
C.SiO44-和SO42-的空间构型相同
D.碳原子在某种情况下的最外层电子排布图可能为:
高二化学单选题中等难度题查看答案及解析
-
NA代表阿伏加德罗常数的数值,下列说法中错误的是( )
A. 完全燃烧1.5 mol乙醇和乙烯的混合物,转移电子数为18 NA
B. 7.8 g由Na2S和Na2O2组成的混合物中含有阴离子的数目为0.1 NA
C. 0.1 mol/L FeCl3溶液中Fe3+的物质的量一定小于0.1 NA
D. 常温常压下,60g甲醛和乙酸的混合物所含碳原子数为2 NA
高二化学单选题中等难度题查看答案及解析
-
下列说法不正确的是
A. 用元素分析仪来确定有机化合物的组成具有快速、微量、精确等特点
B. 根据1H核磁共振谱图可以推知有机物分子中有几种不同类型的氢原子
C. 用铜丝燃烧法可定性确定有机物中是否存在卤素
D. 通过红外光谱可以测知有机物的相对分子质量
高二化学单选题中等难度题查看答案及解析