-
在密闭容器中发生:2NO(g)+2CO(g) 2CO2+N2(g)△H=-QkJ/mol,已知:c(CO2)随温度(T)、时间(t)的变化曲线如右图所示,则:
2CO2+N2(g)△H=-QkJ/mol,已知:c(CO2)随温度(T)、时间(t)的变化曲线如右图所示,则:
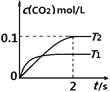
(1)T1___ T2 ,其理由是_________________
(2)在T2温度下,0~2s内的平均反应速率v(N2)=___
(3)在温度T3下,在两个体积均为1.0L的恒容密闭容器中发生该反应.
| 容器编号 | 起始物质的量 | 平衡时物质的量 |
| Ⅰ | 2.0molNO,2.0molCO | 1.0molCO2 |
| Ⅱ | 4.0molNO,4.0molCO | |
①T3时该反应的平衡常数K=___,若起始时向容器Ⅰ中充入1.0mol NO,1.5mol CO和2.0molCO2,0.5molN2,则反应向___(填“正”或“逆”)反应方向进行。
②平衡时两容器中CO的转化率:Ⅰ___Ⅱ,容器Ⅰ中反应达平衡后,若要进一步提高CO的转化率,可采取的措施为___(答一条即可)。
-
在密闭容器中通入NO和CO各2mol发生反应:2NO(g)+2CO(g) 2CO2(g)+N2(g)。容器内CO2随温度(T)、压强(P)和时间(t)的变化曲线如右图所示。以下说法合理的是
2CO2(g)+N2(g)。容器内CO2随温度(T)、压强(P)和时间(t)的变化曲线如右图所示。以下说法合理的是

A.温度T2>T1
B.压强P2>P1
C.该反应的焓变△H<0
D.T2P2曲线表示NO平衡转化率为25%
-
一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g) N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
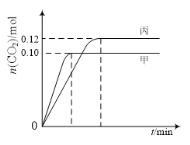
| 容器 | 温度/℃ | 起始物质的量/mol |
| NO (g) | CO (g) |
| 甲 | T1 | 0.20 | 0.20 |
| 乙 | T1 | 0.30 | 0.30 |
| 丙 | T2 | 0.20 | 0.20 |
下列说法正确的是
A. 该反应的正反应为吸热反应
B. 达到平衡时,乙中CO2的体积分数比甲中的小
C. T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)<v(逆)
D. T2℃时,若起始时向丙中充入0.06molN2和0.12 molCO2,则达平衡时N2的转化率大于40%
-
一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g) N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
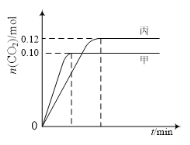
| 容器 | 温度/℃ | 起始物质的量/mol |
| NO (g) | CO (g) |
| 甲 | T1 | 0.20 | 0.20 |
| 乙 | T1 | 0.30 | 0.30 |
| 丙 | T2 | 0.20 | 0.20 |
下列说法正确的是
A. 该反应的正反应为吸热反应
B. 达到平衡时,乙中CO2的体积分数比甲中的小
C. T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)<v(逆)
D. T2℃时,若起始时向丙中充入0.06molN2和0.12 molCO2,则达平衡时N2的转化率大于40%
-
一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:2NO(g)+2CO(g) N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
N2(g)+2CO2(g)。各容器中起始物质的量与反应温度如下表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示:
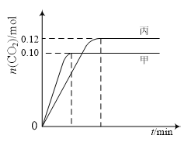
| 容器 | 温度/℃ | 起始物质的量/mol |
| NO (g) | CO (g) |
| 甲 | T1 | 0.20 | 0.20 |
| 乙 | T1 | 0.30 | 0.30 |
| 丙 | T2 | 0.20 | 0.20 |
下列说法正确的是
A. 该反应的正反应为吸热反应
B. 达到平衡时,乙中CO2的体积分数比甲中的小
C. T1℃时,若起始时向甲中充入0.40 mol NO、0.40mol CO、0.40mol N2和0.40mol CO2,则反应达到新平衡前v(正)<v(逆)
D. T2℃时,若起始时向丙中充入0.06molN2和0.12 molCO2,则达平衡时N2的转化率大于40%
-
低碳环保,减轻大气污染,必须从源头上对尾气进行净化处理。回答下列问题
(1)汽车尾气催化转换器中的反应为2NO(g)+2CO(g) 2CO2(g)+N2(g)。若在密闭容器中发生该反应时,c(N2)随温度(T)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。若在密闭容器中发生该反应时,c(N2)随温度(T)和时间(t)的变化曲线如图所示。
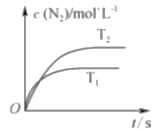
①由图甲可知,温度T1_____T2(填“>”或“<”,下同);该反应的△H_____0。
②能提高尾气转化率的措施有_____(填字母)。
a.升高温度 b.降低温度 c.增大压强 d.增大催化剂的比表面积
(2)煤燃烧产生的烟气中含有氮氧化物,可用CH4催化还原NOx,消除氮氧化物的污染。已知:①CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ•mol﹣1,②N2O4(g)⇌2NO2(g)△H=+56.9k•mol﹣1,③CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣810.1kJ•mol﹣1,从原电池的工作原理分析,可设计为原电池的反应为_____(填序号)。
(3)下图是通过光电转化原理,以燃煤产生的二氧化碳为原料,制备新产品的示意图。试写出光电转化过程中总反应的化学方程式:_____;催化剂a、b之间连接导线上的电流方向是_____。
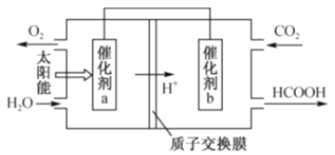
-
燃煤尾气气和汽车尾是造成空气污染的主要原因。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)⇌2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)和时间(t)的变化曲线如图所示。
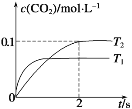
据此判断:
①在T2温度下,0~2 s内的反应速率v(N2)=_______mol /(L·s)。
②该反应的ΔH__________0(选填“>”或“<”)。
(2)煤燃烧产生的烟气中有含氮的氧化物NOx,用CH4催化还原NOx可以消除氮氧化物的污染。
CH4(g)+4NO(g)⇌2N2(g)+CO2(g)+2H2O(g) ΔH<0
CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g) ΔH<0
①若在恒压下,将CH4(g)和NO2(g)置于密闭容器中,发生上述反应。提高NO2转化率的措施有____。
A.加入催化剂 B.降低温度 C.减小投料比[ ] D.增大压强
] D.增大压强
②在容积相同的两个密闭容器内(装有等量的某种催化剂)先各通入等量的CH4,然后再分别充入等物质的量的NO和NO2。在不同温度下,同时分别发生上述的两个反应,并在t秒时测定其中NOx转化率,绘得图像如图所示:
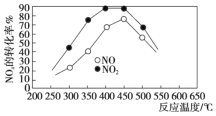
从图中可以得出的结论是:
结论一:在250~450 ℃时,NOx转化率随温度升高而增大,450~600 ℃时NOx转化率随温度升高而减小。推测原因是_____________。
结论二:______________。
-
在不同温度下,向2 L密闭容器中加入1 mol NO和1 mol活性炭,发生反应:2NO(g)+C(s) N2(g)+CO2(g)△H=-213.5 kJ/mol,达到平衡时的数据如下:
N2(g)+CO2(g)△H=-213.5 kJ/mol,达到平衡时的数据如下:
| 温度/℃ | n(活性炭)/mol | n(CO2)/mol |
| T1 | 0.70 | |
| T2 | | 0.25 |
下列说法不正确的是
A. 上述信息可推知:T12
B. T1℃时,该反应的平衡常数K=9/16
C. T2℃时,若反应达平衡后再缩小容器的体积,c(N2):c(NO)不变
D. T1℃时,若开始时反应物的用量均减小一半,平衡后NO的转化率减小
-
向2L密闭容器中加入1molNO和1mol活性炭,发生反应:2NO(g)+C(s)  N2(g)+CO2(g) △H = - 213.5kJ/mol,达到平衡的数据如下:
N2(g)+CO2(g) △H = - 213.5kJ/mol,达到平衡的数据如下:
| 温度/℃ | n(活性炭)/mol | n(CO2)/mol |
| T1 | 0.70 | —— |
| T2 | —— | 0.25 |
下列说法不正确的是( )
A. 上述信息可推知:T1<T2
B. T1℃时,该反应的平衡常数K=9/16
C. T1℃时,若开始时反应物的用量均减小一半,平衡后NO 的转化率减小
D. T2℃时,若反应达平衡后再缩小容器的体积。c(N2)/c(NO)不变
-
向2L密闭容器中加入1molNO和1mol活性炭,发生反应:2NO(g)+C(s)  N2(g)+CO2(g) △H = - 213.5kJ/mol,达到平衡的数据如下:
N2(g)+CO2(g) △H = - 213.5kJ/mol,达到平衡的数据如下:
| 温度/℃ | n(活性炭)/mol | n(CO2)/mol |
| T1 | 0.70 | —— |
| T2 | —— | 0.25 |
下列说法不正确的是( )
A. 上述信息可推知:T1<T2
B. T1℃时,该反应的平衡常数K=9/16
C. T1℃时,若开始时反应物的用量均减小一半,平衡后NO 的转化率减小
D. T2℃时,若反应达平衡后再缩小容器的体积。c(N2)/c(NO)不变
2CO2+N2(g)△H=-QkJ/mol,已知:c(CO2)随温度(T)、时间(t)的变化曲线如右图所示,则:







