-
工业上处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S和CO2.已知:CO(g)+
O2(g)═CO2(g)△H=﹣283.0kJ•mol﹣1 ;S(s)+O2(g)═SO2(g)△H=﹣296.0kJ•mol﹣1此反应的热化学方程式是
A.2CO(g)+SO2(g)═S(s)+2CO2(g)△H=﹣270kJ/mol
B.2CO(g)+SO2(g)═S(s)+2CO2(g)△H=﹣582kJ/mol
C.CO(g)+
SO2(g)═
S(s)+CO2(g)△H=+13kJ/mol
D.CO(g)+
SO2(g)═
S(s)+CO2(g)△H=+135kJ/mol
高二化学选择题中等难度题查看答案及解析
-
工业上处理含CO、SO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质S和CO2,已知:CO(g)+1/2O2(g)═CO2(g)△H=﹣283.0kJ•mol﹣1 S(s)+O2(g)═SO2(g)△H=﹣296.0kJ•mol﹣1此反应的热化学方程式是( )
A. CO(g)+1/2SO2(g)═1/2S(s)+CO2(g)△H=+135kJ/mol
B. CO(g)+1/2SO2(g)═1/2S(s)+CO2(g)△H=+13kJ/mol
C. 2CO(g)+SO2(g)═S(s)+2CO2(g)△H=﹣582kJ/mol
D. 2CO(g)+SO2(g)═S(s)+2CO2(g)△H=﹣270kJ/mol
高二化学单选题中等难度题查看答案及解析
-
处理含 CO、SO2 烟道气污染的一种方法,是将其在催化剂作用下转化为单质S。已知:
2CO(g)+O2(g)=2 CO2(g) △H1=-566.0kJ/mol
S(g)+O2(g)=SO2(g) △H2=-296.0kJ/mol
S(s)+O2(g)=SO2(g) △H3=?
下列说法不正确的是
A. △H3<△H2
B. 将少量 CO 2、SO2分别通入澄清石灰水,都能产生浑浊现象
C. CO2分子中各原子最外层均为8电子稳定结构
D. 相同条件下:2CO(g)+SO2(g)=S(g)+2CO2(g) △H=-270kJ/mol
高二化学选择题中等难度题查看答案及解析
-
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂的作用下转化为单质S。已知:
①CO(g)+0.5O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
则处理CO、SO2的方法的热化学方程式是________________________________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO将NO2还原至N2(CO完全反应),则整个过程中转移电子的物质的量为______mol,放出的热量为_____(用含有a和b的代数式表示)kJ。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1 ①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2 ②
若1 mol CH4还原NO2至N2,整个过程中放出的热量为867 kJ,则ΔH2=_______。
(4)已知下列热化学方程式:
①
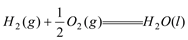 △H=-285.8kJ/mol
△H=-285.8kJ/mol②
 △H=-241.8kJ/mol
△H=-241.8kJ/mol则H2的燃烧热(△H)为________________________。
高二化学简答题简单题查看答案及解析
-
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:①CO(g)+
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是________________________________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为____________mol,放出的热量为____________kJ(用含有a和b的代数式表示)。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH1=-574 kJ·mol-1①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若1 mol CH4还原NO2至N2,整个过程中放出的热量为867 kJ,则ΔH2=____________。
(4)某氮肥厂氨氮废水中的氮元素多以NH
和NH3·H2O形式存在,该废水的处理流程中,NH
在微生物作用的条件下经过两步反应被氧化成NO
。两步反应的能量变化示意如图所示:
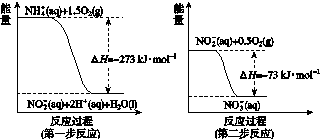
1 mol NH
(aq)全部氧化成NO
(aq)的热化学方程式是________________。
高二化学填空题困难题查看答案及解析
-
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂的作用下转化为单质S。已知:
①CO(g)+0.5O2(g)
CO2(g) ΔH=-283.0kJ·mol-1
②S(s)+O2(g)
SO2(g) ΔH=-296.0kJ·mol-1
则处理CO、SO2的方法的热化学方程式是________________________________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g)
NO(g)+CO2(g) ΔH=-a kJ·mol-1 (a>0)
2CO(g)+2NO(g)
N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下3.36 L CO将NO2还原至N2(CO完全反应),则整个过程中转移电子的物质的量为______mol,放出的热量为_____(用含有a和b的代数式表示)kJ。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)
4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1 ①
CH4(g)+4NO(g)
2N2(g)+CO2(g)+2H2O(g) ΔH2 ②
若1 mol CH4还原NO2至N2,整个过程中放出的热量为867 kJ,则ΔH2=_______。
(4)已知下列热化学方程式:
①H2(g)+0.5O2(g)
H2O(l) △H=-285.8 kJ·mol-1
②H2(g)+0.5O2(g)
H2O(g) △H=-241.8 kJ·mol-1
则H2的燃烧热(△H)为________________________。
高二化学填空题中等难度题查看答案及解析
-
研究 NOx、SO2、CO 等大气污染气体的处理方法具有重要意义。
(1)处理含 CO、SO2 烟道气污染的一种方法是将其在催化剂作用下转化为单质 S。
已知:①CO(g)+ 1/2O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
②S(s)+ O2(g)=SO2(g) ΔH=-296.0kJ·mol-1
此反应的热化学方程式是___________________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
① CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-akJ·mol-1 (a>0)
② 2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-bkJ·mol-1 (b>0)
若用标准状况下 3.36LCO 还原 NO2 至 N2(CO 完全反应)的整个过程中转移电子的物质的量为_______mol,放出的热量为_______ kJ(用含有 a 和 b 的代数式表示)。
(3)用 CH4 催化还原 NOx 也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ·mol-1 ①
CH4(g)+4NO (g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若 1molCH4 还原 NO2 至 N2 整个过程中放出的热量为 867kJ,则 ΔH2=_______ 。
(4)工业上一般用碱溶液来吸收 NO2,SO2。写出用氨水吸收过量 SO2 的离子方程式__________________ 。
高二化学填空题中等难度题查看答案及解析
-
研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
①CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0kJ·mol-1
此反应的热化学方程式是___________________________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g) =NO(g)+CO2(g) ΔH=-akJ·mol-1(a>0)
2CO(g)+2NO(g) =N2(g)+2CO2(g) ΔH=-bkJ·mol-1(b>0)
若用标准状况下3.36LCO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为________mol,放出的热量为________kJ(用含有a和b的代数式表示)
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ·mol-1①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若1molCH4还原NO2至N2,整个过程中放出的热量为867kJ,则ΔH2=________
高二化学填空题中等难度题查看答案及解析
-
研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:1molCO(g)与适量的SO2(g)反应生成S(s)和CO2(g)时,放出135kJ的热量,则此反应的热化学方程式为______________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体,用CO(g)处理NO2(g)的能量转化关系如图所示。

标准状况下,22.4LCO和NO2发生上述反应。整个过程中,转移电子的物质的量为___________mol,放出的热量为___________kJ(用含有a的代数式表示)。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574kJ/mol
② CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2
若1molCH4(g)直接将NO2(g)还原至N2(g),整个过程中放出的热量为867kJ,则△H2=_____________。
高二化学填空题困难题查看答案及解析
-
Ⅰ.烟道气中含有的CO和SO2是重要的污染物,可在催化剂作用下将它们转化为S(s)和CO2,此反应的热化学方程
式为_____________________。
已知:CO(g) +1/2O2(g) = CO2(g) △H=-283.0kJ·mol-1;
S(s)+O2=SO2(g) △H=-296.0 kJ·mol-1
Ⅱ.氨的合成是最重要的化工
生产之一。在2个恒压的密闭容器中,同温度下、使用相同催化剂分别进行反应:3H2(g)+N2(g)
2NH3(g),按不同方式投入反应物,保持恒温,反应达到平衡时有关数据为:
容 器
甲
乙
反应物投入量
3 mol H2、2 mol N2
6 mol H2、4mol N2
达到平衡的时间(min)
t
5
平衡时N2的浓度(mol·L-1)
3
c
(1)该反应的平衡常数表达式K=_______________。
(2)甲容器达到平衡所需要的时间t 5min(填“>”、“<” 或“=”);
Ⅲ.下表是不同温度下水的离子积数据:
温度/℃
25
t1
t2
Kw/ mol2·L-2
1×10-14
a
1×10-12
试回答以下几个问题:
(1)若25< t1< t2,则a________1×10-14(填“<”、“>”或“=”)。
(2)在25℃下,pH=10的NaOH溶液中,水电离产生的c(OH—)为:____________mol/L。
(3)在t2℃下,将pH=9的氢氧化钠溶液V1 L与pH=4的硫酸溶液V2 L混合(设混合后溶液体积为原两溶液体积之和)所得溶液的pH=7,则V1︰V2 = ___________
高二化学填空题困难题查看答案及解析