-
已知:A、B、C、D、E、F六种元素核电荷数依次增大,属元素周期表中前四周期的元素。其中A原子核外有三个未成对电子;B和E可形成离子化合物B2E,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F原子核外最外层电子数与B相同,其余各层均充满。请根据以上信息,回答下列问题:
⑴A、B、C、D的第一电离能由小到大的顺序为________(用元素符号表示)。
⑵E与D的同族短周期元素可形成一种化合物X,X是常见的有机溶剂,X分子的空间构型是________。
⑶F原子的核外电子排布式是____________,F的高价离子与A的简单氢化物形成的配离子的化学式为________。
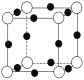
⑷A、F形成某种化合物的晶胞结构如图所示,则其化学式为________(黑色球表示F原子)。
⑸A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,其晶体中所含的化学键类型为________。
-
已知A,B,C,D、E都是周期表中前四周期的元素,且原子序数依次增大,其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题(答题时,A,B,C,D,E用所对应的元素符号表示):
(1)比E核外电子数少5的元素的原子核外电子排布式是_________,A,B,C,D的第一电离能由小到大的顺序为_______。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是________________。
(3)A的氢化物属于______(填“极性”或“非极性”)分子,D的低价氧化物分子的空间构型是_______。
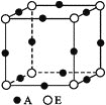
(4)A,E形成的某种化合物的晶胞结构如图所示,则其化学式为______(每个球均表示1个原子)。
-
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)B的轨道排布式是_____________________________________,A、B、C、D的第一电离能由小到大的顺序为___________________________________________。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是________________________;
(3)A的最高价含氧酸根离子中,其中心原子采取____________杂化,D的低价氧化物分子的空间构型是___________________________。
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为________________;(每个球均表示1个原子) 若相邻A原子和E原子间的距离为a nm,阿伏伽德罗常数为NA,则该晶体的密度为_____________g/cm3(用含a、NA的符号表示)。

-
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)B的轨道排布式是_____________________________________,A、B、C、D的第一电离能由小到大的顺序为___________________________________________。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是________________________;
(3)A的最高价含氧酸根离子中,其中心原子采取____________杂化,D的低价氧化物分子的空间构型是___________________________。
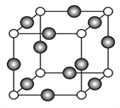
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为________________;(每个球均表示1个原子) 若相邻A原子和E原子间的距离为a nm,阿伏伽德罗常数为NA,则该晶体的密度为_____________g/cm3(用含a、NA的符号表示)。
-
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原子核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)A、B、C、D的第一电离能由小到大的顺序为____________________________________。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是________________________;
(3)A的最高价含氧酸根离子中,其中心原子采取____________杂化,D的低价氧化物分子的空间构型是___________________________。
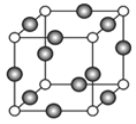
(4)A、E形成某种化合物的晶胞结构如图所示,则其化学式为________________;(每个球均表示1个原子) 若相邻A原子和E原子间的距离为a nm,阿伏伽德罗常数为NA,则该晶体的密度为_____________g/cm3(用含a、NA的符号表示)。
-
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大。其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原予核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满。请根据以上信息,回答下列问题: (答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E的核外电子排布式是________,A、B、C、D的第一电离能由小到大的顺序为________。
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是________;
(3)A的最高价含氧酸根离子中,其中心原子采取________杂化,D的低价氧化物分子的空间构型是________。
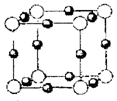
(4)A、E形成某种化合物的晶胞结构如下图所示,则其化学式为________;(每个球均表示1个原子)
-
已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大.其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原予核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)E的核外电子排布式是______,A、B、C、D的第一电离能由小到大的顺序为______.
(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是______;
(3)A的最高价含氧酸根离子中,其中心原子采取______杂化,D的低价氧化物分子的空间构型是______.
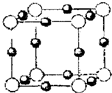
(4)A、E形成某种化合物的晶胞结构如下图所示,则其化学式为______;(每个球均表示1个原子)
-
X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素。
下列说法正确的是 ( )
A. 五种元素的原子半径从大到小的顺序是:M﹥W>Z>Y>X
B. Z与同主族相邻元素的非金属性强弱,可通过它们的氧化物对应水化物的酸性强弱来判断
C. X、Z两元素能形成原子个数比(X:Z)为3:1和4:2的化合物
D. 用M单质的熔点高于其氧化物的熔点
-
已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C、F属同一主族,B原子最外电子层的p能级上的电子处于半满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。请用具体的元素回答下列问题:
(1)E元素基态原子电子排布式为______________。
(2)用电子排布图表示F元素原子的价电子构型____________。
(3)F、G元素对应的最高价含氧酸中酸性较强的化学式为__________。
(4)离子半径:D+__________B3-,第一电离能:B__________C,电负性:C__________F。(填“<”、“>”或“=”)
(5)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为____________,试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式_________________。
-
已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C、F属同一主族,B原子最外电子层的p能级上的电子处于半满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。请用具体的元素回答下列问题:
(1)E元素基态原子电子排布式为______________。
(2)F、G元素对应的最高价含氧酸中酸性较强的化学式为__________。
(3)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为____________(2分),试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式___________________________________________。
(4)写出E与D的最高价氧化物对应的水化物反应的化学方程式____________。
(5)离子半径:D+______B3-,电负性:C_______F。(填“<”、“>”或“=”)(各1分)






