-
已知元素A、B、C、D和E的原子序数依次增大。A、B、C、D四种元素核电荷数均小于20,A、B同主族;B、C、D元素的基态原子具有相同的能层数,它们的基态原子中p能级上未成对电子数分别为1、3、1;E是周期表中(除放射性元素外)第一电离能最小的元素。回答下列问题:
(1)写出下列元素的符号:A 、E 。
(2)C元素的价电子排布图为: ;
该排布遵循的原理主要有: (答完整得分)。
(3)C、D元素形成的化合物主要有: (填化学式,答完整得分);其中相对分子质量较小的分子为 分子(填“极性”或“非极性”),该分子的空间构型为 ,中心原子的杂化方式是 。
(4)化合物BD3的熔点190℃、沸点182.7℃,那么BD3的晶体类型为 ;事实上,在BD3的化合物中往往以B2D6的形式存在,该形式的存在是由于 形成的。(选填“氢键”、“范德华力”、“离子键”、“配位键”)
(5)下图为几种晶胞(或晶胞的1/8)示意图,其中 和
和 代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。
代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。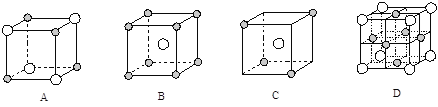
-
已知元素A、B、C、D和E的原子序数依次增大。A、B、C、D四种元素核电荷数均小于20,A、B同主族;B、C、D元素的基态原子具有相同的能层数,它们的基态原子中p能级上未成对电子数分别为1、3、1;E是周期表中(除放射性元素外)第一电离能最小的元素。回答下列问题:
(1)写出下列元素的符号:A ________、E________。
(2)C元素的价电子排布图为:________ ;
该排布遵循的原理主要有:________(答完整得分)。
(3)C、D元素形成的化合物主要有:________(填化学式,答完整得分);其中相对分子质量较小的分子为________分子(填“极性”或“非极性”),该分子的空间构型为________,中心原子的杂化方式是________。
(4)化合物BD3的熔点190℃、沸点182.7℃,那么BD3的晶体类型为________;事实上,在BD3的化合物中往往以B2D6的形式存在,该形式的存在是由于________形成的。(选填“氢键”、“范德华力”、“离子键”、“配位键”)
(5)下图为几种晶胞(或晶胞的1/8)示意图,其中 和
和 代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的________(填序号),在该晶胞中阳离子的配位数为________。
代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的________(填序号),在该晶胞中阳离子的配位数为________。

-
(15分)已知A、B、C、D、E、F、G七种元素原子序数均小于36,它们的核电荷数依次增大。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的基态电子排布中L能层有两个未成对电子,E和D同主族;F原子的基态电子排布中有4个未成对电子;G与F在周期表中同族,且G原子的外围电子排布中有2个未成对电子。根据以上信息填空:
(1) B、C、D三种元素的电负性由大到小的顺序为 (用元素符号表示)
(2)F2+离子的价层电子排布图是 ,
(3)B元素的最高价氧化物对应的水化物中心原子采取的轨道杂化方式为 ,E元素的氢化物的VSEPR模型为 。
(4)A和C形成的二元共价化合物中,分子中既含有极性共价键、又含有非极性共价键的化合物_____(填化学式);其中心原子C的杂化方式为 。
(5)化合物BD2、C2D和阴离子EBC-互为等电子体,它们结构相似,EBC-的电子式为 。F常作为配合物的中心离子,1mol F(BC)63-中含有σ键的数目为_______;
(6)GD的晶体结构与氯化钠相同,在晶胞中G离子的配位数是_______;已知晶胞的边长为a nm,晶体的摩尔质量为b g·mol-1,NA为阿伏加德罗常数的值,则晶体的密度为_________g·cm-3。
-
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36。已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子。
(1)Y原子核外共有________种不同运动状态的电子,T原子有________种不同能级的电子。
(2)X、Y、Z的第一电离能由小到大的顺序为________________(用元素符号表示)。
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为___________。
(4)Z与R能形成化合物甲,甲与氢氟酸反应,生成物的分子空间构型分别为_________、_________。
(5)G、Q、R氟化物的熔点如下表,造成熔点差异的原因为___________________。
| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1539 | 183 |
(6)果农常用的杀菌剂——波尔多液是由T的硫酸盐溶液和生石灰制得。若在所制得的波尔多液的沉淀上,再喷射氨水,会看到沉淀溶解变成蓝色透明溶液,得到配位数为4的配合物,写出上述沉淀溶解过程的离子方程式____________________。

(7)X单质的晶胞如图所示,若X晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个X原子之间的距离为________cm(用ρ、NA表示,并化成最简形式)。
-
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有有2个未成对电子;Q原子的S能级和P能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料,T处于周期表的ds区原子中只有一个未成对的电子。下列说法不正确的是( )
A. Y原子核外有7中不同运动状态的电子,基态T原子有7种不同能级的电子。
B. X、Y、Z的第一电离能由小到大的顺序为X<Z<Y。
C. 由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,且ZXY-中X原子的杂化方式为sp
D. Q的氧化物与X的单质在一定条件下能发生置换反应。
-
(选做题)(8分)有V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且均小于20,其中X、Z是金属元素,V和Z元素原子的最外层都只有一个电子,W和Y元素原子的最外层电子数相等,且W元素原子L层电子数是K层电子数的3倍,X元素原子的最外层电子数是Y元素原子最外层电子数的一半。由此可推知(填元素符号):
V是__________ W是__________ X是__________ Y是__________
-
有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20,其中C、E是金属元素;A和E属同一族,且A为非金属元素,它们原子的最外层电子排布为ns1,B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍。C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)A是________,B是________,E是________(写元素符号)。
(2)写出C元素基态原子的电子排布式__________________________________。
(3)用轨道表示式表示D元素原子的价电子排布__________________________。
-
A、B、C、D、E、F 6种元素,它们的核电荷数依次增大,且都小于36。其中C、E、F是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。请回答下列问题:
(1)C、D、E四种元素的简单离子按半径由小到大的顺序为(用离子符号表示)_______________。
(2)元素B与D的电负性的大小关系是__________,C与E的第一电离能的大小关系是_______。(填>、<、=,用元素符号表示)
(3)用轨道表示式表示D元素原子的价电子构型_______________________。
(4)C、E最高价氧化物对应的水化物相互反应的离子方程式为_________________。
(5)F在元素周期表中的位置是___________区,其基态原子的电子排布式为____________________。
(6)均为A、B、D、E四种元素组成的两种化合物可以相互反应,写出该反应的离子方程式为________。
-
(8分) 有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)由这五种元素组成的一种化合物是(写化学式)________________________。
(2)写出C元素基态原子的电子排布式_________________________。
(3)元素B与D的电负性的大小关系是___________,C与E的第一电离能的大小关系是___________。(填﹥、﹤、﹦)
-
A、B、C、D、E、F 6种元素,它们的核电荷数依次增大,且都小于36。其中C、E、F是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子。
请回答下列问题:
(1)C、D、E四种元素的简单离子按半径由小到大的顺序为(用离子符号表示) 。
(2)元素B与D的电负性的大小关系是 ,C与E的第一电离能的大小关系是 。(填>、<、=,用元素符号表示)
(3)用轨道表示式表示D元素原子的价电子构型 。
(4)C、E最高价氧化物对应的水化物相互反应的离子方程式为 。
(5)F在元素周期表中的位置是 区,其基态原子的电子排布式为 。
(6)均为A、B、D、E四种元素组成的两种化合物可以相互反应,写出该反应的离子方程式为 。
和
代表两种不同的粒子。E与D形成的化合物的晶胞是下列中的 (填序号),在该晶胞中阳离子的配位数为 。


