-
KMnO4是实验室常用的氧化剂,可用作水处理剂等。
(1)实验室用MnO2等为原料制取少量KMnO4的实验流程如下:
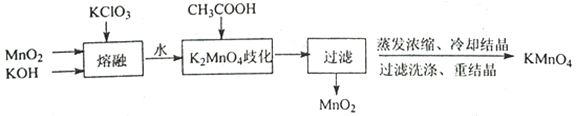
①“熔融”时,可用作坩埚材质的是__________ (填序号)。
a.氧化铝 b.陶瓷 c.铁 d.玻璃
②“K2MnO4歧化”的离子方程式为__________。
③“蒸发浓缩”时,温度需控制在80℃,适宜的加热方式是__________。
(2)高锰酸钾法测定水体COD (化学雷氧量) 的实验步骤如下:
步骤1.准确移取100mL 水样,置于250mL 锥形瓶中。加入10mL1∶3 的硫酸,再加入15.00mL0.0200 mol·L-1KMnO4 溶液(此时溶液仍呈紫红色)。
步骤2.用小火煮沸10min (水中还原性物质被MnO4-氧化,本身还原为Mn2+),取下锥形瓶趁热加10.00mL0.0500mol·L-1Na2C2O4溶液,充分振荡(此时溶液为无色)。
步 骤3.趁热用0.0200 mol·L-1KMnO4溶液滴定至呈微红色,消耗KMnO4 溶液4.500mL。通过计算确定该水样的化学需氧量(写出计算过程)。__________________[已知: COD是指在一定条件下,以氧化1L水样中还原性物质所消耗的氧化剂的量,通常换算为需要的O2的质量(mg),COD的单位mg·L-1。]
-
以二氧化锰为原料制取高锰酸钾晶体的实验流程如下:
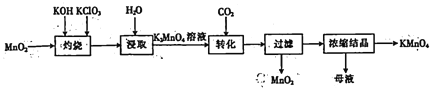
下列有关说法正确的是
A. “灼烧”时,可在玻璃坩埚中进行
B. “浸取”时,可用无水乙醇代替水
C. “转化”反应中,生成的KMnO4与MnO2的物质的量之比为1:2
D. “浓缩结晶”后的母液中可能含有KMnO4和K2CO3两种溶质
-
以二氧化锰为原料制取高锰酸钾晶体的实验流程如下:
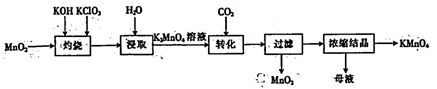
下列有关说法正确的是
A. “灼烧”时,可在玻璃坩埚中进行
B. “浸取”时,可用无水乙醇代替水
C. “转化”反应中,生成的KMnO4与MnO2的物质的量之比为1:2
D. “浓缩结晶”后的母液中可能含有KMnO4和K2CO3两种溶质
-
以二氧化锰为原料制取高锰酸钾晶体的实验流程如下,下列有关说法正确的是
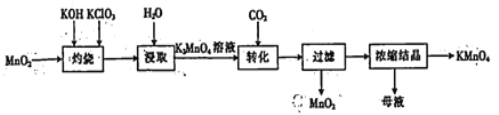
A. “灼烧”时,可在瓷坩埚中进行
B. “浸取”时,可用无水乙醇代替水
C. “转化”反应中,生成的KMnO4与MnO2的物质的量之比为1:2
D. “浓缩结晶”后的母液中仍可能含有KMnO4和K2CO3两种溶质
-
高锰酸钾是常用的氧化剂。某化学小组在实验室以软锰矿(主要成分是MnO2)为原料制备KMnO4,下图是实验室制备高锰酸钾的操作流程。
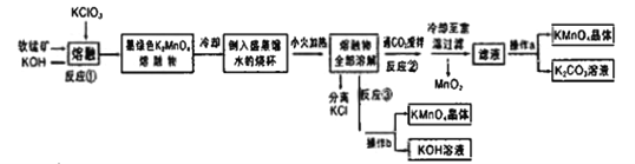
已知:
| 温度 | 溶解度/g |
| K2CO3 | KHCO3 | KMnO4 |
| 20℃ | 111 | 33.7 | 6.38 |
请回答:
(1)反应①的化学方程式为______。加热软锰矿、KClO3、和KOH固体时,除三脚架、玻璃棒、泥三角和铁坩埚外,还用到的仪器有_____,不采用瓷坩埚而选用铁坩埚的理由是________。
(2)反应②中氧化产物与还原产物的物质的量之比为________;上述流程中可以循环利用的物质是__________
(3)实验时,从滤液中得到KMnO4晶体的实验操作a为_____。若CO2过量会生成KHCO3导致得到的KMnO4产品的纯度降低其原因是_________
(4)反应③是模拟工业上采用惰性电极电解法制取高锰酸钾晶体,写出反应的化学方程式_____。
-
高锰酸钾[KMnO4]是常用的氧化剂。工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体。中间产物为锰酸钾[K2MnO4]。下图是实验室模拟制备的操作流程:
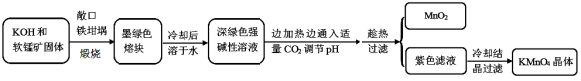
相关资料:
①物质溶解度
| 物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
| 20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
②锰酸钾[K2MnO4]
外观性状:墨绿色结晶。其水溶液呈深绿色,这是锰酸根(MnO42—)的特征颜色。
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42—会发生歧化反应。
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是______________;
(2)实验时,若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低。请写出实验中通入适量CO2时体系中可能发生反应离子方程式 : ;
其中氧化还原反应中氧化剂和还原剂的质量比为_________________________。
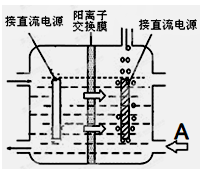
(3)由于CO2的通入量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸。从理论上分析,选用下列酸中________ ,得到的产品纯度更高。
A.醋酸 B.浓盐酸 C.稀硫酸
工业上采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程式_______________
提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图)。使用阳离子交换膜可以提高Mn元素利用率的原因为 ___________________________________。
-
高锰酸钾[KMnO4]是常用的氧化剂。工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体。中间产物为锰酸钾[K2MnO4]。下图是实验室模拟制备的操作流程:
 :
:
相关资料:
①物质溶解度
| 物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
| 20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
②锰酸钾[K2MnO4]
外观性状:墨绿色结晶。其水溶液呈深绿色,这是锰酸根(MnO42—)的特征颜色。
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42—会发生歧化反应。
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是______________;
(2)实验时,若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低。请写出实验中通入适量CO2时体系中可能发生反应离子方程式 : ;其中氧化还原反应中氧化剂和还原剂的质量比为_________________。

(3)由于CO2的通入量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸。从理论上分析,选用下列酸中____________,得到的产品纯度更高。
A.醋酸 B.浓盐酸 C.稀硫酸
(4)工业上采用惰性电极电解锰酸钾溶液制取高锰酸钾,
试写出该电解反应的化学方程式_______________。
提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图)。
图中A口加入的溶液最好为_______。使用阳离子交换膜可以提高Mn元素利用率的原因为_________。
-
(15分)高锰酸钾[KMnO4]是常用的氧化剂。工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体。中间产物为锰酸钾[K2MnO4]。下图是实验室模拟制备的操作流程:

相关资料:
①物质溶解度
| 物质 | KMnO4 | K2CO3 | KHCO3网] | K2SO4 | CH3COOK |
| 20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
②锰酸钾[K2MnO4]
外观性状:墨绿色结晶。其水溶液呈深绿色,这是锰酸根(MnO42—)的特征颜色。
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42—会发生歧化反应。
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是______________;
实验中用铁坩埚煅烧暴露在空气中的固体混合物发生反应的化学方程式为_______。
(2)实验时,若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低。请写出实验中通入适量CO2时体系中可能发生反应离子方程式 : ;
其中氧化还原反应中氧化剂和还原剂的质量比为_________________________。
(3)由于CO2的通人量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸。从理论上分析,选用下列酸中________ ,得到的产品纯度更高。
A.醋酸 B.浓盐酸 C.稀硫酸
(4)工业上一般采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程为_________;
传统工艺采用无膜电解法由于副反应发生,Mn元素利用率和电流效率都会偏低。有同学联想到离子交换膜法电解饱和食盐水提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图)。

图中A口加入的溶液最好为__________。
使用阳离子交换膜可以提高Mn元素利用率的原因为_______________。
-
高锰酸钾(KMnO4)是常用的氧化剂,工业上以软锰矿(主要成分是MnO2)为,原料制备高锰酸钾晶体。中间产物为锰酸钾(K2MnO4)下图1是实验室模拟制备的操作流程:
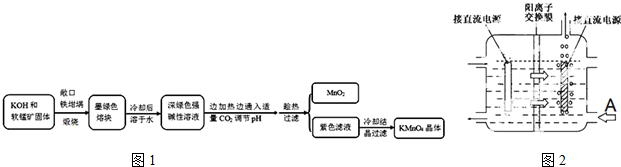
相关资料:
①物质溶解度
| 物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
| 20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
②锰酸钾[K2MnO4]外观性状:墨绿色结晶.其水溶液呈深绿色,这是锰酸根(MnO42-)的特征颜色.
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42-会发生歧化反应.
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是______________;实验中用 铁坩埚煅烧暴露在空气中的固体混合物发生反应的化学方程式为______________。
(2)实验时,若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低.请写出实验中通入适量CO2时体系中可能发生反应离子方程式______________;其中氧化还原反应中氧化剂和还原剂的质量比为________。
(3)由于CO2的通人量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸.从理论上分析,选用下列酸中_______,得到的产品纯度更高.
A.醋酸 B.浓盐酸 C.稀硫酸
(4)工业上一般采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程式______________;传统工艺采用无膜电解法由于副反应发生,Mn元素利用率和电流效率都会偏低.有同学联想到离子交换膜法电解饱和食盐水提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图2).图中A口加入的溶液最好为_________;使用阳离子交换膜可以提高Mn元素利用率的原因为______________。
-
碳酸锰可用作脱硫的催化剂,是合成二氧化锰和制造其他锰盐的原料。工业上从锰泥(主要含KMnO4和少量MnO2、CuO、PbO等)中回收MnCO3的流程如图所示:
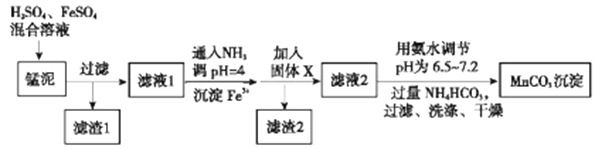
回答下列问题:
(1)“滤渣1”中的主要成分为PbSO4,其中Pb元素的化合价是__。
(2)Fe2+能将MnO2还原为Mn2+,该反应的离子方程式:__。
为检验FeSO4是否被氧化,可往滤液1中加入__溶液(填化学式)。
(3)已知Ksp[Fe(OH)3]=4.0×10-38,通入NH3调pH=4时,溶液中c(Fe3+)=__。
(4)流程中加入固体X能使Cu2+沉淀,则最适宜的固体X为__(填字母)。
a.MnS b.ZnS c.Ca(OH)2 d.Ba(OH)2
(5)加入氨水和过量NH4HCO3生成MnCO3沉淀的离子方程式为__。
(6)处理锰泥时,H2SO4、FeSO4混合溶液中 比值不宜过大,请从节约药品的角度分析,原因是___。
比值不宜过大,请从节约药品的角度分析,原因是___。
(7)若利用100t锰泥制得55tMnCO3,反应中Mn元素的转化率为80.0%,则锰泥中Mn元素的质量分数为__%(精确到小数点后1位)。







 :
:



