-
用所学知识回答下列问题:
(1)已知常温下,Ksp[Mg(OH)2]=5×  ,若某溶液常温下刚 析出Mg(OH)2固体时,c(Mg2+)=5×
,若某溶液常温下刚 析出Mg(OH)2固体时,c(Mg2+)=5×  mol/L,则此时溶液的pH=______。
mol/L,则此时溶液的pH=______。
(2)已知CH3COONH4溶液呈中性,又知CH3COOH溶液加到NaHCO3溶液中有气体放出,试推断常温下NH4HCO3溶液的pH______7(填“>”、“<”或“=”)。
(3)25℃时,pH=11的KOH溶液中,由水电离出的c(OH-)=_______mol/L。
(4)25℃时,pH=11的K2CO3溶液中,由水电离出的c(OH-)=_______mol/L。
-
常温下,已知Mg(OH)2溶度积常数Ksp=1.8×10-11,则足量Mg(OH)2固体溶解在pH=12的NaOH溶液中Mg2+浓度为( )
A.1.8×10-7mol/L B.1.0×10-5mol/L
C.1.0×10-7mol/L D.1.8×10-9mol/L
-
已知:25℃时,Ksp[MgF2] = 7.42×10-11 ,Ksp[Mg(OH)2] = 5.61×10-12 ,请回答下列问题:
 (1)25℃时,①饱和Mg(OH)2溶液与②饱和MgF2溶液相比,c(Mg2+)较大的是 ;(填①或②)
(1)25℃时,①饱和Mg(OH)2溶液与②饱和MgF2溶液相比,c(Mg2+)较大的是 ;(填①或②)
(2)25℃时,在Mg (OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)将 ;Mg (OH)2的Ksp将 ,(填“增大”“减小”或“不变”),请写出Mg (OH)2的溶度积的表达式Ksp = ;
(3)25℃时,在MgF2的悬浊液中加入浓的NaOH溶液后,MgF2 转化成为Mg (OH)2 . (填“能”或“不能”)
(4)某氯化镁溶液里c(Mg2+)=0.0561 mol·L-1,如要生成Mg(OH)2,应调整溶液pH,使之大于________。
-
计算题
(1)常温常压下,已知Ksp(AgCl)=1.8×10-10,Ksp(Mg(OH)2)=5.6×10-12试通过计算说明饱和AgCl溶液和Mg(OH)2溶液溶解度的大小;并且说明溶度积与溶解度之间的关系;[已知1.8½=1.34,1.4½=1.12]
(2)常温下,将0.05mol/L盐酸溶液和未知浓度的NaOH溶液以1:2的体积比混合,所得溶液的pH=12。用上述NaOH溶液13 mL和pH=3的某一元弱酸HA溶液20ml恰好完全反应生成NaA。试求:
①此一元弱酸的物质的量浓度。
②求此条件下该一元弱酸的电离平衡常数。
-
已知:Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
Ⅱ、25℃时有关物质的溶度积如下:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe (OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺线路如下:
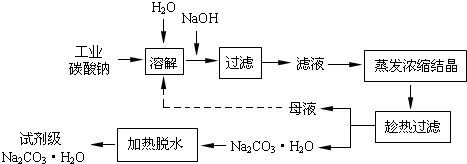
(1)加入NaOH溶液时,反应的离子方程式为__________________;
(2)向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)= ___________;
(3)“母液”中除了含有Na+、CO32-外,还含有_________等离子。
(4)有人从“绿色化学”角度设想将“母液”沿流程中虚线所示进行循环使用。请你分析实际工业生产中是否可行_________(填“可行”或“不可行”),并说明理由__________________;
(5)已知:Na2CO3•10H2O(s)=Na2CO3(s)+10H2O(g)△H=+532.36kJ•mol-1
Na2CO3•10H2O(s)=Na2CO3•H2O(s)+9H2O(g) △H=+473.63kJ•mol-1
写出Na2CO3•H2O脱水反应的热化学方程式__________________;
-
目前世界各国获得镁的主要来源从海水中提取,以下是提取镁的过程中涉及到的几种物质常温下的溶度积常数,根据你所学的知识回答下面的几个问题:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 |
| 溶度积 | 2.8×10-9 | 6.8×10-6 | 5.5×10-6 | 1.8×10-11 |
(1)在从海水中提取镁时,往往用到贝壳(主要成分是CaCO3),你认为________(填“能”或“不能”)通过将贝壳研磨成粉末直接投入海水里制备含镁的沉淀,理由是________。如果不能直接投入,应将贝壳作何处理,试写出化学方程式:________。(若第一个空格填“能”,此空格不填;若填“不能”, 此空格只须第一步处理的化学反应方程式。)
(2)已知某地海水中的镁离子的浓度为1.8×10-3 mol·L-1,则常温下要使镁离子产生沉淀,溶液pH最低应为________。
(3)实验室中常用CaCO3制CO2,其产物之一的氯化钙是应用广泛的化学试剂,可作干燥剂、冷冻剂等。为了测定某氯化钙样品中钙元素的含量,进行如下实验:
(I)准确称取氯化钙样品0.2000g,放入烧杯中,加入适量6mol/L的盐酸和适量蒸馏水使样品完全溶解,再加入35mL 0.25mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀,经检验,Ca2+已沉淀完全。
(II)过滤并洗涤(I)所得沉淀。
(III)加入足量的10% H2SO4溶液和适量的蒸馏水,(II)中沉淀完全溶解,溶液呈酸性,加热至75℃,趁热逐滴加入0.05000 mol/L KMnO4溶液16.00mL,恰好完全反应。请回答:
已知滴定过程发生的反应为2MnO4- + 5H2C2O4 + 6H+ ="=2" Mn2+ +10 CO2↑+8 H2O(已配平)
①0.05000 mol/L KMnO4溶液标准溶液应置于________(选填“酸式”或“碱式”)滴定管中。
②滴定终点的现象为________。
③该氯化钙样品中钙元素的质量百分数为________。
-
根据所学知识回答下列问题。
(1)已知Ksp(BaCO3) =2.6×l0-9,Ksp(BaSO4)=1.1×10-10。
①BaCO3在20 mL 0.01 mol·L-1Na2CO3溶液中的Ksp _________(填“大于”、“小于”或“等于”)其在20 mL 0.01 mol·L-1 BaCl2溶液中的Ksp
②现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为_______mol/L。
③向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中c(CO32—)/c(SO42—)=___________(保留三位有效数字)。
(2)已知25℃ 时,Ksp[AgCl]=1.8×10-10,现将足量氯化银分别放入:a.100mL蒸馏水中;b.100mL 0.2 mol/LAgNO3溶液中;c.100mL 0.1 mol/L氯化铝溶液中;d.100mL 0.1 mol/L盐酸溶液中。充分搅抖后,相同温度下银离子浓度由大到小的顺序是_______________。(填写序号);b中氯离子的浓度为__________mol/L。
-
镁是一种重要的金属资源,在工业上用途广泛。回答下列问题:
(1)已知某温度下Mg(OH)2的Ksp = 6.4×l0-12,当溶液中c(Mg2+) ≤1.0×10-5mol/L可视为沉淀完全,则此温度下应保持溶液中c(OH-) ≥ ______mol·L-1。
(2)已知常温下CH3COOH的电离常数为:Ka = l.75×10-5mol/L;NH3·H2O的电离常数为,Kb =1.76×l0-5mol/L。A.NH4Cl溶液显酸性,原因是_________________________(用离子方程式表示),NH4Cl溶液中所有离子的浓度由大到小的顺序为_________________________;
B.CH3COONH4溶液显___________ (填“酸”、“碱”或“中”)性。
C.将饱和NH4Cl溶液滴入少量的Mg(OH)2悬浊液中,可看到白色沉淀溶解。产生这种现象的原因存在以下两种观点。
观点①:2NH4+ + Mg(OH)2= 2NH3·H2O+ Mg2+ ;
观点②的离子方程式为_________________________。
要验证①和②谁是Mg(OH)2溶解的主要原因,可选取______________(填序号)代替NH4Cl溶液作对照实验。
a. NH4NO3 b. (NH4)2SO4 c. CH3COONH4 d. NH4HSO4
-
已知常温时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13.0,则下列说法不正确的是( )
A. 所得溶液中的c(H+)=1.0×10-13 mol·L-1
B. 所得溶液中由水电离产生的c(H+)=1.0×10-13 mol·L-1
C. 所加的烧碱溶液pH=13.0
D. 所得溶液中的c(Mg2+)=5.6×10-10 mol·L-1
-
已知在25℃时,Ksp[Mg(OH)2]=3.2×10-11,Ksp[Cu(OH)2]=2.0×10-20
(1)在25℃时,向0.02mol/L的MgCl2溶液中加入NaOH固体,如果生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为______mol/L;
(2)在25℃时,向浓度均为0.02mol/L的MgCl2和CuCl2混合溶液中逐滴加入NaOH溶液,先生成______沉淀(填化学式);生成该沉淀的离子方程式为_______;当两种沉淀共存时,c(Mg2+)/c(Cu2+)=________。
,若某溶液常温下刚 析出Mg(OH)2固体时,c(Mg2+)=5×
mol/L,则此时溶液的pH=______。
