-
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:______与盐酸反应最剧烈,____与盐酸反应的速度最慢;____与盐酸反应产生的气体最多.
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为______________________________;
(3)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_________,________________;
Ⅱ.利用图装置可验证同主族元素非金属性的变化规律
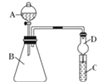
(4)干燥管D的作用为_______________;
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液________________________的现象,即可证明.但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有______________溶液的洗气瓶.
-
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果:__________与盐酸反应最剧烈,__________与盐酸反应最慢。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_______,________________。
Ⅱ.利用下图装置可以验证非金属性的变化规律。
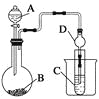
(3)仪器A的名称为________,干燥管D的作用是______________。
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_________________________。
(5)若要证明非金属性:C>Si,则A中加________、B中加Na2CO3、C中加________,观察到C中溶液的现象为__________________________。
-
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果:__________与盐酸反应最剧烈,__________与盐酸反应最慢。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_______,________________。
Ⅱ.利用下图装置可以验证非金属性的变化规律。
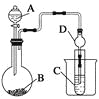
(3)仪器A的名称为________,干燥管D的作用是______________。
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_________________________。
(5)若要证明非金属性:C>Si,则A中加________、B中加Na2CO3、C中加________,观察到C中溶液的现象为__________________________。
-
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果:__________与盐酸反应最剧烈,__________与盐酸反应最慢。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_______,________________。
Ⅱ.利用下图装置可以验证非金属性的变化规律。
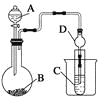
(3)仪器A的名称为________,干燥管D的作用是______________。
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_________________________。
(5)若要证明非金属性:C>Si,则A中加________、B中加Na2CO3、C中加________,观察到C中溶液的现象为__________________________。
-
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
(1)将镁、铝、铁各0.1 mol分别投入到过量且等量的0.1 mol·L-1的盐酸中,写出与盐酸反应最慢的金属发生反应的化学方程式__________________。
(2)利用下图装置可以验证非金属性的变化规律。
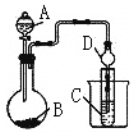
①实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属比硫强;装置B中所装药品为_____________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_________________________。
②若要证明非金属性:C>Si,则A中加________、B中加Na2CO3、C中加Na2SiO3,观察到C中的实验现象为有白色沉淀物生成。离子方程式为_____________(所通气体过量)。
-
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,写出与盐酸反应最慢的金属发生反应的离子方程式__________。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理___________?并说明理由:________________。
Ⅱ.利用下图装置可以验证非金属性的变化规律。

(3)实验室中现有药品Na2S、KMn O4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置B中所装药品为_____________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_________________________。
O4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置B中所装药品为_____________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为_________________________。
(4)若要证明非金属性:C>Si,则A中加________、B中加Na2CO3、C中加Na2SiO3,观察到C中的实验现象为有白色沉淀物生成。离子方程式为____________________(假设所通气体是过量的)。
-
某化学研究性学习小组为探究元素性质的变化规律,设计了如下实验:
(1)甲同学根据同周期元素原子结构的变化规律,预测出同一周期,从左至右元素的金属性逐渐减弱.请你根据实验室常用试剂和仪器帮助甲同学设计实验,简述实验步骤和现象(以第三周期元素为例):______.
(2)乙同学欲比较N、C、Si的非金属性强弱,设计了图1所示的实验装置,其能否达到实验目的______(填“能”或“不能”),设计的理论依据是______. 但也有同学根据硝酸具有挥发性,认为乙同学的实验装置存在不足,请你帮助该同学提出修改意见______.
(3)丙同学从资料中获悉:元素周期表中处于象硼与硅这样“对角线”位置的某些元素性质相似.预测金属铍应该具有与______相似的性质,能证明其预测的实验方案是______.
(4)丁同学设计了如图2装置验证元素性质递变规律.A、B、C处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.丁同学可能观察到的现象有______. 从环保角度考虑,该装置有明显不足,请指出并提出改进建议______.

-
某化学兴趣小组的同学学习了同周期元素性质递变规律后,设计了一套实验方案进行实验探究,并记录了有关实验现象如下表.
| 实验操作 | 实验现象 |
| 1.用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成一个小球,在水面上无定向移
动,随之消失,溶液变红色
(B)产生气体,可在空气中燃烧,溶液变成浅红色
(C)反应不十分强烈,产生的气体可以在空气中燃
烧
(D)剧烈反应,产生可燃性气体
(E)溶液的碱性逐渐减弱
(F)生成淡黄色沉淀 |
| 2.向新制的H2S饱和溶液中滴加新制的氯水 |
| 3.钠与滴有酚酞试液的冷水反应 |
| 4.镁带与2mol.L-1的盐酸反应 |
| 5.铝条与2mol.L-1的盐酸反应 |
| 6.测定 0.1mol/L的Na2SiO3、Na3PO4、Na2SO4溶液的pH |
请你帮助该同学整理并完成实验报告
(1)实验目的:________.
(2)实验用品:仪器:①________ ②________ ③________④试管夹 ⑤镊子 ⑥小刀 ⑦玻璃片⑧砂纸 ⑨胶头滴管等
药品:钠、镁带、铝条、2mol.L-1的盐酸、新制的氯水、饱和H2S溶液、AlCl3溶液、NaOH溶液等.
(3)请你写出上述的实验操作与对应的现象
1________,2________,3________,4________,5________,6________(用A-F表示)
(4)实验结论:________.
(5)设计一个不同于本题给予的实验方案,证明金属性镁比铝强(试剂任选,简述实验原理):________.
-
(一)某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验:利用如图装置可以验证元素的非金属性的变化规律。
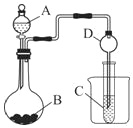
(1)图中:A装置名称是___,干燥管D的作用是___。
(2)实验室中现有药品Na2S、KMnO4、MnO2、浓盐酸,请从中选择合适药品设计实验验 证氯的非金属性大于硫,烧瓶中发生反应的离子方程式为___。
(3)若要用此装置证明酸性:HNO3>H2CO3>H2SiO3,进而证明非金属性:N>C>Si,从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
装置A、C中所选试剂分别为__(填序号);能说明酸性H2CO3>H2SiO3的实验现象是__。
(二)四种短周期元素W、X、Y、Z,原子序数依次增大,请回答下列问题。
| W | X | Y | Z |
| 结构或性质 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应 呈黄色 | 在同周期主族元素形成的简单离子中,离子半径最小,它的最高价氧化物为两性氧化物 | 最高正价与最低负价之和为零 |
(1)Z在元素周期表中位于___族。
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学反应,该元素是___(填元素符号)。
(3)①下列可作为比较X和Y金属性强弱的依据是___(填序号)。
a.自然界中的含量
b.单质与酸反应时失去的电子数
c.单质与水反应的难易程度
d.最高价氧化物对应水化物的碱性
②从原子结构的角度解释X的金属性强于Y的原因:___。
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,反应的化学方程式是__。
-
Ⅰ、某化学研究性学习小组为探究元素性质的变化规律,设计了如下实验:
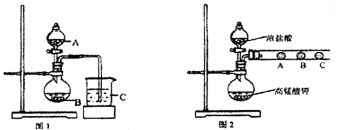
(1)甲同学欲比较N、C、Si的非金属性强弱,设计了图1所示的实验装置,其设计的依据是 ;但该装置存在缺陷,请指出 。
(2)乙同学设计了如图2装置验证元素性质递变规律。A、B、C处分别是蘸有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红纸。乙同学可能观察到的现象
A. ;B. ;C. 。
从环保角度考虑,该装置有明显不足,请指出提出改进建议 。
Ⅱ、另一化学研究性学习小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定。已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应)。
步骤一:电解精制:电解时,粗铜应与电源的 极相连。阴极上的电极反应式为 。
步骤二:电解完成后,该小组同学按以下流程对电解液进行处理:

(1)阳极泥的综合利用:稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该步反应的离子方程式: 。
残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的信息:
请根据以上信息简要解释溶解阳极泥不用王水的原因 。
(2)滤液含量的测定:以下是该小组探究滤液的一个实验流程。

则 滤液中
滤液中 的浓度为
的浓度为  ,
, 的浓度为
的浓度为  。
。










