-
有一无色透明溶液,欲确定是否含有下列离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,实验如下:
实验步骤
实验现象
①用玻璃棒蘸取少量该溶液,点在pH试纸中部
试纸变为红色
②取少量该溶液放入洁净的试管中,加入Cu片和浓硫酸,加热
有无色气体产生,气体遇空气可以变成红棕色
③取少量该溶液放入洁净的试管中,加入BaCl2溶液
有白色沉淀生成
④取③中反应后的上层清液,加入AgNO3溶液
有稳定的白色沉淀生成,且不溶于稀硝酸
⑤取少量该溶液,加入NaOH溶液
有白色沉淀生成,当NaOH过量时,沉淀部分溶解
由此判断:
(1)溶液中一定存在的离子是____________________;溶液中肯定不存在的离子是____________________。
(2)写出实验步骤②中所发生反应的离子方程式:_____________________。
(3)为了进一步确定其他离子,应该补充的实验及对应欲检验离子的名称______。
高一化学推断题中等难度题查看答案及解析
-
有一无色透明的溶液,要确定是否含有以下离子:K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如下:
实验步骤
实验现象
(1)取少量该溶液,加几滴甲基橙
溶液变红色
(2)取少量该溶液加热浓缩,加Cu片和浓H2SO4,加热
有无色气体产生,气体遇空气可以变成红棕色
(3)取少量该溶液,加BaCl2溶液
有白色沉淀生成
(4)取(3)中上层清液,加AgNO3溶液
有稳定的白色沉淀生成,且不溶于HNO3
(5)取少量该溶液,加NaOH溶液
有白色沉淀生成,当NaOH过量时沉淀部分溶解
由此判断:
(1)溶液中肯定存在的离子是___________________________________________________________,溶液中肯定不存在的离子是__________________________________________________________________。
(2)为进一步确定其他离子,应该补充的实验及对应欲检离子的名称(如为溶液反应,说明使用试剂的名称,不必写详细操作步骤)。_________________________________________________________。
高一化学填空题困难题查看答案及解析
-
有一无色透明的溶液,要确定是否含有以下离子:H+、K+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,取该溶液实验如下:
实验步骤
实验现象
(1)取少量该溶液,加几滴紫色石蕊溶液
溶液变红色
(2)取少量该溶液加热浓缩,加Cu片和浓H2SO4,加热
有无色气体产生,气体遇空气可以变成红棕色
(3)取少量该溶液,加BaCl2溶液
有白色沉淀生成
(4)取(3)中上层清液,加AgNO3溶液
有稳定的白色沉淀生成,且不溶于HNO3
(5)取少量该溶液,加NaOH溶液
有白色沉淀生成,当NaOH过量时沉淀部分溶解
由此判断:
(1)溶液中肯定存在的离子是 ,溶液中肯定不存在的离子是 。
(2)为进一步确定其他离子,应该补充的实验及对应欲检离子的名称(如为溶液反应,说明使用试剂的名称,不必写详细操作步骤)。 。
高一化学填空题困难题查看答案及解析
-
有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Ba2+、NO3-、SO42-、Cl-、CO32-,实验如下:
实验步骤
实验现象
①取少量原溶液,加入几滴酚酞试液
溶液变成红色
②取少量原溶液加热浓缩,加入Cu片和一定浓度的H2SO4
有无色气体产生,该气体遇空气变成红棕色
③取少量原溶液,加入BaCl2溶液
有白色沉淀生成
④取③中上层清液,先加入稀硝酸,再加入AgNO3溶液
有白色沉淀生成
由此判断:
(1)溶液中肯定存在的离子是________________________,肯定不存在的离子是________________,可能存在的离子是________________。
(2)实验②中生成无色气体的离子方程式是________________________________。
(3)为进一步确定可能存在的阴离子,应该补充的实验设计是__________________。
高一化学填空题困难题查看答案及解析
-
在无色透明的强酸性溶液中,下列各组离子能大量共存的是( )
A.K+、Fe2+、ClO- 、NO3- B.Na+、Ca2+、NO3-、CO32-
C.Mg2+、Al3+、Cl-、SO42+ D.Ba2+、NH4+、Cl-、HCO3-
高一化学单选题简单题查看答案及解析
-
在无色透明的酸性溶液中,能大量共存的离子组是
A. Mg2+、NH4+、NO3-、Cl-
B. Al3+、Ag+、NO3-、Fe2+
C. K+、CO32-、Cl-、Ba2+
D. Na+、OH-、SO42-、Fe3+
高一化学单选题中等难度题查看答案及解析
-
某无色透明的溶液中含有Cu2+、Mg2+、Al3+、Ba2+、H+、Ag+、SO42-、HCO3-、OH-、NO3-中的三种离子,若向其中加入石蕊试液,溶液显蓝色,则原溶液中可能存在的离子是
A. Ba2+、OH-、NO3- B. Ag+、HCO3-、NO3-
C. Mg2+、Al3+、SO42- D. Mg2+、SO42-、OH-
高一化学单选题中等难度题查看答案及解析
-
某无色透明酸性溶液中可能含有K+、Fe2+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、SO42-、NO3-中的若干种离子。某同学取50 mL的溶液进行如下实验:
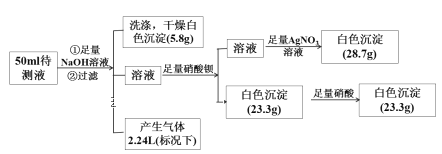
回答下列问题:
(1)原溶液中肯定存在的离子是____________ ,肯定不存在的离子是______________ 。
(2)原溶液中可能存在的离子是______________ 。
(3)原溶液中Cl-的浓度为______________ 。
(4)原溶液中c(K+)范围:_______________ (若不存在,说明理由)
高一化学推断题困难题查看答案及解析
-
有一透明溶液,欲确定是否含有下列离子:K+、Al3+、Ba2+、NO3-、SO42-、Cl-、HCO3-,实验如下:
实验步骤
实验现象
(1)取pH试纸检验
溶液呈酸性
(2)取少量该溶液,加入Cu片和稀硫酸,加热
有无色气体产生,气体遇空气可以变成红棕色
(3)取少量该溶液,加入BaCl2溶液
有白色沉淀生成
(4)取(3)中反应后的上层清液,加入AgNO3溶液
有白色沉淀生成,且不溶于稀硝酸
(5)取少量该溶液,加入NaOH溶液
有白色沉淀生成,当NaOH过量时,沉淀溶解
由此判断:
(1)溶液中一定存在的离子有____________;溶液中肯定不存在的离子有__________;不能确定的离子有______________。
(2)写出上述实验步骤(2)中反应的离子方程式_______________________________。
(3)写出上述实验步骤(5)中沉淀溶解对应的反应的离子方程式_________________。
高一化学简答题中等难度题查看答案及解析
-
在无色透明的酸性溶液中,下列离子能大量共存的是
A. K+、Cu2+、NO3-、SO42- B. CO32-、Na+、Cl-、SO42-
C. Al3+、Cl-、NO3-、Mg2+ D. H+、Ba2+、NO3-、SO42-
高一化学单选题简单题查看答案及解析