-
由质量均为100g的铁片、铜片和足量CuSO4溶液组成原电池装置,经过一段时间后,两电极的质量差变为12g,则下列说法正确的是( )
A. 铁片溶解了12g B. 导线中通过了0.2mol电子
C. 铜片上析出了6gCu D. 铜片溶解了6.4g
高二化学单选题简单题查看答案及解析
-
在用Zn、Cu片和CuSO4溶液组成的原电池装置中,经过一段时间工作后,下列说法中正确的是
A.锌片是正极,铜片质量不变 B.电流方向是从锌片流向铜片
C.锌片是负极,铜片质量不变 D.锌片是负极,铜片质量增加
高二化学选择题简单题查看答案及解析
-
如图是一个铜锌双液原电池装置图,下列说法正确的是
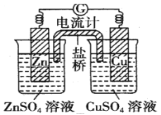
A. 盐桥中的阴离子向CuSO4溶液中移动
B. 盐桥的作用之一是平衡电荷
C. 铜片作电池的负极
D. 电子从锌电极经溶液流向铜电极
高二化学单选题简单题查看答案及解析
-
如图,铁片、铜片和CuSO4溶液可以构成原电池或电解池,下列说法正确的是( )
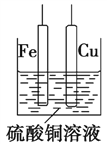
A. 构成原电池时,Cu极反应式为Cu-2e-=Cu2+
B. 构成电解池时,Cu极质量可能减少也可能增加
C. 构成电解池时,Fe极质量一定减少
D. 构成的原电池或电解池在工作时的反应原理一定不同
高二化学null困难题查看答案及解析
-
以铅蓄电池为电源,石墨为电极电解CuSO4溶液,装置如下图。若一段时间后Y电极上有3.2 g红色物质析出,停止电解。下列说法正确的是
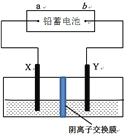
A. a为铅蓄电池的负极
B. 电解结束时,左侧溶液质量增重4g
C. 铅蓄电池工作时正极电极反应式为:PbSO4+2e-=Pb+SO42-
D. 电解过程中,铅蓄电池的负极增重15.15g
高二化学单选题困难题查看答案及解析
-
利用如图装置可以测定铜锌原电池工作时转移电子的物质的量,假设量筒的量程足够大,锌片和铜片中无杂质,气体积已转换为标准状况。下列说法正确的是

A. a电极的电极材料是铜
B. 如果将稀硫酸换为CuSO4溶液,则不能达到实验目的
C. 锌与稀硫酸反应时放出的热量对实验测定不产生影响
D. 若量筒中收集到aLH2,则电解质溶液中通过了a/11.2mol电子
高二化学单选题中等难度题查看答案及解析
-
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
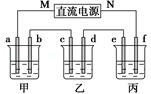
接通电源,经过一段时间后,乙中c电极质量增加16g.据此回答问题:
(1)电源的N端为 极;
(2)电极b上发生的电极反应为 ;
(3)列式计算电极a上生成的气体在标准状况下的体积: L;
(4)丙中K2SO4质量分数将变为 .
高二化学填空题困难题查看答案及解析
-
(12分)下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极。
(1)接通电源,经过一段时间后,测得丙中K2SO4溶液质量减少4.5g,乙中c电极质量增加。
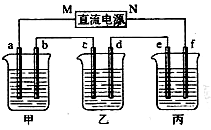
据此回答
问题:①电源的N端为________极;(2分)
②电极b上发生的电极反应为________;(2分)
③列式计算电极b上生成的气体在标准状态下的体积:________L;(2分)
④电极c的质量变化是________g;
⑤电解前后各溶液的pH值是否发生变化(填增大,减小,不变)
甲溶液________;
乙溶液________;
丙溶液;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
________,原因 ________
高二化学填空题中等难度题查看答案及解析
-
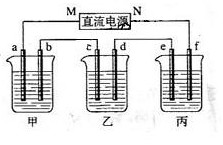
(6分)下图所示装置中,甲、乙、丙 三个烧杯依次分别盛放100g 5.00%的NaOH溶液、
足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极
接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①列式计算电极b上生成的气体在标准状态下的体积是多少?
②电极c的质量变化多少克?
高二化学计算题简单题查看答案及解析
-
右图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题:
①电源的N端为______极;
②电极b上发生的电极反应为______;
③列式计算电极b上生成的气体在标准状况下的体积:______
④电极c的质量变化是______g;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:
甲溶液______;
乙溶液______;
丙溶液______;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?______.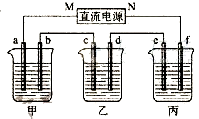
高二化学解答题中等难度题查看答案及解析