-
下面是某学生实验的一次数据,请完成计算
坩埚质量
坩埚与晶体总质量
加热后坩埚与固体总质量
11.721g
22.692g
18.631g
X=__________________;(精确到0.01)
实验相对误差是_________________。(保留小数点后一位)
高二化学填空题简单题查看答案及解析
-
化学实验是研究物质性质的基础。
(1)下列有关实验操作或测量数据合理的是________(填序号)。
a.用铁坩埚加热CuSO4·5H2O晶体测定结晶水质量分数
b.用干燥的pH试纸测定浓硫酸的pH
c.用规格为20 mL的量筒,量取16.8 mL的Na2CO3溶液
(2)某废水样品中含有一定量的Na+、CO32-、SO32-,某研究小组欲测定其中SO32-的浓度。
实验方案:
ⅰ.用烧杯盛取废水适量,加少量活性炭,除去废水中的杂质;过滤,取滤液;
ⅱ.精确量取20.00 mL过滤后废水试样,选择使用紫色的0.1 mol/L KMnO4(H2SO4酸化)溶液进行滴定;
ⅲ.记录数据,计算。
①下列滴定方式中,最合理的是(夹持部已分略去)______(填字母序号)。

②滴定过程中,有关反应的离子方程式是__________________________________。
(3)某同学制备Fe(OH)3胶体:用洁净的烧杯取适量蒸馏水加热至沸腾,向烧杯中滴加 1 mol/L的FeCl3溶液,并不断用玻璃棒搅拌,结果溶液变浑浊。该同学制备胶体失败的原因是 ,你认为成功制得Fe(OH)3胶体的特征现象是_________。
(4)用下图装置进行CO2性质的有关实验。

试剂瓶B中盛有饱和NaHCO3溶液,其目的是:
_________________________________________。
②反应过程中,E中澄清石灰水变浑浊,E中的混合体系中除存在电离平衡、水解平衡外,还存在溶解平衡,用方程式表示该溶解平衡关系:
____________________ ___________。
高二化学实验题极难题查看答案及解析
-
某校化学研究性学习小组设计如下实验方案,测定放置已久的小苏打样品中纯碱的质量分数。
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。实验中加热至恒重的目的是_________________。
(2)方案二:按下图装置进行实验。并回答以下问题:
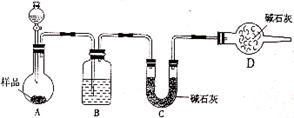
①分液漏斗中应该装___________(填“盐酸”或“稀硫酸”),D装置的作用是_________________________________;
②实验中除称量样品质量外,还需称________装置(用字母表示)前后质量的变化。
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液,过滤洗涤,干燥沉淀,称量固体质量,计算:
①过滤操作中,除了烧杯、漏斗外还用到的玻璃仪器有_____________;
②若加入试剂改为氢氧化钡,已知称得样品9.5g,干燥后的沉淀质量为19.7g,则样品中碳酸钠的质量分数为____________(保留一位小数)。
高二化学实验题困难题查看答案及解析
-
下列关于测定胆矾晶体里结晶水含量的实验操作,会引起测定结果偏高的是
A.加热时,强热蒸干,硫酸铜表面出现黑色固体
B.坩埚内附着有少量氯化钠固体
C.加热时,胆矾晶体未完全变白即停止加热
D.加热胆矾晶体后在空气中冷却称量
高二化学选择题简单题查看答案及解析
-
测定硫酸铜晶体中含结晶水含量的实验,造成结果偏高的原因是( )
①坩埚用水洗后没有烘干;②加热时有少量晶体溅出;③把加热得到的白色粉末放在空气中冷却、称量;④加热完了粉末中有少量的黑色固体。
A、①②③ B、 ①② C、 ②③ D、 ①②④
高二化学单选题中等难度题查看答案及解析
-
测定硫酸铜晶体中结晶水含量的实验,下列四项中造成结果偏高的原因有
①坩埚用水洗后没有烘干②加热时有少量晶体溅出③把加热得到的白色粉末放在空气中冷却、称量④加热后粉末中有少量的黑色固体
A.①②③ B.①② C.②③ D.①②④
高二化学选择题简单题查看答案及解析
-
将固体MnC2O4·2H2O放在坩埚里加热,固体质量随温度变化的数据如下表:
温度(℃)
25
50
75
100
214
280
固体质量(g)
17.9
17.9
16.0
14.3
14.3
7.10
下列说法错误的是
A.25~50 ℃,MnC2O4·2H2O未发生变化
B.75 ℃时,MnC2O4·2H2O部分失去结晶水
C.100℃时,坩埚内固体均为MnC2O4
D.280℃时,坩埚内固体为混合物
高二化学选择题中等难度题查看答案及解析
-
硫酸铜晶体在不同温度下可失去部分或全部结晶水甚至分解成氧化物。某学生在不同温度下给8.000 g硫酸铜晶体加热(温度逐渐升高),实验结果记录如下:
实验次序
温度(℃)
冷却后剩余固体的质量(g)
1
102
6.848
2
113
5.696
3
258
5.120
4
570
2.560
(1)第1次实验后,试样晶体失去结晶水的质量是_____ g。
(2)通过计算确定第二次实验后固体物质的化学式为______________。
(3)第四次实验后,剩余固体为一种黑色粉末(假设为纯净物),将该黑色粉末溶解于稀硫酸中,至少需要0.50mol/L的稀硫酸多少毫升?(写出计算过程)
高二化学实验题中等难度题查看答案及解析
-
硫酸铜晶体在不同温度下可失去部分或全部结晶水甚至分解成氧化物。某学生在不同温度下给8.000 g硫酸铜晶体加热(温度逐渐升高),实验结果记录如下:
实验次序
温度(℃)
冷却后剩余固体的质量(g)
1
102
6.848
2
113
5.696
3
258
5.120
4
570
2.560
(1)第1次实验后,试样晶体失去结晶水的质量是________g。
(2)通过计算确定第二次实验后固体物质的化学式为______________。
(3)第四次实验后,剩余固体为一种黑色粉末(假设为纯净物),将该黑色粉末溶解于稀硫酸中,至少需要0.50mol/L的稀硫酸多少毫升?(写出计算过程)
高二化学计算题困难题查看答案及解析
-
测定硫酸铜晶体(CuSO4·xH2O)里结晶水的含量,实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.001g为止 ⑦根据实验数据计算硫酸铜结晶水的含量。请回答下列问题:
(1)现有坩埚、坩埚钳、三脚架、泥三角、玻璃棒、干燥器、药匙、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是____________________。
(2)实验步骤⑥的目的是_____________________________。
(3)某学生实验后得到如下数据:
名称
质量
第一次
第二次
瓷坩锅质量(m0)
14.520
14.670
瓷坩埚+硫酸铜晶体的质量(m1)
17.020
18.358
瓷坩埚+无水硫酸铜粉末的质量(m2)
16.070
17.004
硫酸铜晶体的质量(m1—m0)
无水硫酸铜粉末的质量(m2—m0)
结晶水的质量(m1—m2)
用表格数据计算x值;第一次:5.4,第二次为:______平均值:___________。
实验误差=_________________(保留一位小数)【实验误差=(实验值-理论值)/理论值】
该学生产生实验误差的原因可能是(填入选项的编号):__________________。
A.被测样品中含有加热不挥发的杂质 B.被测样品中含有加热易挥发的杂质
C.实验前被测样品已有部分失水 D.加热前所用的坩埚未完全干燥
高二化学实验题中等难度题查看答案及解析