-
某化学兴趣小组利用饱和氯水与石灰石的反应,制取较浓的HClO溶液,并对所得溶液中的部分阴离子进行检验.
(1)步骤1中产生气体反应的离子方程式是______,过滤的目的是______.实验操作 实验现象 步骤1 在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,过滤,将滤液分为若干份 有少量气泡产生,溶液的黄绿色褪去 步骤2 将第一份滤液与稀盐酸混合 产生大量气泡 步骤3 将第二份滤液加热 溶液变浑浊,且有大量无色气体产生
(2)步骤2、步骤3的实验目的都是______,为达到该实验目的,还可以采取的方法是______.
(3)步骤3中反应的离子方程式是:______ CaCO3↓+H2O+CO2↑高三化学解答题中等难度题查看答案及解析
-
(16分)某化学兴趣小组利用饱和氯水与石灰石的反应,制取较浓的HClO溶液,并对所得溶液中的部分阴离子进行检验。
实验操作
实验现象
步骤1
在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,过滤,将滤液分为若干份
有少量气泡产生,溶液的黄绿色褪去
步骤2
将第一份滤液与稀盐酸混合
产生大量气泡
步骤3
将第二份滤液加热
溶液变浑浊,且有大量无色气体产生
⑴ 步骤1中发生反应的离子方程式是____________________________________,
过滤的目的是____________________________________________________。
⑵ 步骤2、步骤3的实验目的都是_____________________________,为达到该实验目的,还可以采取的方法是______________________________________。
⑶步骤3中反应的离子方程式是:________ 。
(4)请你设计一个简单的实验方案,证明步骤1所得滤液中的HClO浓度比饱和氯水中HClO浓度大:_____________________________________________________。
高三化学实验题中等难度题查看答案及解析
-
饱和氯水与石灰石反应是制取较浓HClO溶液的方法之一。某兴趣小组进行了如下实验探究。
实验一:定性研究。
①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水(如图所示),充分反应,有少量气泡产生,溶液浅黄绿色退去;
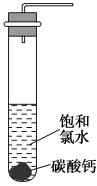
②过滤,将滤液滴在有色布条上,发现滤液比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
第三份滤液加热,看到滤液变浑浊且有大量无色气体产生。经检测,上述实验中产生的无色气体均为CO2。
请回答:
(1)反应后所得的溶液漂白性比氯水强的原因是 。
(2)依据上述实验可推知:滤液中的溶质除CaCl2、HClO外,还有 (填写溶质的化学式)。
实验二:定量研究。
在圆底烧瓶底部,用一塑料网包住块状石灰石(过量)与150 mL饱和氯水反应,按下图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,将装置密封后再加热,煮沸烧瓶中的液体,量筒中的气体不再增加时停止实验。

请回答:
(3)实验结束后检测到量筒中收集到的气体除CO2外还有O2,请写出Ⅰ中产生O2的化学反应方程式 。
(4)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,请你对装置Ⅲ进行改进(水槽中仍为水),最简单的方法是 。
高三化学实验题困难题查看答案及解析
-
饱和氯水与石灰石反应是制取较浓HClO溶液的方法之一。某兴趣小组进行了如下实验探究①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水(如下图所示),充分反应,有少量气泡产生,溶液浅黄绿色褪去;②过滤,将滤液滴在有色布条上,发现滤液比氯水的漂白性更强;③为了确定反应产物,将滤液分为三份,分别进行以下实验:第一份与石灰水混合,立即产生大量白色沉淀;第二份与稀盐酸混合,立即产生大量无色气体;第三份滤液加热,看到滤液变浑浊且有大量无色气体产生。经检测,上述实验中产生的无色气体均为CO2 。依据上述实验可推知:滤液中的溶质除CaCl2、HClO外,还有
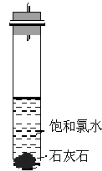
A.Ca (ClO)2 B.CaCO3 C.Ca(HCO3)2 D.CaO
高三化学选择题中等难度题查看答案及解析
-
某化学兴趣小组制取氯酸钾和氯水并进行探究实验。
【实验一】 制取氯酸钾和氯水
利用如图所示的实验装置进行实验。(部分夹持装置已省略)

(1)仪器a的名称是________,写出装置A中发生反应的离子方程式:________________________________________________。
装置B中的现象为__________________________________。
(2)为了使Cl2在装置C中被KOH溶液充分吸收,装置A中滴加浓盐酸的速率宜________(填“快”或“慢”)。
(3)有同学认为对调装置B和装置C的位置不利于提高装置C中氯酸钾的产率,你是否认同该观点并说明理由:____________________________。
【实验二】 测定饱和氯水中氯元素的含量
实验步骤如下:
①从装置B中量取25.00 mL氯水于锥形瓶中,向其中慢慢地充入SO2,溶液黄绿色完全消失后再充入一段时间的SO2。
②向锥形瓶中加入足量BaCO3粉末,过滤,洗涤,将滤液导入滴定池中。
③取0.01 mol·L-1的AgNO3标准溶液装入棕色滴定管,用电势滴定法(在化学计量点附近,溶液的电极电势有最大的变化)测定氯元素的含量。通过测得的电动势(E)可知溶液中c(Cl-)的变化,部分数据如下表:
V(AgNO3溶液)/mL
35.00
39.00
39.80
39.98
40.00
40.02
41.00
43.00
45.00
E/mV
-225
-200
-150
-100
32.5
165
245
270
295
(4)量取25.00 mL氯水所用的仪器是____________________________________;
操作②的目的是____________________________________________________。
(5)测定氯元素含量的过程中,使用棕色滴定管的原因是____________________。
(6)达到该次滴定终点时,消耗AgNO3溶液的体积为________ mL。
高三化学实验题中等难度题查看答案及解析
-
某中学化学兴趣小组想制取饱和氯水,并进行氯水的性质实验。他们使用如图装置制取较多量的饱和氯水,请回答:
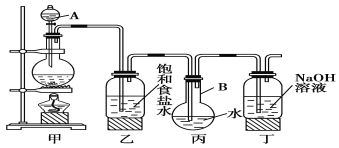
(1)写出仪器的名称:A_________。
(2)写出丙、丁装置中发生反应的离子方程式:丙_________,丁_______。
(3)有同学提出如下改进建议:
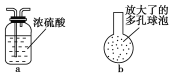
①在乙和丙之间增加上图中的a装置,你认为有无必要___ (填“有”或“无”)。
②在丙的长导管下口处,接上图中的b装置,可以提高氯气的吸收效果。原因是_______。
(4)用制得的氯水分别进行下列实验:①滴入碳酸钠溶液中,有气体生成,说明氯水中发生反应的粒子是____;②滴入AgNO3溶液中,发生反应的离子方程式是_____。
(5)用滴管将制得的饱和氯水慢慢滴入含酚酞的NaOH稀溶液中。当滴到最后一滴时红色突然退去。产生上述现象的原因可能有两种(简要文字说明):①是由于____________;②是由于________。
高三化学实验题简单题查看答案及解析
-
碳铵是一种较常使用的化肥,它在常温下易分解。某化学兴趣小组对碳铵的成分存在疑问,进行了如下探究。
【定性实验】检验溶液中的阴、阳离子。
取少量固体放入试管中,加入盐酸,把生成的气体通入澄清石灰水中,有白色沉淀生成。再另取少量碳铵放入试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验生成的气体,石蕊试纸变蓝色。
(1)根据实验现象,推测碳铵中所含有阴离子可能是 和 。
(2)据实验现象,碳铵与足量NaOH溶液加热反应的离子方程式可能是 。
【定量实验】测定碳铵中C元素和N元素质量比。
该兴趣小组准确称取ag碳铵,加热使之分解,并把产物通入碱石灰中,如下图所示。
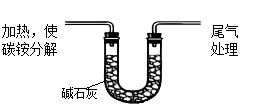
(1)碳铵固体应放在 中进行加热。
A.试管 B.蒸发皿 C.烧瓶 D.坩埚
(2)从安全的角度考虑,尾气处理的装置可以选用 。

A B C D
(3)若灼烧后没有固体残余,称量U形管在实验前后的质量差为bg。由此测得N元素的质量是 g。
(4)为了测定碳铵中碳元素的质量,他们设计的实验方案是将ag碳铵完全溶解于水,加入过量BaCl2,然后测定生成沉淀质量。请你评价该方案是否合理。 (填“合理”“不合理”),理由是 。
高三化学实验题极难题查看答案及解析
-
某化学兴趣小组同学展开对漂白剂亚氯酸钠
的研究.
实验I:制取
晶体
己知:
饱和溶液在温度低于
时析出晶体是
,高于
时析出晶体是
,高于
时
分解成
和
。利用如图所示装置进行实验.
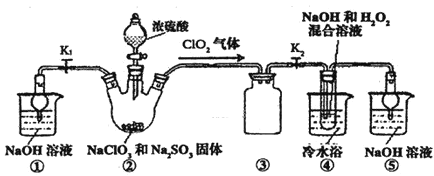
装置
的作用是 ______ ;装置
的作用是 ______ .
装置
中产生
的还原剂是 ______ ;装置
中制备NaClO2的化学方程式为 ______ .
从装置
反应后的溶液获得
晶体的操作步骤为:
减压,
蒸发结晶;
趁热过滤;
______ ;
低于
干燥,得到成品.
实验Ⅱ:测定某亚氯酸钠样品的纯度.
设计如下实验方案,并进行实验:
准确称取所得亚氯酸钠样品mg于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应
已知:
将所得混合液配成250mL待测溶液.
移取
待测溶液于锥形瓶中,加几滴淀粉溶液,用c
标准液滴定,至滴定终点。重复2次,测得平均值为V
已知:
达到滴定终点时的现象为 ______ .
该样品中
的质量分数为 ______
用含m、c、V的代数式表示
.
在滴定操作正确无误的情况下,此实验测得结果偏高,原因用离子方程式表示为 ______ .
高三化学实验题困难题查看答案及解析
-
化学兴趣小组在实验室进行“海带提碘”的实验过程如图:

(1)操作①的名称是_____,操作②的主要仪器是_____;氧化步骤的离子方程式是_____。
(2)探究异常:取样检验时,部分同学没有观察到溶液变蓝色。他们假设原因可能是加入的氯水过量,氧化了①I2;②淀粉;③I2 和淀粉。他们在没有变蓝色的溶液中,滴加_____(选填“四氯化碳”“碘水”“淀粉溶液”)后,若出现_____现象,即可证明假设①正确,同时排除假设②③.能同时排除假设②③的原因是_____。
(3)查阅资料:Cl2 可氧化 I2,反应的化学方程式为_____Cl2+_____I2+_____ H2O→_____ HIO3+_____ HCl.配平上述方程式,并标出电子转移的方向和数目_______。
(4)探究氧化性:在盛有 FeCl3 溶液的试管中,滴入几滴 KI 溶液,将反应后的溶液均匀倒入两支试管,试管 a 中加入 1 mL 苯振荡静置,出现______(填实验现象),证明有 I2存在;试管b 中滴入 KSCN 溶液,溶液显血红色,证明有_____存在。
(5)比较氧化性:综合上述实验,可以得出的结论是氧化性:Cl2>FeCl3,理由是_____。
高三化学实验题中等难度题查看答案及解析
-
可用作食品添加剂。
能发生以下反应:
淡黄色
某化学兴趣小组进行以下探究。回答有关问题:
制取
反应原理:
用如图所示装置进行实验。
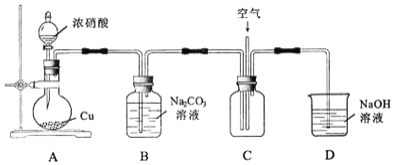
铜与浓硝酸反应的离子方程式为______。
实验过程中,需控制B中溶液的
,否则产率会下降,理由是______。
往C中通入空气的目的是______
用化学方程式表示
。
反应结束后,B中溶液经蒸发浓缩、冷却结品、______等操作,可得到粗产品晶体和母液。
测定粗产品中
的含量
称取mg粗产品,溶解后稀释至
取出
溶液,用
酸性溶液平行滴定三次,平均消耗的体积为VmL。
已知:
稀释溶液时,需使用的玻璃仪器除烧杯、玻璃棒外,还有______
填标号
。
A.容量瓶
量筒
胶头滴管
锥形瓶
当观察到______时,滴定达到终点。
粗产品中
的质量分数为______
用代数式表示
。
设计实验方案证明母液中含有
______
限选用的试剂:硝酸、硝酸银溶液、硝酸钡溶液、氯化钡溶液
。
高三化学实验题中等难度题查看答案及解析