-
电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
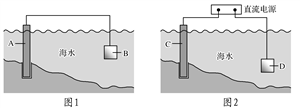
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择________(填字母序号)。
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:___________________________。
(2)图2中,钢闸门C作________极。若用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应式为_____________________________________,检测该电极反应产物的方法是_________________________________________。
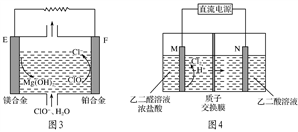
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的________极(填“正”或“负”)。F电极上的电极反应式为_______________________________________________________________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因:___________________________________________________。
(4)乙醛酸( )是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
①N电极上的电极反应式为_____________________________________。
②若有2molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为________ mol。
-
电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。

(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择__________(填字母序号)
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因_______________。

(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图2为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的_____________极(填“正”或“负”)。F电极上的电极反应式为_____________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因____________。
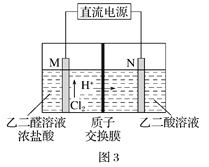
(3)乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图3所示,该装置中阴、阳两极为惰性电极,两级室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
①N电极上的电极反应式为______________。
②若有2molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为________________mol。
-
电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。
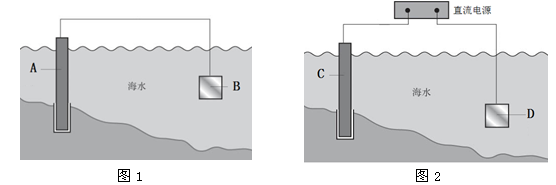
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择________(填字母序号)。
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:__________________________。
(2)图2中,钢闸门C做_____极。用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应式为______________________,检测该电极反应产物的方法是_______________________。
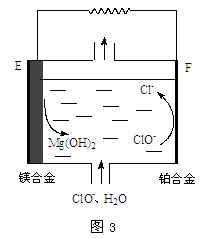
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的极________(填“正”或“负”)。F电极上的电极反应式为___________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因_______。
-
(13分)电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。

(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择________(填字母序号)。
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:__________________________。
(2)图2中,钢闸门C做_____极。用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应式为______________________,检测该电极反应产物的方法是_______________________。
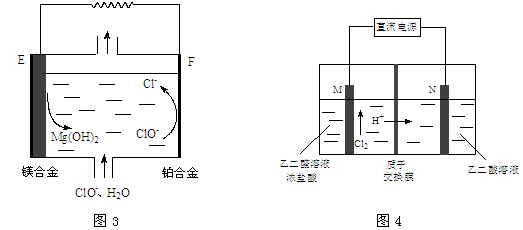
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的极________(填“正”或“负”)。F电极上的电极反应式为___________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因_______。
(4)乙醛酸(HOOC-CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两级室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。
①N电极上的电极反应式为_________________。
②若有2molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为________mol。
-
(17分)电化学原理在金属腐蚀、能量转换、物质合成等方面应用广泛。

(1)通常可用图l、图2所示的两种方式减缓海水埘钢闸门A的腐蚀,则图l中材料B通常选择_________(填字母序号),图2 中材料C最好选择_________(填字母序号)。
a.钠块 b.铜块 c.锌块 d.石墨

则图2中C上发生的主要电极反应式为___________________。
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①D为该燃料电池的________极(填“正”或“负”)。E电极上的电极反应式为_______。
②镁燃料电池负极容易发生自腐蚀使负极利用率降低,该过程中产生的气体a为_______(填化学式)。
(3)乙醇酸(HOOC—CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸。
①乙二醛(OHC—CHO)与M电极的气体产物反应生成乙醛酸,则反应的化学方程式为____________。
②该电解装置工作中若有0.5molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为____________mol。
-
下列关于金属腐蚀与防护的说法不正确的是
A.金属腐蚀就是金属失去电子被氧化的过程。
B.铝制品的耐腐蚀性强,说明铝的化学性质不活泼
C.将海水中钢铁闸门与电源的负极相连,可防止闸门被腐蚀
D.铁在NaOH和NaNO2的混合液中发蓝、发黑,使铁表面生成一层致密的氧化膜Fe3O4,防止钢铁腐蚀,其反应为:9Fe+8H2O+4NaNO2=3Fe3O4+4NH3↑+4NaOH
-
电化学原理具有极为广泛的应用,请回答下列问题:
(1)电镀是防止金属腐蚀的重要方法,铁制品表面上镀铜的装置示意图如图所示:
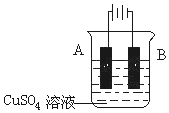
①A电极对应的金属是__________(写元素名称)。
②电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为a g,则电镀时电路中通过的电子为_________mol。
(2)工业上常用电解熔融氯化镁获得金属镁,若电解槽中有水分,则生成的MgOHCl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率,写出生成MgO 的化学方程式_________________。
(3)“镁-次氯酸盐”燃料电池的装置如图所示:
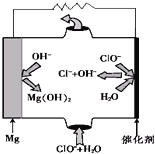
①该电池的正极反应式为__________________。
②若用该电池为电源,用惰性电极电解CuSO4溶液,电解一段时间后,向电解液中加入0.1mol Cu2(OH)2CO3,恰好使溶液恢复到电解前的浓度和pH。电解过程产生的气体体积(在标准状况下)为____________。
-
根据下图,有关金属的腐蚀与防护的叙述正确的是
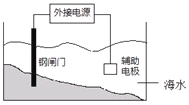
A.钢闸门含铁量高,无需外接电源保护
B.该装置的原理是“牺牲阳极的阴极保护法”
C.将钢闸门与直流电源的负极相连可防止其被腐蚀
D.辅助电极最好接锌质材料的电极
-
化学已渗透到人类生活的各个方面。下列说法不正确的是( )
A.阿司匹林具有解热镇痛作用
B.可以用Si3N4、Al2O3制作高温结构陶瓷制品
C.在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀
D.禁止使用四乙基铅作汽油抗爆震剂可减少汽车尾气污染
-
化学已渗透到人类生活的各个方面.下列说法不正确的是( )
A.阿司匹林具有解热镇痛作用
B.可以用Si3N4、Al2O3制作高温结构陶瓷制品
C.在入海口的钢铁闸门上装一定数量的铜块可防止闸门被腐蚀
D.禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染


)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸。











