(1)试在方框中填入合适的化合物的结构简式:

(2)写出下列化学反应方程式:
B-→C______
高三化学解答题中等难度题

高三化学解答题中等难度题

高三化学解答题中等难度题查看答案及解析
聚四氟乙烯的耐热性和化学稳定性都超过其他塑料,甚至在王水中也不发生变化,故号称“塑料王”,在工业上有着广泛的用途,按照下列所示的合成路线:
(1)试在方框中填入合适的化合物的结构简式:
 (2)写出下列化学反应方程式:
(2)写出下列化学反应方程式:
B→C______________________________________________。
C→D______________________________________________。
高三化学填空题简单题查看答案及解析
聚四氟乙烯的耐热性和化学稳定性都超过了一般塑料,甚至在王水中也不变化,故号称“塑料王”,在工业上有着广泛的用途。其合成路线如图所示:

(1)在方框中填入合适的有机物的结构简式。
(2)写出下列化学反应方程式,并指出反应类型。
B―→C________________________________________________________,
反应类型是____________;
C―→D_____________________________________________________________,
反应类型是____________。
高三化学填空题简单题查看答案及解析
I.氟乙烯在耐热性和化学稳定性上都超过了其他塑料,号称“塑料之王”,可用于制造
飞机、导弹的无油轴承,密封填料,人造血管,滑雪板,不粘锅等。其合成路线如下
图所示:

写出下列化学反应方程式。
B→C: ;
C→D: 。
Ⅱ.牛奶放置时间长了会变酸,这是因为牛奶中含有不少乳糖,在微生物的作用下乳糖分
解而变成乳酸,乳酸的结构简式为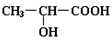
(1)乳酸分子中含有________和_________两种官能团(写名称);
(2)已知有机物中若含有相同的官能团,则化学性质相似。完成下列问题:
乳酸与足量金属钠反应的化学方程式为___________________。
高三化学推断题困难题查看答案及解析
聚四氟乙烯的耐热性和化学稳定性超过其他塑料,被称为“塑料王”。其合成路线如下:
三氯甲烷HF,SbCl3二氟一氯甲烷△四氟乙烯聚四氟乙烯
下列说法中,不正确的是( )
A.“塑料王”不能使酸性高锰酸钾溶液褪色
B.三氯甲烷(CHCl3)不可以用甲烷与氯气的取代反应来制取
C.四氟乙烯(CF2===CF2)中所有的原子都在同一个平面上
D.二氟一氯甲烷(CHClF2)中所有原子最外层都达到了8电子稳定结构
高三化学选择题中等难度题查看答案及解析
曾传出“塑料王”聚四氟乙烯材料在高温使用时会产生癌物,“塑料王”的耐热性和化学稳定性超过其他塑料。合成路线如下:

下列说法中,不正确的是 ( )
A.“塑料王”与有机玻璃都为合成高分子材料
B.二氟一氯甲烷是一种氟利昂,分子中只含共价键
C.四氟乙烯(CF2=CF2)中所有的原子都在同一个平面上
D.聚四氟乙烯中碳原子共直线形成链状分子
高三化学选择题简单题查看答案及解析
聚四氟乙烯的耐热性和化学稳定性超过其他塑料,被称为“塑料王”。其合成路线如下:
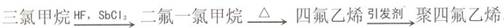
下列说法中,不正确的是 ( )
A.“塑料王”不能使酸性高锰酸钾溶液褪色
B.三氯甲炕(CHCl3)可以用甲院与氯气的取代反应来制取
C.四氟乙烯 (CF2=CF2)中所有的原子都在同一个平面上
D.二氟一氯甲院 (CHClF2)中所有原子最外层都达到了8电子稳定结构
高三化学单选题中等难度题查看答案及解析
CO、CO2是重要的工业原料,在工业上有着广泛的用途.

(1)已知相关反应的能量变化如图1所示.
则用CH4(g)和H2O(g)反应制得H2(g)和CO(g)的热化学反应方程为 .
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:CO(g)+2H2(g)⇌CH3OH(g)△H1<0,
CO在不同温度下的平衡转化率(α)与压强(p)的关系如图2所示
①a、b两点H2的反应速率:v(a) v(b)(填“>”、“<”、“=”)
②相同压强下,CO的转化率先达到0.5的是 (填“T1”或“T2 ),原因是 .
③在T1点温度下,下列叙述不能说明上述反应能达到化学平衡状态的是 (填字母)
a.H2的消耗速率是CH3OH生成速率的2倍
b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变
d.CO和CH3OH的物质的量之和保持不变
④计算图2中a点的平衡常数KP= (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(3)氨气和CO2在一定条件下可合成尿素,其反应为:2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g)
合成塔中氨碳比[]与CO2转化率[α(CO2)]的关系如图3所示.则
应控制在4.0的理由是 .
高三化学填空题简单题查看答案及解析
乙苯是一种用途广泛的有机原料,可制备多种化工产品。
(一)制备苯乙烯(原理如反应I所示):
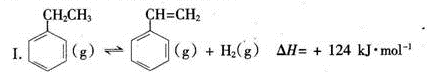
(1)部分化学键的键能如下表所示:

根据反应I的能量变化,计算x= ____。
(2)工业上,在恒压设备中进行反应I时,常在乙苯蒸气中通入一定量的水蒸气。用化学一平衡理论解释通入水蒸气的原因为____ 。
(3)从体系自由能变化的角度分析,反应I在____(填“高温”或“低温”)下有利于其自发进行。
(二)制备α-氯乙基苯(原理如反应II所示):
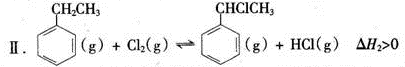
(4)T℃时,向10 L恒容密闭容器中充人2mol乙苯(g)和2 mol Cl2(g)发生反应Ⅱ,5 min时达到平衡,乙苯和Cl2、α-氯乙基苯和HC1的物质的量浓度(c)随时间(t)变化的曲线如图l所示:
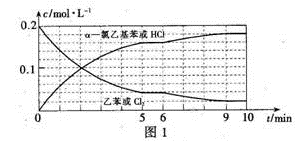
①0—5 min内,以HC1表示的该反应速率v(HCl)=____ 。
②T℃时,该反应的平衡常数K=____ 。
③6 min时,改变的外界条件为________。
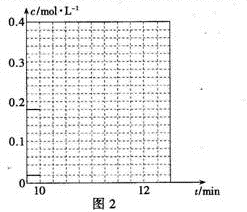
④10 min时,保持其他条件不变,再向容器中充人1moI乙苯、1 mol Cl2、1 mol α-氯乙基苯和l mol HCl,12 min时达到新平衡。在图2中画出10-12 min,Cl2和HC1的浓度变化曲线(曲线上标明Cl2和HC1);0—5 min和0—12 min时间段,Cl2的转化率分别用α1、α2表示,则αl α2(填“>”、“<”或“=”)。
高三化学填空题困难题查看答案及解析
乙苯是一种用途广泛的有机原料,可制备多种化工产品。
(一)制备苯乙烯(原理如反应I所示):
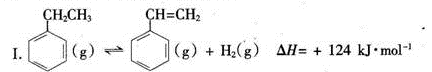
(1)部分化学键的键能如下表所示:

根据反应I的能量变化,计算x= ____。
(2)工业上,在恒压设备中进行反应I时,常在乙苯蒸气中通入一定量的水蒸气。用化学平衡理论解释通入水蒸气的原因为____ 。
(3)从体系自由能变化的角度分析,反应I在____(填“高温”或“低温”)下有利于其自发进行。
(二)制备α-氯乙基苯(原理如反应II所示):

(4)T℃时,向10 L恒容密闭容器中充人2mol乙苯(g)和2 mol Cl2(g)发生反应Ⅱ,5 min时达到平衡,乙苯和Cl2、α-氯乙基苯和HCl的物质的量浓度(c)随时间(t)变化的曲线如图l所示:

①0—5 min内,以HCl表示的该反应速率v(HCl)=_____________。
②T℃时,该反应的平衡常数K=_____________。
③6 min时,改变的外界条件为_____________。
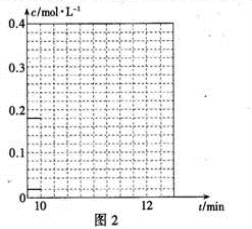
④10 min时,保持其他条件不变,再向容器中充人1moI乙苯、1 mol Cl2、1 mol α-氯乙基苯和l mol HCl,12 min时达到新平衡。在图2中画出10-12 min,Cl2和HCl的浓度变化曲线(曲线上标明Cl2和HC1);0—5 min和0—12 min时间段,Cl2的转化率分别用α1、α2表示,则αl α2(填“>”、“<”或“=”)。
高三化学填空题简单题查看答案及解析