-
某无色工业废水中可能含有Na+、Mg2+、Al3+、Cu2+、Cl-、SO42-中的几种离子。
a.取10 mL该废水于试管中,加入足量的Ba(NO3)2溶液和稀硝酸,产生白色沉淀,充分反应后过滤,向滤液中加入AgNO3溶液无沉淀产生。
b.另取10 mL该废水于试管中,滴加NaOH溶液先产生白色沉淀,后部分沉淀溶解,生成沉淀的物质的量随加入NaOH的物质的量关系如图所示。
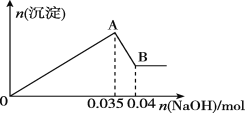
根据上述实验回答下列问题:
(1)该废水中一定不含有的离子有______________(填离子符号)
(2)实验室配制100 mL 1.0 mol·L-1的NaOH溶液时,用到的玻璃仪器除烧杯、玻璃棒、量筒外,还需要______________(填仪器名称)
(3)写出A→B过程中发生反应的离子方程式:______________
(4)该废水中,c(Al3+)=____________
-
某无色废水中可能含有Fe3+、Al3+、Na+、Cl﹣、OH﹣、SO42﹣、中的几种离子.分别取三份废水进行如下实验:
I.进行焰色反应实验,火焰为无色.
Ⅱ.取100mL废水,加入足量的BaCl2溶液,生成2.33g白色沉淀.
Ⅲ.取100mL废水,逐滴加入1.0mol/L的NaOH溶液,消耗NaOH溶液的体积与生成沉淀的质量如图所示.

请根据上述信息回答下列问题:
(1)该废水中一定不含有的离子是_______________.
(2)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器有:___________________.
(3)写出图中A→B反应的离子方程式:___________________.
(4)通过计算,该废水中_____________Cl﹣(填“含有”或“不含有”);
若含有,则c(Cl﹣)=_____________(若不 含有,此问不必作答).
含有,此问不必作答).
-
某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100 mL,进行了三组实验,其操作和有关图像如下所示:
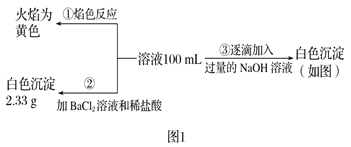
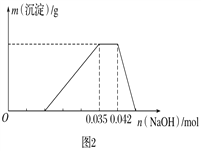
请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的离子有____________________。
(2)实验③中所发生反应的离子反应方程式为___________________________。
(3)依据图2判断出的原溶液中阳离子的种类及物质的量的比值为________。
(4)原溶液中NO3-是否存在?________ (“存在”、“不存在”或“不确定”)
-
某无色废水中可能含有
H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关图像如下所示:Ⅰ:
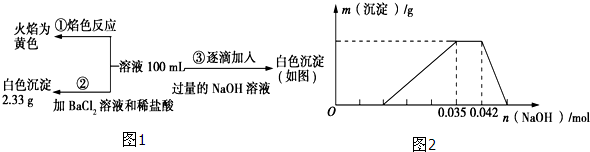
请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的离子有__________;
(2)实验③中所发生反应的离子反应方程式__________;
(3)分析图象,在原溶液中c(NH4+)与c(Al3+)的比值为, NO3-是否存在?__________填(“存在”“不存在”或“不确定”)。
Ⅱ:现有A、B、C、D、E五种可溶性强电解质,它们在水中可电离产生下列离子(各离子不重复)。
| 阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 | OH-、Cl-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性;
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生;
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀;
④上述沉淀包括难溶物和微溶物.
试回答下列问题:
(1)A溶液呈碱性的原因是__________________(用离子方程式表示);
(2)D是______________溶液,E是______________溶液(均写化学式)。
-
某无色废水中可能含有
H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关图像如下所示:Ⅰ:
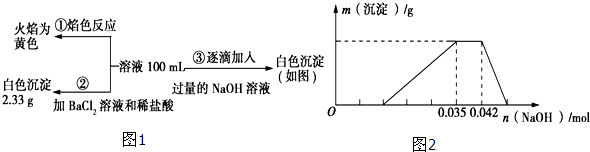
请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的离子有__________;
(2)实验③中所发生反应的离子反应方程式__________;
(3)分析图象,在原溶液中c(NH4+)与c(Al3+)的比值为, NO3-是否存在?__________填(“存在”“不存在”或“不确定”)。
Ⅱ:现有A、B、C、D、E五种可溶性强电解质,它们在水中可电离产生下列离子(各离子不重复)。
| 阳离子 | H+、Na+、Al3+、Ag+、Ba2+ |
| 阴离子 | OH-、Cl-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性;
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生;
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀;
④上述沉淀包括难溶物和微溶物.
试回答下列问题:
(1)A溶液呈碱性的原因是__________________(用离子方程式表示);
(2)D是______________溶液,E是______________溶液(均写化学式)。
-
(8分)有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、NO3-、SO42-、Cl-、HCO3-、Cu2+,取该溶液实验如下:
①取少量该溶液,加几滴石蕊试液, 溶液变红色
②取少量该溶液,浓缩,加Cu片和浓H2SO4,加热, 有无色气体产生,后在空气中又变成红棕色
③取少量该溶液,加BaCl2溶液, 有白色沉淀生成
④取③中上层清液,加AgNO3溶液, 有白色沉淀生成,且不溶于HNO3
⑤取少量该溶液,加NaOH溶液, 有白色沉淀生成,当NaOH过量时沉淀部分溶解
根据上述实验现象判断:
(1)溶液中肯定存在的离子是________。
(2)溶液中肯定不存在的离子是________。
(3)为进一步确定可能存在的离子,应该补充的实验是________ 。
-
某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO32-、SO42-、Cl-中的若干种离子。该小组同学取100 mL水样进行实验,向水样中先滴加硝酸钡溶液,再滴加1 mol·L-1的硝酸,实验过程中沉淀质量的变化情况如图所示:

注明:Ob段表示滴加硝酸钡溶液;bd段表示滴加稀硝酸
(1)水样中一定含有的阴离子是________,其物质的量浓度之比为________。
(2)写出BC段所表示反应的离子方程式:__________________________________________。
(3)由B点到C点变化过程中消耗硝酸的体积为________。
(4)试根据实验结果推断K+是否存在?________(填“是”或“否”);若存在,K+的物质的量浓度c(K+)的范围是__________________。(若K+不存在,则不必回答该问)
(5)设计简单实验验证原水样中可能存在的离子:_____________________。(写出实验步骤、现象和结论)
-
某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO32-、SO42-、Cl-中的若干种离子。该小组同学取100 mL水样进行实验,向水样中先滴加硝酸钡溶液,再滴加1 mol·L-1的硝酸,实验过程中沉淀质量的变化情况如图所示:
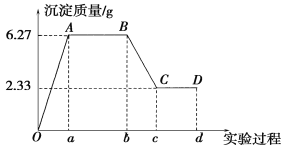
注明:Ob段表示滴加硝酸钡溶液;bd段表示滴加稀硝酸
(1)水样中一定含有的阴离子是________,其物质的量浓度之比为________。
(2)写出BC段所表示反应的离子方程式:__________________________________________。
(3)由B点到C点变化过程中消耗硝酸的体积为________。
(4)试根据实验结果推断K+是否存在?________(填“是”或“否”);若存在,K+的物质的量浓度c(K+)的范围是__________________。(若K+不存在,则不必回答该问)
(5)设计简单实验验证原水样中可能存在的离子:_____________________。(写出实验步骤、现象和结论)
-
某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO32-、SO42-、Cl-中的若干种离子。该小组同学取100mL水样进行实验,向水样中先滴加硝酸钡溶液,再滴加1 mol/L的硝酸,实验过程中沉淀质量的变化情况如图所示:
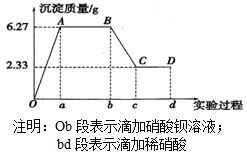
(1)水样中一定含有的阴离子是___________,其物质的量浓度之比为________。
(2)写出BC段所表示反应的离子方程式:___________________。
(3)由B点到C点变化过程中消耗硝酸的体积为________。
(4)试根据实验结果推断K+是否存在___________?(填“是”或“否”);若存在,K+的物质的量浓度c (K+)的范围是____________。(若K+不存在,则不必回答该问)
(5)设计简单实验验证原水样中可能存在的离子:_________(写出实验步骤、现象和结论)。
-
Ⅰ.下列是某研究性学习小组对某无色水样成分的检测过程,已知该水样中只可能含有K+ 、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO32-、SO42-、Cl-中的若干种离子,该小组同学取了100ml水样进行实验:向水样中先滴加硝酸钡溶液,再滴加1mol·L-1硝酸,实验过程中沉淀质量与所加试剂量的关系变化如下图所示:
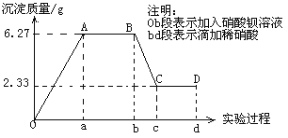
(1)仅凭观察可知该水样中一定不含有的阳离子是________。
(2)由B点到C点变化过程中消耗硝酸的体积为__________ml。
(3)试根据实验结果推测K+是否存在_______(填“是”或“否”)若存在,其物质的量浓度的范围是______mol·L-1(若不存在,则不必回答)。
(4)设计简单实验验证原水样中可能存在的离子__________________________________(写出实验步骤、现象和结论)。
II.湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
(1)写出并配平湿法制高铁酸钾反应的离子方程式:_________________________。
(2)若反应过程中转移了0.3 mol电子,则还原产物的物质的量为________ mol。
(3)低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),原因_______________________________________________________________________。
(4)已知K2FeO4能水解产生Fe(OH)3用作净水剂,请写出水解的离子方程式___________









