-
现有反应的化学方程式为aFeCl2+bKNO3+ cHCl=d FeCl3+eKCl+f X+gH2O。若b=1,d=3,X为生成物,其分子式应为 ( )
A. NH4Cl B. NO2 C. NO D. N2
高一化学单选题中等难度题查看答案及解析
-
(1)在反应式: aFeCl2+bKNO3+cHCl=dFeCl3+eKCl+fX+gH2O中,若b=1,d=3,则X 的分子式为____________。
(2)完成以下氧化还原反应的离子反应方程式,并标出电子转移的方向和数目:___________
___CrI3+____Cl2+______——____K2CrO4 + ____KIO4 +___KCl+______
【答案】 NO

【解析】(1)根据原子守恒得:a=d=3、e=b=1,根据氯原子守恒,则c=4,再由氢原子守恒,则g=2,所以最后根据N、O原子守恒,推出X的化学式为NO,故答案为:NO;
(2)假设CrI3的系数为1,根据Cr元素守恒,K2CrO4的系数为1,根据I守恒,KIO4的系数为3,根据化合价升降守恒,Cl2的系数为
,根据Cl守恒,KCl的系数为27,根据质量守恒定律,反应物中需要一种含有K和O元素的物质,应该为KOH,则生成物中含有H2O,根据K守恒,KOH的系数为32,则H2O的系数为16,因此配平为2CrI3+27Cl2+64KOH =2K2CrO4 + 6KIO4 +54KCl+32H2O,电子转移的方向和数目表示为:
 ,故答案为:
,故答案为: 。
。【题型】填空题
【结束】
26A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行)。

(1)若A、B、C 三种物质的溶液均显碱性,焰色反应均为黄色,C受热分解转化为B
①A与过量W转化为C的总反应的离子方程式_______________。
②B溶液中通入W生成C的离子方程式_______________。
③A溶液与C溶液反应的化学方程式为_______________。
(2)若B的溶液显黄色,一定条件下B的饱和溶液可与沸水反应生成红褐色分散系
①C溶液中加入氢氧化钠溶液的现象_______________。
②B与W转化为C的离子反应方程式_______________。
③一定条件下W与水反应的化学方程式_______________。
(3)若A为NaOH,且C为白色沉淀
①C为_______________。
②A与某金属单质也可生成B,该反应的离子方程式_______________。
③C溶于A的离子反应方程式_______________。
④B与W混合生成白色沉淀的离子反应方程式_______________。
高一化学推断题困难题查看答案及解析
-
某反应的化学方程式为:aFeCl2+bKNO3+cHCl=dFeCl3+eKCl+fX+gH2O,若b=1,d=3,则X的化学式为( )
A.N2 B.NO C.NO2 D.NH4Cl
高一化学选择题简单题查看答案及解析
-
某反应的化学方程式为:aFeCl2+bKNO3+cHCl=dFeCl3+eKCl+fX+gH2O,若b=1,d=3,则X的化学式为( )
A.N2 B.NO C.NO2 D.NH4Cl
高一化学单选题简单题查看答案及解析
-
现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图。
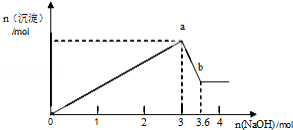
(1)a点对应的沉淀为 (填化学式).
(2)写出ab段反应的离子方程式
(3)计算原混合液中FeCl3的物质的量浓度为多少?(要写计算过程)
高一化学计算题困难题查看答案及解析
-
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH + HCl = NaCl + H2O,
B.2FeCl3 + Cu = 2FeCl2 + CuCl2
判断能否设计成原电池A.________B.________。(填“能”或“不能”)
(2)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生原电池腐蚀,一段时间后某电极产生3.36L标准状况下的气体。
①负极是(填“锌”或“铜”),发生________反应(填“氧化”或“还原”);
②正极的电极反应式为________;
③产生这些气体共需转移电子________mol。
高一化学填空题简单题查看答案及解析
-
现有下列物质:①稀硫酸 ②小苏打 ③氨水 ④二氧化碳 ⑤FeCl3固体 ⑥稀NaOH溶液 ⑦硝酸亚铁溶液。
(1)上述物质中属于电解质的物质序号为______ 。
(2)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是______。
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为______。
(4)能导电的物质序号为_______________。
(5)④与⑥充分反应后,将溶液小火蒸干,得到固体混合物。固体组成成分可能是(用化学式表示)___________________________。
(6)实验室用⑤制备胶体的化学方程式为__________________________________。如果将1molFeCl3全部制成胶体,制得的胶体________(选填“带负电”“电中性”“带正电”),胶粒数目________NA(选填“大于”“等于”“小于”)。
高一化学综合题中等难度题查看答案及解析
-
现有下列物质:①稀硫酸 ②氧化铝固体 ③氨水 ④二氧化碳 ⑤FeCl3固体 ⑥稀NaOH溶液,按要求填空:
(1)上述物质中属于电解质的物质序号为______ ;
(2)有两种物质发生反应的离子方程式为:H++OH-=H2O,这两种物质的序号是______;
(3)加入盐酸、NaOH溶液均能发生化学反应的物质序号为______;试用离子方程式说明:_______________、______________;
(4)能导电的物质序号为_______________;
(5)实验室用⑤制备胶体的化学方程式为_______________________。
高一化学填空题中等难度题查看答案及解析
-
(本题共9分)化学能在一定的条件下可以转化为电能。
(一)现有如下两个反应:
① 2FeCl3 + Cu = 2FeCl2 + CuCl2
② Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
(1)根据两个反应的本质判断,您认为可以设计成原电池的是________(填反应序号),理由是________。
(二)请根据Zn + CuSO4 = ZnSO4 + Cu反应,选择适宜的材料和试剂设计一个原电池。
(2)画出原电池装置图,并在图中标注出电极和电解质溶液的名称。
(3)写出该原电池电极反应式:正极:;负极:________。
高一化学填空题简单题查看答案及解析
-
(8分)化学能在一定的条件下可以转化为电能。
(一)现有如下两个反应:
① 2FeCl3 + Cu = 2FeCl2 + CuCl2
② Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
(1)根据两个反应的本质判断,您认为可以设计成原电池的是 (填反应序号)。
(二)请根据Zn + CuSO4 = ZnSO4 + Cu反应,选择适宜的材料和试剂设计一个原电池。
(2)画出原电池装置图,并在图中标注出电极和电解质溶液的名称。
(3)写出该原电池电极反应式:正极:;负极:________。
高一化学实验题简单题查看答案及解析