-
某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高综合效益,而且还能防止环境污染,生产流程如下:

已知石油裂解已成为生产H的主要方法,E的溶液能发生银镜反应,G是具有香味的液体,试回答下列问题。
(1)F中所含官能团的名称是_____________________________________。
(2)G的结构简式为___________________________。
(3)写出D→E的化学方程式,并注明反应类型:____________________________。
(4)F→G的反应装置如图所示:
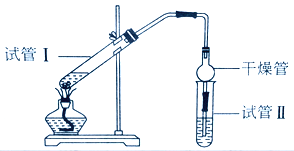
a.图中倒置球形干燥管的作用_____________________________;
b.试管Ⅱ中加有饱和Na2CO3溶液,其作用是: ____________________;
c.具有一个羟基的化合物M 10 g,与F反应生成产物11.85 g,并回收了未反应的M 1.3 g,则M的相对分子质量为____;
(5)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管Ⅱ,再测有机物层的厚度,实验记录如下:
| 实验编号 | 试管Ⅰ中试剂 | 试管II中试剂 | 有机层的厚度/cm |
| A | 2ml乙醇、1ml乙酸、1ml18mol/L浓硫酸 | 饱和碳酸钠溶液 | 3.0 |
| B | 2ml乙醇、1ml乙酸、 | 0.1 |
| C | 2ml乙醇、1ml乙酸、3ml 2mol/L硫酸 | 0.6 |
| D | 2ml乙醇、1ml乙酸、3ml 1mol/L硫酸 | 0.3 |
a.实验D与实验C相对照可证明___________________________________________________。
b.分析实验A、C的数据,可以推测出浓硫酸的__________提高了乙酸乙酯的产率。
(6)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)________。
①单位时间里,生成1 mol乙酸乙酯,同时生成1 mol水
②单位时间里,生成1 mol乙酸乙酯,同时生成1 mol乙酸
③单位时间里,消耗1 mol乙醇,同时消耗1 mol乙酸
④混合物中各物质的浓度不再变化
(7)写出G的一种同分异构体(与G同类)的结构简式:_______________。
-
某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用。不仅可以提高经济效益,而且还能防止环境污染,生产流程如下:
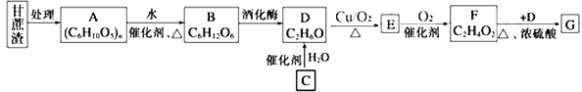
已知石油裂解已成为生产C的主要方法,E的溶液能发生银镜反应,G是具有果香味的液体,试填空:
(1)B的名称:__________;D中官能团的名称:__________。
(2)写出C发生加聚反应的方程式:__________。
(3)D→E的化学方程式:__________;F→G的化学方程式:__________。
(4)已知HCOOCH3也具有果香味,则该物质与G的关系互称为__________,与F的关系互称为:__________。
下图为实验室制取G的装置图,图中a试剂名称为__________,实验结束后分离a和G的方法为__________。
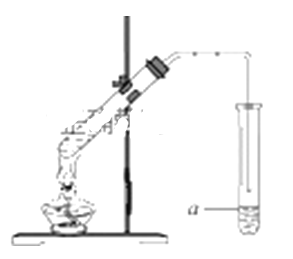 。
。
-
某制糖厂以甘蔗为原料制糖, 同时得到大量的甘蔗渣, 对甘蔗渣进行综合利用不仅可以提高经济效益, 而且还能防止环境污染, 现按下列方式进行综合利用.
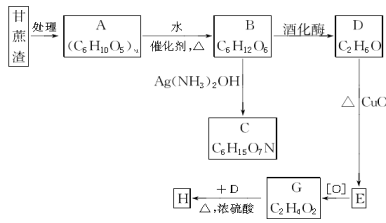
已知H是具有香味的液体.
(1)A的名称是________, H的名称是________,其同分异构体还有(写结构简式)________ _。
(2)写出D→E的化学方程式: __________。写出B→C的离子方程式: ____________。
-
某厂以甘蔗为原料制糖,对产生的大量甘蔗渣按下图所示转化进行综合利用。其中B是A水解的最终产物;C的化学式为C3H6O3,一定条件下2个C分子间脱去2个水分子可生成一种六元环状化合物;D可使溴水褪色。(图中部分反应条件及产物没有列出)
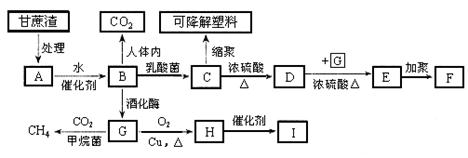
(1)写出下列物质的结构简式:
①高分子化合物F_________________;②C脱水生成的六元环状化合物的结构简式___________。
(2)写出反应G→H的化学方程式:________。
(3)写出A与浓硝酸在一定条件下的反应________,该反应类型为________。
-
某厂以甘蔗为原料制糖,对产生的大量甘蔗渣按下图所示转化进行综合利用。其中B是A水解的最终产物;C的化学式为C3H6O3,一定条件下2个C分子间脱去2个水分子可生成一种六元环状化合物;D可使溴水褪色;F是具有香味的液体。(图中部分反应条件及产物没有列出)
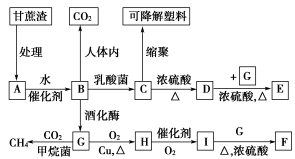
回答下列问题:
(1)A的名称是________,F的结构简式__________,
D的结构简式________。
(2)C→D的反应类型为________。D→E的反应类型为________。
(3)写出下列反应的方程式:
A→B:______________________________;
G→H:______________________________________。
(4)H分子所含官能团的名称是________,实验室中常用于检验该官能团的试剂的名称是(只写一种)_____________________________。
-
工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。为了保护环境,同时提高硫酸工业的综合经济效益,应尽可能将尾气中的SO2转化为有用的副产品。请按要求回答下列问题:
(1)将尾气通入氨水中,能发生多个反应,写出其中可能发生的两个氧化还原反应的化学方程式:__________________、__________________。
(2)在尾气与氨水反应所得到的高浓度溶液中,按一 定比例加入氨水或碳酸氢铵,此时溶液的温度会自行降低,并析出晶体。①导致溶液温度降低的原因可能是______________;②析出的晶体可用于造纸工业,也可用于照相用显影液的生产。已知该结晶水合物的相对分子质量为134,则其化学式为______________。
-
工业生产需要大量原料,消耗大量能源,在得到所需产品同时产生了大量废气、废水、废渣。某工厂排放的废水中含有Cu2+、Fe2+、Hg2+、H+等离子,某化学小组为了充分利用资源和保护环境,准备回收废水中的铜和汞,同时得到绿矾。他们设计了如下实验方案:
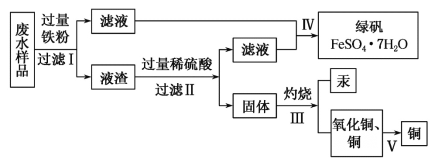
(1)现有仪器:酒精灯、玻璃棒、坩埚、蒸发皿、蒸馏烧瓶、烧杯、铁架台等,完成步骤Ⅳ的实验操作还需要选择的玻璃仪器是__________设计简单实验检验绿矾是否变质,简述你的操作:__________。
(2)步骤Ⅰ中加入过量铁粉的目的是__________,步骤Ⅱ中__________(填“能”或“不能”)用盐酸代替硫酸。
(3)步骤V利用氧化铜制取铜有如下四种方案:
方案甲:利用氢气还原氧化铜;
方案乙:利用一氧化碳还原氧化铜;
方案丙:利用炭粉还原氧化铜;
方案丁:先将氧化铜溶于稀硫酸,然后加入过量的铁粉、过滤,再将滤渣溶于过量的稀硫酸,再过滤、洗涤、烘干。
从安全角度考虑,方案__________不好;从产品纯度考虑,方案__________不好。
(4)写出步骤Ⅱ中涉及反应的离子方程式:__________;步骤Ⅳ得到绿矾的操作蒸发浓缩__________、__________。
-
将磷肥生产中形成的副产物石膏(CaSO4·2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图。
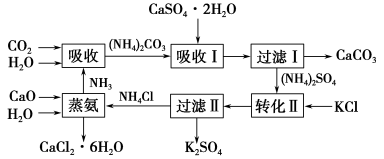
(1)本工艺中所用的原料除CaSO4·2H2O、KCl外,还需要__________等原料。
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式: ______________________。
(3)过滤Ⅰ操作所得固体中,除CaCO3外还含有____________(填化学式)等物质,该固体可用作生产水泥的原料。
(4)氯化钙结晶水合物(CaCl2·6H2O)是目前常用的无机储热材料,选择的依据是__________。
a.熔点较低(29 ℃熔化) b.能导电
c.能制冷 d.无毒
(5)上述工艺流程中体现的绿色化学理念是____________________________
-
将磷肥生产中形成的副产物石膏(CaSO4·2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图。

(1)本工艺中所用的原料除CaSO4·2H2O、KCl外,还需要________等原料。
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式:______________________________________________________________。
(3)过滤Ⅰ操作所得固体中,除CaCO3外还含有________(填化学式)等物质,该固体可用作生产水泥的原料。
(4)过滤Ⅰ操作所得滤液是(NH4)2SO4溶液。检验滤液中含有CO32-的方法是:_______________________________________________________________。
(5)已知不同温度下K2SO4在100 g水中达到饱和时溶解的量如下表:
| 温度/℃ | 0 | 20 | 60 |
| K2SO4溶解的量/g | 7.4 | 11.1 | 18.2 |
60 ℃时K2SO4的饱和溶液591 g冷却到0 ℃,可析出K2SO4晶体________g。
(6)氯化钙结晶水合物(CaCl2·6H2O)是目前常用的无机储热材料,选择的依据是________。
a.熔点较低(29 ℃熔化) b.能导电
c.能制冷 d.无毒
(7)上述工艺流程中体现绿色化学理念的是:________________________________________________________________。
-
将磷肥生产中形成的副产物石膏(CaSO4·2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义。以下在石膏转化为硫酸钾和氯化钙的工艺流程示意图。
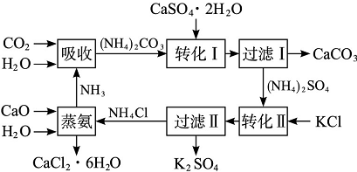
(1)本工艺中所用的原料除CaSO4·2H2O外,还需要____________等原料。
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式:__________________。
(3)过滤Ⅰ操作所得滤液是(NH4)2SO4溶液。检验滤液中含有CO32—的方法是:_______________。
(4)氯化钙结晶水合物(CaCl2·6H2O)是目前常用的无机储热材料,选择的依据是________。
a.熔点较低(29 ℃熔化) b.能导电 c.易溶于水 d.无毒
(5)上述工艺流程中体现绿色化学理念的是_________________________。



 。
。





