-
合成氨工业生产中所用的αFe催化剂的主要成分是FeO、Fe2O3。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4∶5,其中Fe2+与Fe3+物质的量之比为________。
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1∶2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为________(用小数表示,保留2位小数)。
(3)以Fe2O3为原料制备上述催化剂,可向其中加入适量碳粉,发生如下反应:2Fe2O3+C
4FeO+CO2↑。
高三化学填空题困难题查看答案及解析
-
合成氨工业生产中所用的α Fe催化剂的主要成分为FeO、Fe2O3。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4∶5,其中Fe2+与Fe3+物质的量之比为________。
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1∶2时,其催化剂活性最高,此时混合物中铁的质量分数为________(保留两位小数)。
(3)写出由C(炭粉)与Fe2O3在高温下反应制备α铁触媒的化学方程式(另一种产物可溶于水):____________________________________________________________。
(4)为制得这种活性最高的催化剂,理论上应向480 g Fe2O3粉末加入炭粉的质量是多少?,生成该实验条件下CO2的体积是多少?(请写出计算过程。假设此实验条件下,气体摩尔体积为24 L·mol-1)。___________
高三化学综合题中等难度题查看答案及解析
-
钒及其化合物在特种钢材的生产、高效催化剂的制备及航天工业中用途广泛。工业上以富钒炉渣(主要成分为V2O5,含少量Fe2O3和FeO等杂质)为原料提取五氧化二钒的工艺流程如图所示:
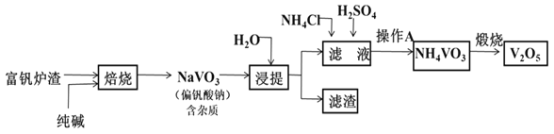
(1)五氧化二钒中钒的化合价为__。
(2)焙烧炉中发生的主要反应化学方程式为__;也可用氯化钠和氧气代替纯碱进行焙烧反应,写出对应的化学反应方程式__,该方法的缺点是:__。
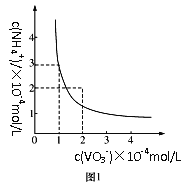
(3)已知NH4VO3难溶于水,在水中的Ksp曲线如图1所示,则在实验中进行操作A所需要的玻璃仪器有__;向10mL含NaVO30.2mol/L的滤液中加入等体积的NH4Cl溶液(忽略混合过程中的体积变化),欲使VO3-沉淀完全,则NH4Cl溶液的最小浓度为__。(当溶液中某离子浓度小于1×10-5mol/L时,认为该离子沉淀完全)
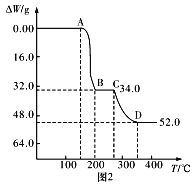
(4)为研究煅烧过程中发生的化学变化,某研究小组取234gNH4VO3进行探究,焙烧过程中减少的质量随温度变化的曲线如图2所示,则C点所得物质化学式为__,写出CD段发生反应的化学方程式:__。
高三化学工业流程中等难度题查看答案及解析
-
工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)为原料制备高档颜料——铁红(Fe2O3),具体生产流程如下:
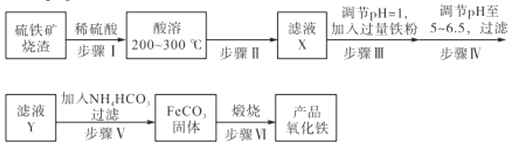
试回答下列问题:
(1)实验室实现“步骤II”中分离操作所用的玻璃仪器有____、玻璃棒和烧杯等;该步骤是为了除去_______(填相关物质的化学式)。
(2)检验步骤III已经进行完全的操作是_______________________。
(3)步骤V的反应温度一般需控制在35℃以下,其目的是______________;该步骤中反应生成FeCO3的离子反应方程式为___________。
(4)步骤VI中发生反应的化学反应方程式为____________________。
(5)步骤V中,FeCO3达到沉淀溶解平衡时,若c(Fe2+)=1×10-6mol/L,欲使所得的FeCO3中不含有Fe(OH)2,应控制溶液的pH≤_____ (已知:Ksp[Fe(OH)2]=4.9×10-17,lg7=0.8)。
(6)欲测定硫铁矿矿渣中Fe元素的质量分数,称取ag样品,充分“酸溶” “水溶”后过滤,向滤液中加入足量的H2O2,充分反应后加入NaOH溶液至不再继续产生沉淀,经过滤、洗涤、灼烧至固体恒重,冷却后称得残留固体bg,测得该样品中Fe元素的质量分数为______。
高三化学综合题困难题查看答案及解析
-
古埃及人在公元前一千多年前曾用橄榄石(硅酸盐)作饰品,称它为“太阳的宝石”。某小组以某橄榄石(主要成分可看作为MgO、FeO和SiO2,还含有少量的MnO等)为原料制备工业合成氨的活性催化剂(FeO和Fe2O3质量比为9:20的混合物)的一种流程如下:

金属离子生成氢氧化物沉淀的pH如下表:
金属离子
开始沉淀的pH
沉淀完全的pH
Mg2+
7.6
9.4
Fe2+
6.5
9.9
Fe3+
1.5
3.3
Mn2+
8.2
10.6
回答以下问题:
(1)从绿色化学角度分析,试剂1宜选择___(填字母)。加入试剂1的目的是___(用离子方程式表示)。
a.H2O2 b.MnO2 c.HNO3 d.K2Cr2O7
(2)调节pH范围为___。
(3)单位时间内“酸浸”中金属浸出率与温度、盐酸浓度的关系如图所示。

x___(填“>”“<”或“=”)2。当盐酸浓度相同时,温度高于45℃,浸出率降低的主要原因是___。
(4)“还原”过程中,不仅要控制温度,而且要控制氧化铁和炭粉(C)的比例。若“还原”时产生气体的相对分子质量为36,理论上,480kgFe2O3需要加入___kg炭粉(C)。
高三化学工业流程中等难度题查看答案及解析
-
无水AICl3可用作有机合成的催化剂,食品膨松剂等。工业上由铝土矿(主要成分是Al2O3和Fe2O3)和石油焦(主要成分是碳单质)制备无水AlCl3的流程如下:

(1)在焙烧炉中发生反应:①Fe2O3(S) +3C(s)
2Fe(s) +3CO(g);
②3CO(g)+Fe2O3(s)
2Fe(s)+3CO2(g).
则反应②的平衡常数的表达式为K= ________。
(2)Al2O3、Cl2和C在氯化炉中高温下发生反应,当生成1molAlCl3时转移________mol电子;炉气中含有大量CO和少量Cl2,可用Na2SO3溶液除去Cl2,其离子方程式为:________。
(3)升华器中发生反应的化学方程式为 ________。
(4)工业上另一种由铝灰为原料制备无水AlCl3工艺中,最后一步是由AlCl3·6H2O脱去结晶水制备无水AICl3,此反应必须在氯化氢的气流中加热,其原因是________。
已知SOCl2为无色液体且极易与水反应生成HC1和SO2,AlC13·6H2O与SOCl2混合加热可制取无水AlCl3,写出该反应的化学方程式:________。
高三化学填空题困难题查看答案及解析
-
无水AlCl3可用作有机合成的催化剂、食品膨松剂等。工业上由铝土矿(主要成分是A12O3和Fe2O3)和石油焦(主要成分是C)按下图所示流程进行一系列反应来制备无水AlCl3。
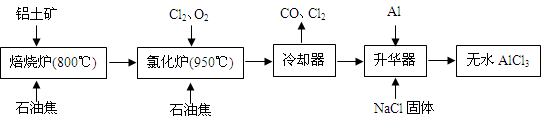
(1)氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则AlCl3是:________晶体,其结构式为:________。
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式是________。
(3)冷却器排出的尾气中含有大量CO和少量Cl2,需用Na2SO3溶液除去Cl2,此反应的离子方程式为:________。
(4)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是:________。
(5)AlCl3产品中Fe元素含量直接影响其品质,为测定产品中Fe元素的含量,现称取16.25g无水AlCl3产品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重残留固体质量为0.32g。则产品中Fe元素的含量为:________。
高三化学填空题困难题查看答案及解析
-
无水AlCl3易升华,可用作有机合成的催化剂等.工业上由铝土矿(主要成分是Al2O3和Fe2O3)和石油焦(主要成分是C)为原料制备无水AlCl3的工艺(碳氯化法)流程如下:
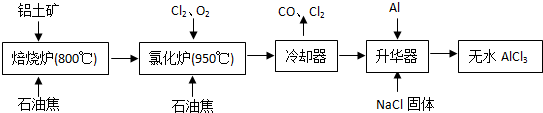
(1)氯化炉中Al2O3、Cl2和C反应的化学方程式为______ 2A1C13+3CO高三化学解答题中等难度题查看答案及解析
-
(12分)无水A1C13可用作有机合成的催化剂,食品膨松剂等。工业上由铝土矿(主要成分是A12O3和Fe2O3)和石油焦(主要成分是碳单质)制备无水A1C13的流程如下
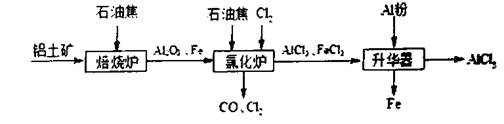
(1)在焙烧炉中发生反应:①
②
。则反应②的平衡常数的表达式为K=________。
(2)氯化炉中A12O3,C12和C在高温下反应的化学方程式为________;其炉气中含有大量CO和少量C12,可用溶液除去C12,并回收CO。
(3)升华器中主要含有A1C13和FeC13,需加入一定量A1,其目的是 。
(4)工业上另一种由铝灰为原料制备无水A1C13工艺中,最后一步是由A1C136H2O脱去结晶水制备无水A1C13,直接加热不能得到无水A1C13,其原因是________。已知SOC12为无色液体且极易与水反应生成HC1和SO2,A1C136H2O与SOC12混合加热可制取无水A1C13,写出该反应的化学方程式:
高三化学填空题中等难度题查看答案及解析
-
氯化亚铜(化学式为CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇;在空气中迅速被氧化,风光则分解。某实验小组用工业废液(主要成分为Cu2S和Fe2O3)制取氯化亚铜并同时生成电路板蚀刻液,设计流程如:
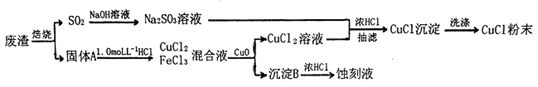
根据以上信息回答下列问题:
(1)固体A的成分为Fe2O3和_________,为提高固体A的溶解速率,可采取的措施是__________(任写一种)。
(2)沉淀B为________,不宜将沉淀剂CaO改为NaOH溶液,其理由是______________________。
(3)在Na2SO3的水溶液中逐滴加入CuCl2的水溶液中,再加入少量浓盐酸混匀,倾出清液,抽滤即得CuCl沉淀,写出该反应的离子方程式________________________ _,CuCl沉淀的洗涤剂应选用_________以减少沉淀的溶解损失,所得CuCl粉末应密封在真空或充有______的避光装置中保存。
(4)熔融态氯化亚铜时快时导电性差,实验测得氯化亚铜蒸汽的相对分子质量为199,则氯化亚铜分子式为_________,属___________(填:共价或离子)化合物。
(5)氯化亚铜在热水中迅速与水反应生成砖红色固体,写出该反应的化学方程式________ _______。
高三化学简答题困难题查看答案及解析