-
治理S02、CO、NOx污染是化学工作者研宂的重要课题。
I.硫酸厂大量排放含SO2的尾气会对环境造成严重危害。
(1)工业上可利用废碱液(主要成分为Na2C03)处理硫酸厂尾气中的S02,得到Na2S03溶液,该反应的离子方程式为_____。
II.沥青混凝土可作为反应:2CO(g)+02(g) 0CO2(g)的催化剂。图甲表示恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥音混凝土(ɑ型、β型)催化时,CO的转化率与温度的关系。
0CO2(g)的催化剂。图甲表示恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥音混凝土(ɑ型、β型)催化时,CO的转化率与温度的关系。
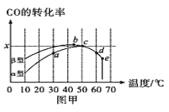
(2)a、b、c、d四点中,达到平衡状态的是_____。
(3)已知c点时容器中02浓度为0.02mol/L,则50℃时,在α型沥音混凝土中CO转化反成的平衡常数K=
_____ (用含 的代数式表示)。
的代数式表示)。
(4)下列关于图中的说法正确的是_____。
A.C0转化反应的平衡常数K(a)<K(c)
B.在均未达到平衡状态时,同温下型沥音混凝土中CO转化速率比α型要大
C.b点时CO与O2分子之间发生有效碰撞的几率在整个实验过程中最高
D.e点转化率出现突变的原因可能是温度升高后催化剂失去活性
Ⅲ.某含钴催化剂可以催化消除柴油车尾气中的碳烟(C)和NOx。不同温度下某含钴催化剂可同时催化去除柴油车尾气中的碳烟(C)和NOx。不同温度下,将10mol模拟尾气(成分如下表所示)以相同的流速通过该催化剂,测得所有产物(CO2、N2、N2O)与NO的相关数据图乙所示。
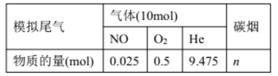
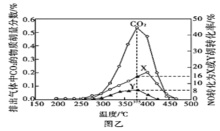
(5)375℃时,测得排出的气体中含0.45molO2和0.052molCO2,则Y的化学式为_________。
(6)实验过程中采用NO模拟NOx,而不采用NO2的原因是_____。
-
SO2和NOx在化学工业上有重要用途,也是大气污染的主要来源,开发和利用并重,预防和治理并举是当前工业上和环境保护领域研究的主要课题之一。
(1)在接触法制硫酸的过程中,发生2SO2(g)+O2(g)  2SO3(g) △H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题:
2SO3(g) △H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题:
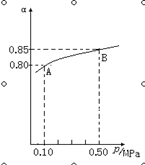
①平衡状态由A到B时,平衡常数K(A)________K(B)(填“>”、“<”或“=”);
②将2.0molSO2和1.0molO2置于10L的密闭容器中,若40s后反应达到平衡,此时体系总压强为0.10MPa,这一段时间内SO2的平均反应速率为________。
该反应的平衡常数为________。
(2)用CH4催化还原NOx可消除氮的氧化物的污染,例如:CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol—1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol—1
取标准状况下4.48LCH4并使之完全反应:
①若将NO2还原至N2,整个过程中转移电子的物质的量为________;
②若还原NO2和NO的混合物,放出的总热量Q的取值范围是________。
-
SO2和NOx在化学工业上有重要用途,也是大气污染的主要来源,开发和利用并重,预防和治理并举是当前工业上和环境保护领域研究的主要课题之一。
(1)在接触法制硫酸的过程中,发生2SO2(g)+O2(g)  2SO3(g) △H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题:
2SO3(g) △H<0反应,某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如下图所示,根据图示回答下列问题:
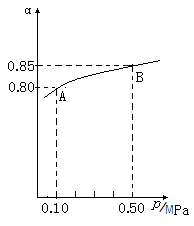
①平衡状态由A到B时,平衡常数K(A)________K(B)(填“>”、“<”或“=”);
②将2.0molSO2和1.0molO2置于10L的密闭容器中,若40s后反应达到平衡,此时体系总压强为0.10MPa,这一段时间内SO2的平均反应速率为________。
该反应的平衡常数为________。
(2)用CH4催化还原NOx可消除氮的氧化物的污染,例如:
CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g) △H=—574kJ·mol—1
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H=—1160kJ·mol—1
取标准状况下4.48LCH4并使之完全反应:
①若将NO2还原至N2,整个过程中转移电子的物质的量为________;
②若还原NO2和NO的混合物,放出的总热量Q的取值范围是________。
-
燃煤的烟气中常含有大量的NOx、CO、SO2等有害气体,治理污染、消除有害气体对环境的影响是化学工作者研究的重要课题。
Ⅰ.已知氮氧化物可采用强氧化剂Na2S2O8氧化脱除,过程如下所示:
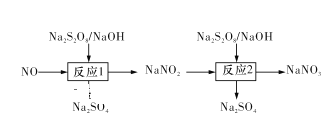
(1)写出反应1的离子方程式:____ 。
(2)反应2为NO2-+S2O82-+2OH-=NO3-+2SO42-+H2O。此反应在不同温度下达到平衡时,NO2-的脱除率与Na2S2O8初始浓度的关系如图1所示。
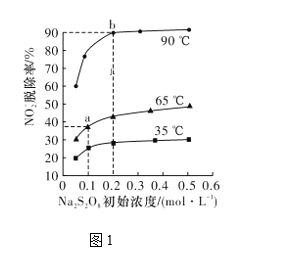
①比较a、b点的反应速率:va正____vb逆(填“>”“<”或“=”)。
②根据图像可以判断该反应为吸热反应,理由是____________。
Ⅱ.沥青混凝土可作为反应2CO(g)+O2(g) 2CO2(g)的催化剂。图2表示在相同的恒容密闭容器、相同的起始浓度、相同的反应时间段下,使用相同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
2CO2(g)的催化剂。图2表示在相同的恒容密闭容器、相同的起始浓度、相同的反应时间段下,使用相同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
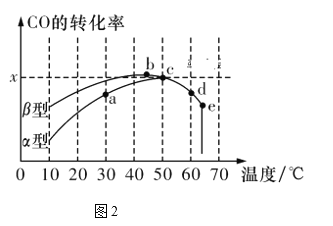
(3)下列关于图2的说法正确的是________。
A.在均未达到平衡状态时,同温下β型沥青混凝土中CO转化速率比α型要大
B.b点时CO与O2分子之间发生有效碰撞的几率在整个实验过程中最高
C.a、b、c、d四点中,达到平衡状态的只有b、c两点
D.e点转化率出现突变的原因可能是温度升高后催化剂失去活性
(4)已知c点时容器中O2浓度为0.02 mol/L,则50 ℃时,在α型沥青混凝土中CO转化反应的平衡常数K=_____________(用含x的代数式表示)。
Ⅲ.利用图3所示装置(电极均为惰性电极)可吸收SO2。
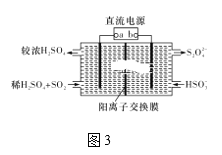
(5)直流电源b极为____,阳极发生的反应为______。
-
燃煤的烟气中常含有大量的NOx、CO、SO2等有害气体,治理污染、消除有害气体对环境的影响是化学工作者研究的重要课题。
Ⅰ.已知氮氧化物可采用强氧化剂Na2S2O8氧化脱除,过程如下所示:
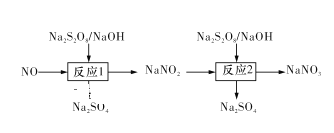
(1)写出反应1的离子方程式:____ 。
(2)反应2为NO2-+S2O82-+2OH-=NO3-+2SO42-+H2O。此反应在不同温度下达到平衡时,NO2-的脱除率与Na2S2O8初始浓度的关系如图1所示。
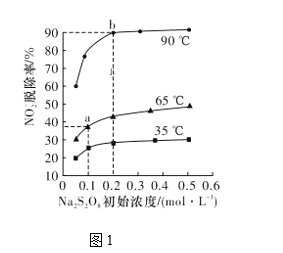
①比较a、b点的反应速率:va正____vb逆(填“>”“<”或“=”)。
②根据图像可以判断该反应为吸热反应,理由是____________。
Ⅱ.沥青混凝土可作为反应2CO(g)+O2(g) 2CO2(g)的催化剂。图2表示在相同的恒容密闭容器、相同的起始浓度、相同的反应时间段下,使用相同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
2CO2(g)的催化剂。图2表示在相同的恒容密闭容器、相同的起始浓度、相同的反应时间段下,使用相同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
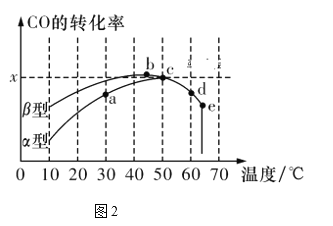
(3)下列关于图2的说法正确的是________。
A.在均未达到平衡状态时,同温下β型沥青混凝土中CO转化速率比α型要大
B.b点时CO与O2分子之间发生有效碰撞的几率在整个实验过程中最高
C.a、b、c、d四点中,达到平衡状态的只有b、c两点
D.e点转化率出现突变的原因可能是温度升高后催化剂失去活性
(4)已知c点时容器中O2浓度为0.02 mol/L,则50 ℃时,在α型沥青混凝土中CO转化反应的平衡常数K=_____________(用含x的代数式表示)。
Ⅲ.利用图3所示装置(电极均为惰性电极)可吸收SO2。
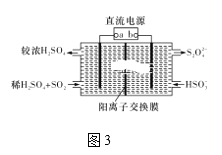
(5)直流电源b极为____,阳极发生的反应为______。
-
S02的含量是空气质量日报中一项重要检测指标,也是最近雾霾天气肆虐我国大部分地区的主要原因之一。加大S02的处理力度,是治理环境污染的当务之急。
I.电化学法处理SO2。
硫酸工业尾气中的SO2经分离后,可用于制备硫酸,同时获得电能,装置如右图所示(电极均为惰性材料):
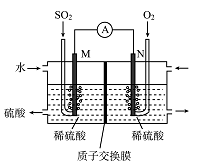
(1)M极发生的电极反应式为________________。
(2)若使该装置的电流强度达到2.0A,理论上每分钟应向负极通入标准状况下气体的体积为 L(已知:1个e所带电量为1.6×10-19C)。
Ⅱ,溶液与电化学综合(钠碱循环法)处理SO2。
(3)钠碱循环法中,用Na2SO3溶液作为吸收液来吸收SO2,该反应的离子方程式为 。
(4)吸收液吸收SO2的过程中,pH随n(SO32-)/n(HSO3-)变化关系如右图所示:
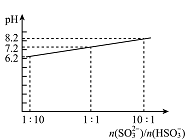
①用图中数据和变化规律说明NaHSO3溶液呈酸性的原因 。
②n(SO32-)/n(HSO3-)=1:1时,溶液中离子浓度由大到小的顺序是 。
(5)当吸收液的pH降至约为6时,需送至电解槽处理,直至得到pH>8的吸收液再循环利用,其电解示意图如下:
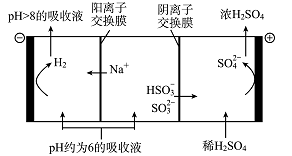
①写出阳极发生的电极反应式 ;
②当电极上有2 mol电子转移时阴极产物的质量为 。
-
雾霾天气严重影响人们的生活健康,治理污染是化学工作者义不容辞的职责,因而对SO2、NOx等进行研究其有重要意义。
请根据以下信息回答有关问题:
I.NOx是汽车尾气的主要污染物之一。
(1)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:

该反应的△H=__________。
(2)科学家通过实验发现,在紫外线照射下TiO2会使空气中的某些分子产生活性基团OH,并且活性基团OH可与NO2、NO发生反应生成硝酸和水。根据左下图示,请写出OH与NO反应的化学方程式__________。
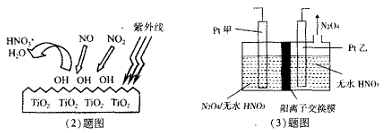
(3)电解法可将工业废气中含有的NO2消除。原理是先将NO2转化为N2O4,然后电解得到N2O5 (常温下为无色固体,常做绿色硝化剂)。电解原理如右上图所示,该电解池中生成N2O5的电极反应式是___________。
Ⅱ.工业上采取多种措施减少SO2的排放。
(4)碘循环工艺具体流程如下:
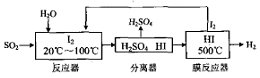
① 用化学方程式表示反应器中发生的反应___________。
② 在HI分解反应中使用膜反应器分离出H2的目的是__________。
③ 该工艺流程的优点有________。
(5)喷雾干燥法脱硫是除去SO2的常见方法,先将含SO2的废气溶于水,再用饱和石灰浆吸收,吸收液中c(Ca2+)一直保持为0.70mol/L,则吸收液中的c(SO42-)为_____。[已知该温度下,Ksp (CaSO3)=1.4×10-7]
-
工业废气、汽车尾气排放出的NOx、SO2等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
Ⅰ. NOx的消除。汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可发生如下反应:2NO(g)+2CO(g)  N2(g)+2CO2(g) △H。
N2(g)+2CO2(g) △H。
(1)已知:CO燃烧热的△H1=-283.0kJ·mol-l,
N2(g)+O2(g)  2NO(g) △H2=+180.5kJ·mol-1,则△H=____________。
2NO(g) △H2=+180.5kJ·mol-1,则△H=____________。
(2)某研究小组探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。
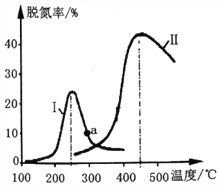
①以下说法正确的是__________________(填字母)。
A.两种催化剂均能降低活化能,但△H不变
B.相同条件下,改变压强对脱氮率没有影响
C.曲线Ⅱ中的催化剂适用于450℃左右脱氮
D.曲线Ⅱ中催化剂脱氮率比曲线I中的高
②若低于200℃,图中曲线I脱氮率随温度升高而变化不大的主要原因为___________;判断a点是否为对应温度下的平衡脱氮率,并说明其理由:____________。
Ⅱ.SO2的综合利用
(3)某研究小组对反应NO2+SO2 SO3+NO △H<0进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[no(NO2):no(SO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[a(NO2)]。部分实验结果如右图所示。
SO3+NO △H<0进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[no(NO2):no(SO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[a(NO2)]。部分实验结果如右图所示。
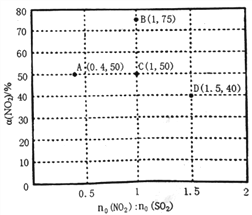
①如果将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是________________。
②图中C、D两点对应的实验温度分别为TC和TD,通过计算判断:TC__________TD(填“>”、“=”或“<”)。
(4)已知25℃时,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。若氨水的浓度为2.0mol·L-1,溶液中的c(OHˉ)= ____________mol·L-1;将SO2通入该氨水中,当溶液呈中性时溶液中的 =__________。
=__________。
-
工业废气、汽车尾气排放出的NOx、SO2等,是形成雾霾的主要物质,其综合治理是当前重要的研究课题。
Ⅰ.NOx的消除。汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可发生如下反应:2NO(g)+2CO(g)  N2(g)+2CO2(g) △H。
N2(g)+2CO2(g) △H。
(1)已知:CO燃烧热的△H1=-283.0kJ·mol-l,N2(g)+O2(g)  2NO(g) △H2=+180.5kJ·mol-1,则△H=____________。
2NO(g) △H2=+180.5kJ·mol-1,则△H=____________。
(2)某研究小组探究催化剂对CO、NO转化的影响。将NO和CO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中NO含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如下图所示。

①以下说法正确的是__________________(填字母)。
A.两种催化剂均能降低活化能,但△H不变
B.相同条件下,改变压强对脱氮率没有影响
C.曲线Ⅱ中的催化剂适用于450℃左右脱氮
D.曲线Ⅱ中催化剂脱氮率比曲线I中的高
②若低于200℃,图中曲线I脱氮率随温度升高而变化不大的主要原因为___________;判断a点是否为对应温度下的平衡脱氮率,并说明其理由:____________。
Ⅱ.SO2的综合利用
(3)某研究小组对反应NO2+SO2 SO3+NO △H<0进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(NO2):n0(SO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[α(NO2)]。部分实验结果如下图所示。
SO3+NO △H<0进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n0(NO2):n0(SO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定NO2的平衡转化率[α(NO2)]。部分实验结果如下图所示。
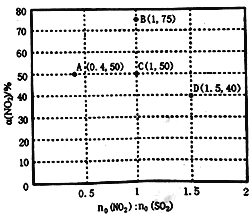
①如果将图中C点的平衡状态改变为B点的平衡状态,应采取的措施是____________。
②图中C、D两点对应的实验温度分别为TC和TD,通过计算判断:TC__________TD(填“>”、“=”或“<”)。
(4)已知25C时,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka=6.2×10-8。若氨水的浓度为2.0mol·L-1,溶液中的c(OHˉ)= _________mol·L-1;将SO2通入该氨水中,当溶液呈中性时溶液中的 =__________。
=__________。
-
治理SO2、CO、NOx污染是化学工作者研究的重要课题。
Ⅰ.软锰矿(MnO2)、菱锰矿(MnCO3)吸收烧结烟气中的SO2制取硫酸锰。pH值对SO2 吸收率的影响如图所示。在吸收过程中,氧气溶解在矿浆中将 H2SO3氧化成硫酸。
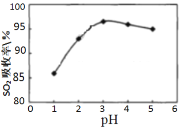
(1)SO2的吸收率在pH=_____效果最佳,MnO2所起的作用是_______,菱锰矿作为调控剂与硫酸反应, 确保pH的稳定,该反应的化学方程式为___________。
Ⅱ.沥青混凝土可作为2CO(g)+O2(g) 2CO2(g)反应的催化剂。图表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
2CO2(g)反应的催化剂。图表示在相同的恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
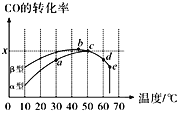
(2)CO转化反应的平衡常数K(a)____K(c)(填“>”“<”或“=”,下同),在均未达到平衡状态时,同温下β型沥青混凝土中CO转化速率___α型,e点转化率出现突变的原因可能是______。
Ⅲ.N2H4是一种具有强还原性的物质。燃烧过程中释放的能量如下:(已知a>b)
① N2H4(g)+2O2(g) == NO2(g)+1/2N2(g)+2H2O(g) ΔH1=a kJ·mol-1
② N2H4(g)+2O2(g) == 2NO(g)+2H2O(g) ΔH2=b kJ·mol-1
(3)已知反应活化能越低,反应速率越大。假设某温度下,反应Ⅰ的速率(v1)大于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是______。
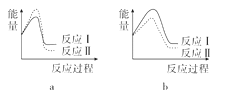

(4)试写出NO(g)分解生成N2(g)和NO2(g)的热化学方程式为_____________。
Ⅳ.某含钴催化剂可以催化消除柴油车尾气中的碳烟(C)和NOx。不同温度下,将模拟尾气(成分如下表所示)以相同的流速通过该催化剂,测得所有产物(CO2、N2、N2O)与NO的相关数据结果如下图所示。
| 模拟尾气 | 气体(10mol) | 碳烟 |
| NO | O2 | He |
| 物质的量(mol) | 0.025 | 0.5 | 9.475 | n |
(5)375℃时,测得排出的气体中含0.45 molO2和0.0525mol CO2,则Y的化学式为_____。实验过程中不采用NO2的模拟NOx原因是_________。

0CO2(g)的催化剂。图甲表示恒容密闭容器、相同起始浓度、相同反应时间段下,使用同质量的不同沥音混凝土(ɑ型、β型)催化时,CO的转化率与温度的关系。

的代数式表示)。




















 =__________。
=__________。





