铝和氢氧化钾都是重要的工业产品,工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯,其工作原理如图2所示。下列有关说法错误的是
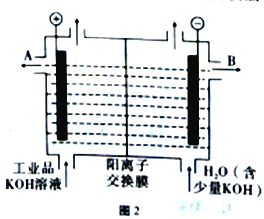
A. 工业冶炼铝采用的是电解法
B. 铝与氢氧化钾溶液反应的离子方程式是2A1+2OH-+2H2O=2A1O2-+3H2↑
C. 图中电解槽的阳极反应式是2H2O-4e-=4H++O2↑
D. 除去杂质后的氢氧化钾溶液从图中的B处流出
高三化学null中等难度题
铝和氢氧化钾都是重要的工业产品,工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯,其工作原理如图2所示。下列有关说法错误的是

A. 工业冶炼铝采用的是电解法
B. 铝与氢氧化钾溶液反应的离子方程式是2A1+2OH-+2H2O=2A1O2-+3H2↑
C. 图中电解槽的阳极反应式是2H2O-4e-=4H++O2↑
D. 除去杂质后的氢氧化钾溶液从图中的B处流出
高三化学null中等难度题
铝和氢氧化钾都是重要的工业产品,工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯,其工作原理如图2所示。下列有关说法错误的是

A. 工业冶炼铝采用的是电解法
B. 铝与氢氧化钾溶液反应的离子方程式是2A1+2OH-+2H2O=2A1O2-+3H2↑
C. 图中电解槽的阳极反应式是2H2O-4e-=4H++O2↑
D. 除去杂质后的氢氧化钾溶液从图中的B处流出
高三化学null中等难度题查看答案及解析
工业品氢氧化钾溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。下列说法不正确的是
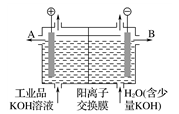
A. 阴极材料可以是Fe,含氧酸根杂质不参与电极上放电
B. 该电解槽的阳极反应式为:4OH―― 4e-= 2H2O+O2↑
C. 通电后,该电解槽阴极附近溶液pH会减小
D. 除去杂质后氢氧化钾溶液从出口B导出
高三化学选择题中等难度题查看答案及解析
工业品氢氧化钾溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。下列说法不正确的是
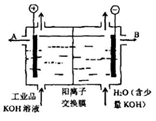
A.阴极材料可以是Fe,含氧酸根杂质不参与电极上放电
B.该电解槽的阳极反应式为:4OH―― 4e-= 2H2O+O2↑
C.通电后,该电解槽阴极附近溶液pH会减小
D.除去杂质后氢氧化钾溶液从出口B导出
高三化学选择题中等难度题查看答案及解析
工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。下列说法中正确的是
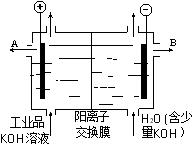
A.该电解槽的阳极反应式是4OH--2e-→2H2O+ O2↑
B.通电开始后,阴极附近溶液pH会减小
C.除去杂质后氢氧化钾溶液从液体出口A导出
D.用氯化钾制备氢氧化钾也可采用这种离子交换膜电解法
高三化学选择题中等难度题查看答案及解析
铝和氢氧化钾都是重要的工业产品。请回答:
(1)工业冶炼铝的化学方程式是 。
(2)铝与氢氧化钾溶液反应的离子方程式是 。
(3)工业品氢氧化钾的溶液中含有某些含氧酸杂质,可用离子交换膜法电解提纯。
电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
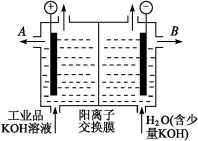
①该电解槽的阳极反应式是 。
②通电开始后,阴极附近溶液pH会增大,请简述原因 。
③除去杂质后的氢氧化钾溶液从溶液出口 (填写“A”或“B”)导出。
高三化学填空题中等难度题查看答案及解析
(8分)氢氧化钾是重要的工业产品。请回答:
(1)铝与氢氧化钾溶液反应的离子方程式是 。
(2)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
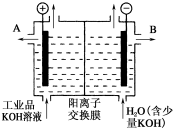
①该电解槽的阳极反应式是 。
②通电开始后,阴极附近溶液pH会增大,请简述原因: 。
③除去杂质后的氢氧化钾溶液从液体出口 (填写“A”或“B”)导出。
高三化学填空题中等难度题查看答案及解析
用电解法可提纯含有某些含氧酸根杂质的粗KOH溶液,其工作原理如图所示。下列有关说法错误的是
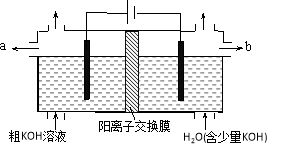
A.阳极反应式为4OH--4e-=2H2O+O2↑
B.通电后阴极区附近溶液pH会增大
C.K+通过交换膜从阴极区移向阳极区
D.纯净的KOH溶液从b出口导出
高三化学选择题中等难度题查看答案及解析
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
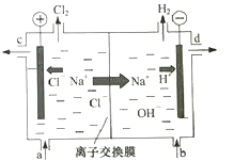
完成下列填空:
(1)写出电解饱和食盐水的离子方程式___。
(2)精制饱和食盐水从图中___位置补充,氢氧化钠溶液从图中___位置流出(选填“a”、“b”、“c”或“d”)。
(3)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。
写出该反应的化学方程式___。
(4)室温下,0.1mol/LNaClO溶液的pH___0.1mol/LNa2SO3溶液的pH(选填“大于”、“小于”或“等于”)。
(5)浓度均为0.1mol/L的Na2SO3和Na2CO3的混合溶液中,SO32-、CO32-、HSO3-、HCO3-浓度从大到小的顺序为___。
已知:H2SO3:Ki1=1.54×10−2,Ki2=1.02×10−7,HClO:Ki1=2.95×10−8,H2CO3:Ki1=4.3×10−7,Ki2=5.6×10−11。
高三化学综合题中等难度题查看答案及解析
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。如图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。

完成下列填空:
(1)写出电解饱和食盐水的离子方程式_______。
(2)离子交换膜的作用为:______、______。
(3)精制饱和食盐水从图中_____位置补充,氢氧化钠溶液从图中_____位置流出(选填“a”、“b”、“c”或“d”)。
高三化学解答题简单题查看答案及解析
电解原理在化学工业中有广泛应用。不仅可以制备物质,还可以提纯和净化。
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离了交换膜只允许阳离子通过,请回答以下问题:
①图中A极要连接电源的_______(填“正”或“负”)极
②精制饱和食盐水从图中_____位置补充,氢氧化钠溶液从图中_____位置流出。(选填“a”“b” “c” “d” “e”或“f”)
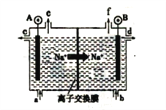
③电解总反应的离子方程式是_____________。
(2)化学在环境保护中起着十分重要的作用,电化学降解法可用于治理水中硝酸盐的污染,电化学降解NO3-的原理如图所示
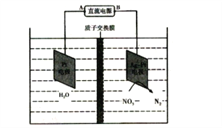
①电源正极为____(填A或B),阴极反应式为_____________。
②若电解过程中转移了5mol电子,则膜左侧电解液的质量变化为__________g。
高三化学填空题中等难度题查看答案及解析